Nachgefragt
Können wir uns das erklären?
Wir haben noch nicht geklärt, warum der anaerobe und der aerobe Prozess verschieden viel Energie freisetzen, oder?
Nein. Wir haben bisher nur festgestellt, dass einmal viel ATP synthetisiert werden kann und einmal wenig.
Gibt es denn Erklärungsansätze auf schulischem Niveau, die uns zumindest ein Muster dahinter erkennen lassen?
Ja und einige davon kennst Du bereits teilweise.
Verschieden genaue Ansätze
Exakt wäre eine Betrachtung der sogenannten „freie Enthalpie“ (ΔG, auch Gibbs-Energie genannt)“ wie in M4. Diese ergibt sich aus zwei wichtigen Größen: Enthalpie (H) und Entropie (S).
Vereinfachend betrachtet man oftmals nur die Enthalpiedifferenz ΔH. Ein großer Teil davon stammt aus den unterschiedlichen Bindungsenthalpien. Um die Größe von ΔH zu berechnen, kann man eine Bilanz der Bindungsenergien aller gebrochenen und neu geknüpften Bindungen in den Molekülen ziehen, wie in M3 gezeigt.
Für eine erste Abschätzung von beiden Größen reicht es uns heute, einfach auf die Polarität der gebrochenen und neu geknüpften Bindungen und die Größe bzw. Anzahl der Moleküle zu achten wie in M2.
Wir probieren das mal im „thinking classroom“.
Erklärung der Methode und konkrete Aufgabe.1
Aufgaben
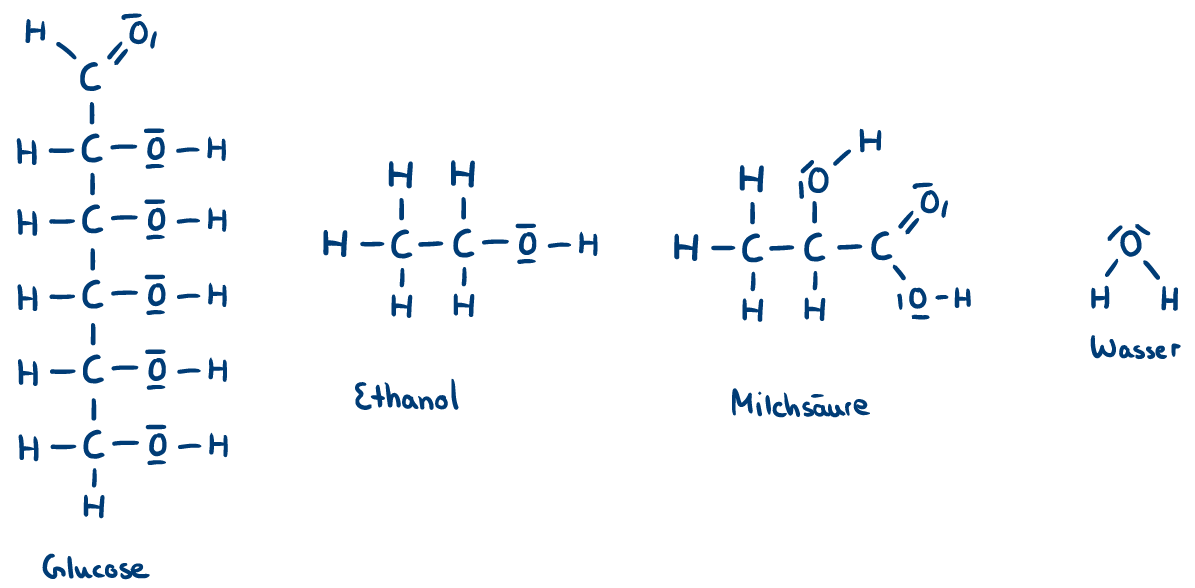
- Erklären Sie mit einer begründenden Abschätzung nach den zwei Faustregeln in M2 die Tatsache, dass beim Abbau von Glucose mit Sauerstoff mehr Energie frei wird als beim Abbau ohne Sauerstoff, in dem Sie
- für beide Reaktionen eine Reaktionsgleichung mit Strukturformeln aller beteiligten Moleküle notieren,
- alle polaren Bindungen in allen Strukturformeln bestimmen und für beide Reaktionen deren Anzahl vor und nach der Reaktion vergleichen.
- Die Zahl und Größe der Moleküle vor und nach der Reaktion vergleichen.
vertiefende Aufgaben
- Die beiden Faustregeln in M2 stellen eine starke Vereinfachung der Aussagen in M4 dar. Ordnen Sie jede Faustregel dem Term in der Gibbs-Helmholtz-Gleichung zu, den diese vereinfachend betrachtet.
Freiwillig
- Geben Sie die formale Reaktionsgleichung der Milchsäuregärung an (1 Molekül Glucose wird in 2 Moleküle Milchsäure zerlegt).
- Formulieren Sie basierend auf den Faustregeln eine begründete Vermutung über die Energieausbeute dieser Reaktion.
- Berechnen Sie nach dem Vorbild in M3 die Energiebilanz in KJ für den aeroben und anaeroben Abbau von 1 Mol Glucose in Hefezellen.
Die Polarität hilft uns vereinfachend
Zwei einfache Faustregeln
Wir können es uns einfacher machen, denn in den von uns betrachteten Fällen helfen uns zwei einfache Faustregeln.
- Entstehen bei der Reaktion insgesamt mehr oder stärker polare Bindungen, ist die Bilanz der Bindungsenergien wahrscheinlich negativ und Energie wird frei.
- Werden große Moleküle in viele kleine Moleküle zerlegt oder z. B. Flüssigkeiten zu Gasen, nimmt die Entropie wahrscheinlich zu und Energie wird frei.
Trifft sogar beides zu, wird höchst wahrscheinlich Energie freigesetzt.
Elektronegativität
Je größer die Elektronegativitätsdifferenz ΔEN zwischen den an der Bindung beteiligten Atomen ist, desto größer ist die Polarität der Bindung.
Erinnere dich: die Werte der Elektronegativität kann man dem Periodensystem entnehmen. Für uns wichtige Elektronegativitätswerte sind: Wasserstoff-Atom (H) 2,1, Kohlenstoff-Atom (C) 2,5, Sauerstoff-Atom (O) 3,5
Die Übergänge zwischen den Bindungstypen sind fließend, die folgenden ΔEN-Werte stellen daher nur einen Richtwert dar:
ΔEN < 0,5 unpolare Elektronenpaarbindung
ΔEN ≥ 0,5 polare Elektronenpaarbindung
ΔEN > 1,5 Ionenbindung
Beispielhafte Anwendung der Faustregeln
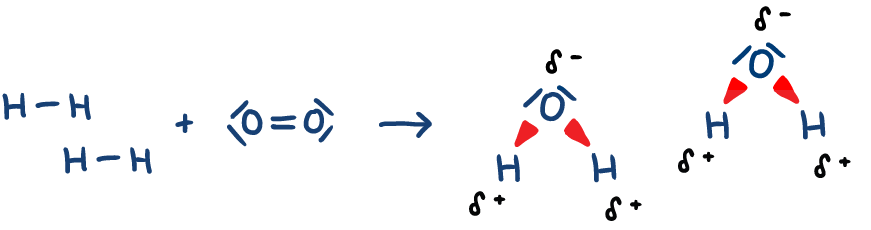
Auf Teilchenebene betrachtet werden bei der sogenannten Knallgasreaktion die unpolaren Bindungen zwischen den Wasserstoff-Atomen und den Sauerstoff-Atomen gespalten. Dabei entstehen polare Elektronenpaarbindungen zwischen den Wasserstoff- und Sauerstoff-Atomen (s. Abb. 3).
Die polaren Bindungen sind durch Keile gekennzeichnet. Die breitere Seite eines Keils zeigt in die Richtung des partial negativ geladenen Atoms.
Hier greift Faustregel Nr. 1 aber Faustregel Nr. 2 nicht. Bei der Reaktion wird dennoch insgesamt Energie frei, obwohl aus drei kleinen Teilchen zwei etwas größere entstehen. Wollte man es genauer betrachten, müsste man sowohl die Enthalpie als auch die Entropie exakt berechnen bzw. bestimmen.
Bilanz von Bindungsenergie
Eine beispielhafte Bilanz
Setzt die Neuknüpfung der Bindungen mehr Energie frei, als zum Brechen der alten Bindungen notwendig war, ist die Reaktion exotherm.
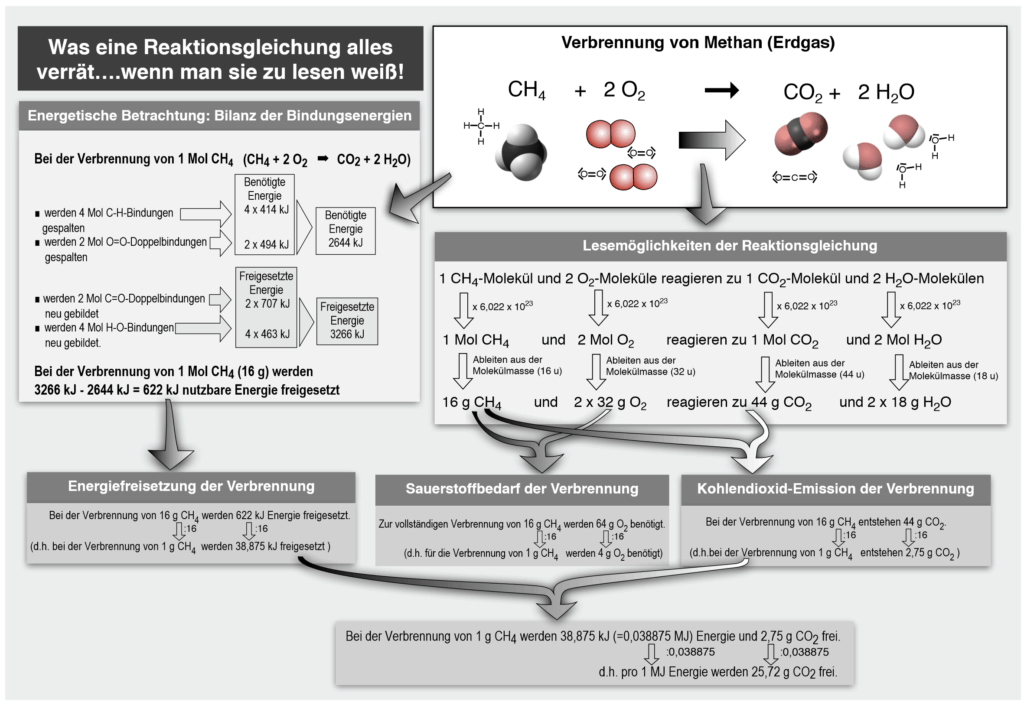
Bilanz am Beispiel der Verbrennung von Methan.2
Die Gibbs-Helmholtz-Gleichung
Ein Blick auf die Gleichung
ΔH gibt die Änderung der Enthalpie (Reaktionsenthalpie) an, und beschreibt, wie viel Wärme bei konstantem Druck von einem System aufgenommen oder abgegeben wird.
T ist die absolute Temperatur (in Kelvin).
ΔS gibt die Änderung der Entropie und beschreibt, wie sehr die „Unordnung“ (oder Freiheit) im System zunimmt oder abnimmt.
Weiteres
Eine Reaktion nennt man exergonisch, wenn sie freiwillig abläuft und dabei freie Energie (Gibbs-Energie, ΔG < 0) freisetzt.
Beide von uns betrachteten Reaktionen (aerober und anaerober Abbau) laufen exergonisch ab, denn es wird in beiden Energie freigesetzt. Erstere liefert aber viel mehr Energie, vor allem weil der Term ΔH größer ist.
Eine Reaktion ist endergonisch, wenn sie nicht freiwillig abläuft und Energie zugeführt werden muss (ΔG > 0). So ist beispielweise die Umwandlung von Lactat zu Glucose in der Leber (Gluconeogenese) ein endergonischer Prozess: Der Körper muss hier Energie aufwenden, um aus Lactat wieder Glucose herzustellen.