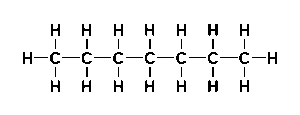Zwischenmolekulare Wechselwirkungen? Das hatten wir doch schon, oder?
Übersicht
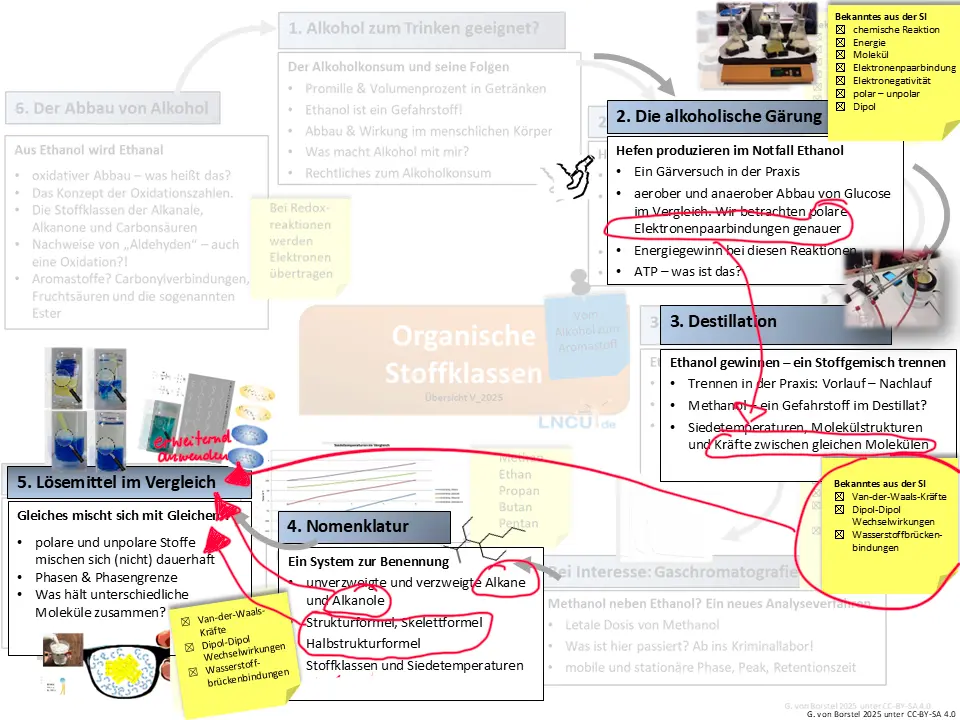
Was rückt nun in den Fokus? 2
Ein einfaches System zum Einstieg
Wir haben doch schon mit Hilfe der zwischenmolekulare Wechselwirkungen die Siedetemperaturen erläutert, oder?
Ja, korrekt. Da ging es in der Regel um Wechselwirkungen zwischen gleichen Molekülen. Die selben Gedanken und Erklärungen können wir aber auch verwenden, wenn wir uns überlegen, warum die Moleküle verschiedener Stoffe (nicht) gut zusammenhalten.
Aufgaben
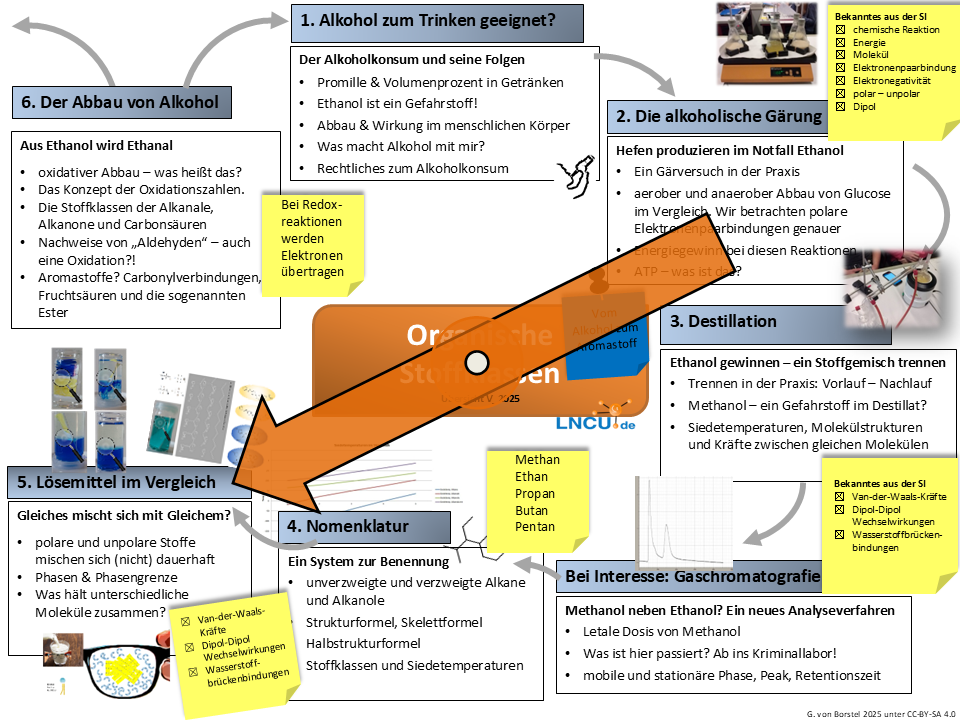
- Beschreiben Sie das in Galerie 1 abgebildete Szenario.
- Stellen Sie einen sinnvollen Zusammenhang zwischen der Havarie eines Schiffes, dessen Tank leck schlägt, und der Kapitelüberschrift her.
Öl und Wasser - was passiert da?
Löslichkeiten und Mischbarkeiten
Was rückt nun in den Fokus? 3
Ein einfaches System zum Einstieg
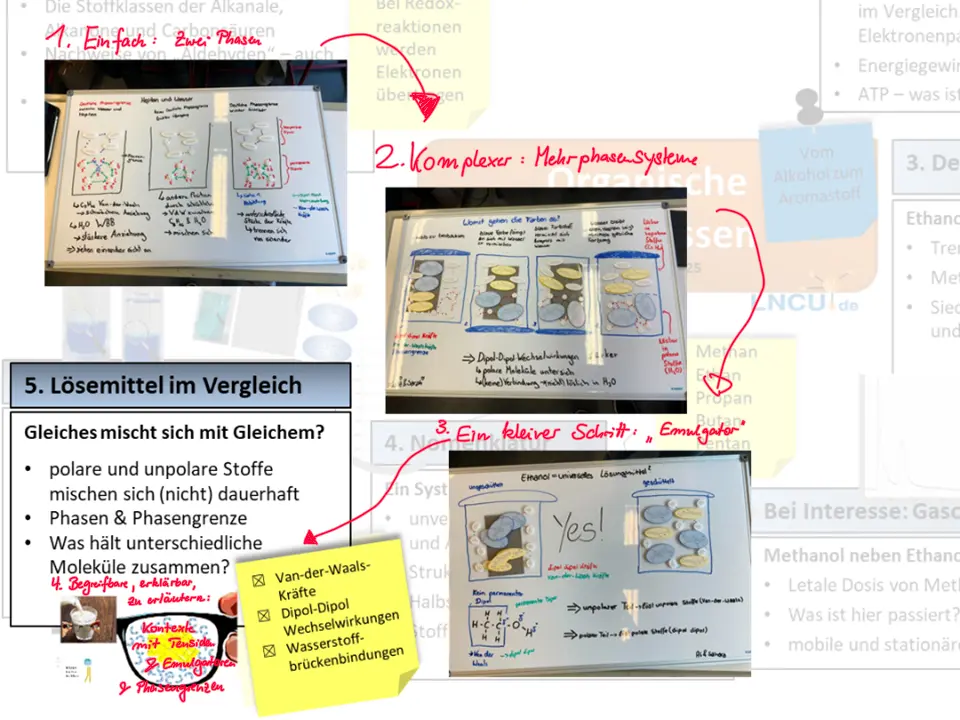
Wir wollen im Folgenden mit Hilfe eines Modellversuchs unter Verwendung von Teilchendarstellungen nachvollziehen, warum sich Heptan nicht dauerhaft mit Wasser mischen lässt.
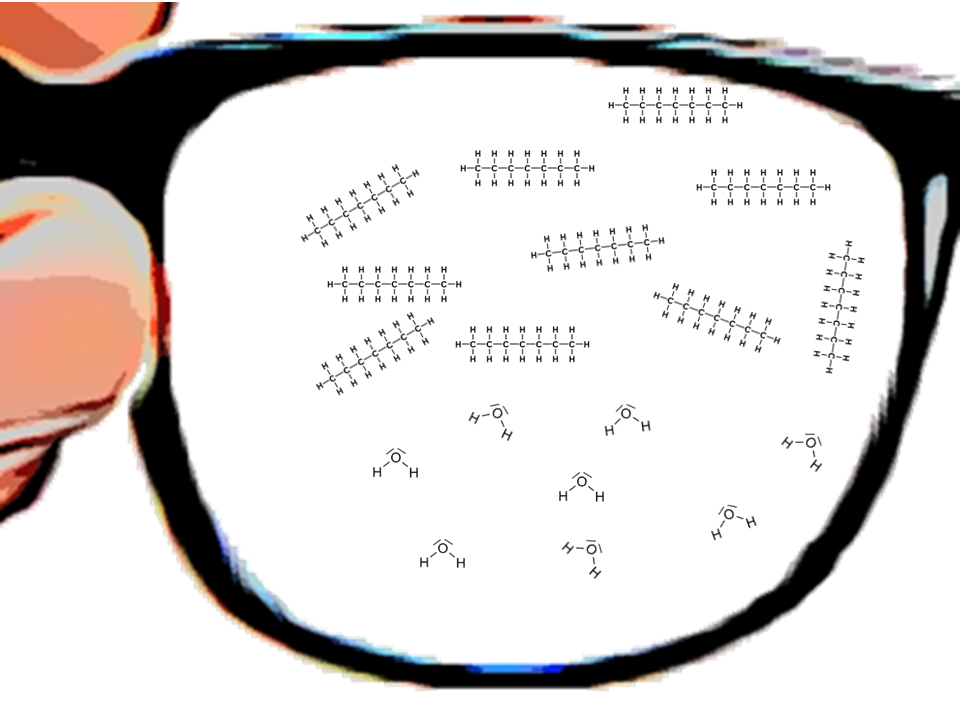
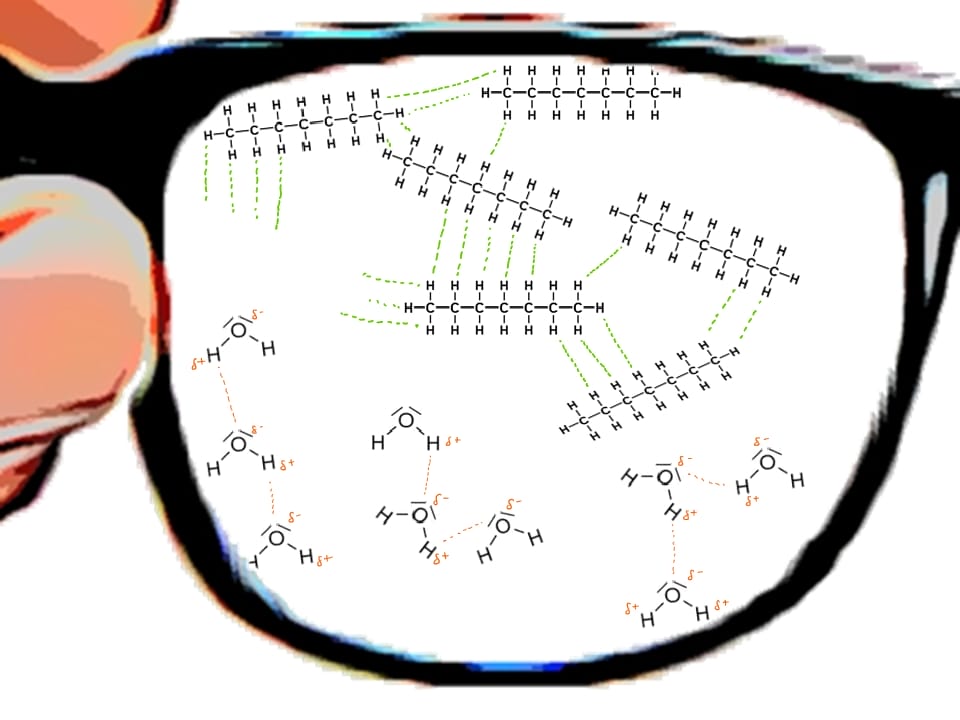
Unsere Erläuterungen werden auf Teilchenebene erfolgen
Ein Blick durch unsere Teilchenbrille.4
Aufgaben
- Führen Sie den Modellversuch V1 durch. Betrachten Sie gegebenenfalls zusätzlich das Video V1.
- Beschreiben Sie ihre Beobachtungen unter der Verwendung des Fachbegriffs Phasengrenze, den Sie recherchieren.
- Betrachten Sie die drei Fotos zu den ausgewählten Zeitpunkten 1 bis 3 in M3. Erstellen Sie analog zu dem bereits dargestellten Teilchenmodell für den ersten Zeitpunkt die noch fehlenden Darstellungen auf Teilchenebene für die anderen beiden Situationen. Nutzen Sie dazu bevorzugt „haptische“ Modelle. Halten Sie ihre Darstellungen der Teilchenebene als Bild fest.
- Zeichnen Sie in ihre Abbildungen Teilladungen und zwischenmolekulare Kräfte z. B. in Form von Pfeilen exemplarisch ein.
- Bereiten Sie sich darauf vor, die Beobachtungen mit Hilfe der Darstellungen verbal zu erläutern.
Versuch
Materialien
- Schutzbrille
- Schnappdeckelglas mit Deckel
- ggf. haptische Teilchenmodelle
- für die Darstellung zur Versuchsauswertung
Chemikalien
-
Heptan
- Anstelle von Mineralöl nutzen wir im Versuch Heptan.
- Wasser
Aufbau und Entsorgung
Beide Flüssigkeiten wurden zuvor von der Lehrperson eingefüllt. Das Glas ist aufgrund des Gefährdungspotentials von Heptan verschlossen und muss verschlossen bleiben.
Geben Sie nach dem Versuch das verschlossene Glas zurück. Wir verwenden es für Folgeversuche.
Durchführung
- Betrachten Sie zunächst das mit Heptan und Wasser gefüllte Gefäß. Schütteln Sie dann das verschlossene Gefäß kräftig für mehrere Sekunden. Stellen Sie es ab und beobachten Sie für 20 Sekunden.
- Führen Sie den Versuch erneut durch und halten Sie Beobachtungen zu prägnanten Zeitpunkten fotografisch und in Worten fest.
Videografie des Versuchs
Alternativ bzw. additiv: Video des Versuchs5