Material
Weiteres
Im Körper eines Menschen zirkulieren rund 6 Liter Blut – eine relativ empfindliche Flüssigkeit mit einem pH-Wert von etwa 7,4. Doch was würde passieren, wenn jemand eine ganze Zitrone isst und die gesamte Säure direkt ins Blut gelangt? Könnte eine einfache Zitrusfrucht tödlich sein?
Eine durchschnittliche Zitrone enthält rund 60 mL Saft. Darin gelöst sind etwa 3,6 g reine Zitronensäure. Mit einem pKS-Wert von 3,13 dissoziiert nur ein Bruchteil der Säure – rund 0,1 %. Trotzdem reicht diese Menge aus, um den pH-Wert des Blutes von 7,4 auf 5,5 abzusenken: Zwei pH-Einheiten Unterschied – genug, um das Leben eines Menschen zu beenden.
Doch keine Sorge: Dank seiner Pufferwirkung bleibt der pH-Wert des Blutes nahezu stabil – egal, wie viele Zitronen man isst. Zum Glück, sonst wäre jede Limonade ein tödliches Getränk!
Weiteres

Zitronen als potentielle Mordwaffe?1
Aufgaben
- Notieren Sie ihre Beobachtungen zu den vier Demoversuchen in V1. Erklären Sie diese, auch unter Zuhilfenahme von M2.
- Vollziehen Sie rechnerisch nach, warum der pH-Wert des Blutes eines Menschen – nach dem Verzehr einer Zitrone – gemäß M1 von 7,4 auf 5,5 theoretisch sinken müsste.
Lösung zu A2
Eigenschaften eines Essigsäure-Natriumacetat-Gemisches
Materialien
- Schutzbrille
-
2 100 mL Bechergläser
- 1 250 mL Becherglas
- Pipette
- Spatel
- Waage
Chemikalien
- Essigsäure 1 mol/L
- Natriumacetat
- dest. Wasser
- Universalindikator-Lösung
Entsorgung
Am Ende alle Flüssigkeiten vereinen und über den Abguss entsorgen.
Die folgenden vier Versuche werden als Demoversuche durch die Lehrkraft vorgeführt.
Versuch 1
Lässt sich der pH-Wert vorhersagen?
Ja, weil der pKS-Wert der Essigsäure bekannt ist. Dieser beträgt 4,76. Essigsäure ist demnach eine schwache Säure, weshalb hier die Formel zur pH-Wert-Berechnung von schwach Säuren herangezogen werden kann:
Versuch 2
- In ein weiteres Becherglas so viel festes Natriumacetat in 50 mL dest. Wasser auflösen, dass die Konzentration ebenfalls 1 mol/L ergibt.
- Einige Tropfen Universalindikator-Lösung hinzufügen und den pH-Wert mittels pH-Meter ermitteln.
Wie viel Gramm Natriumacetat werden hierfür benötigt?
Zunächst wird berechnet, wie groß die Stoffmenge (n) an Natriumacetat in 50 mL Lösung bei einer Konzentration von 1 mol/L ist. Danach wird die Stoffmenge in eine Stoffmasse (m) umgerechnet. Hierfür wird die molare Masse von Natriumacetat herangezogen.
Versuch 3
- Zu 50 mL Essigsäure der Konzentration 1 mol/L wird so viel festes Natriumacetat zugegeben, sodass die Lösung 1 mol/L Essigsäure UND 1 mol/L Natriumacetat enthält.
- Einige Tropfen Universalindikator-Lösung hinzufügen und den pH-Wert mittels pH-Meter ermitteln.
Lässt sich der pH-Wert vorhersagen?
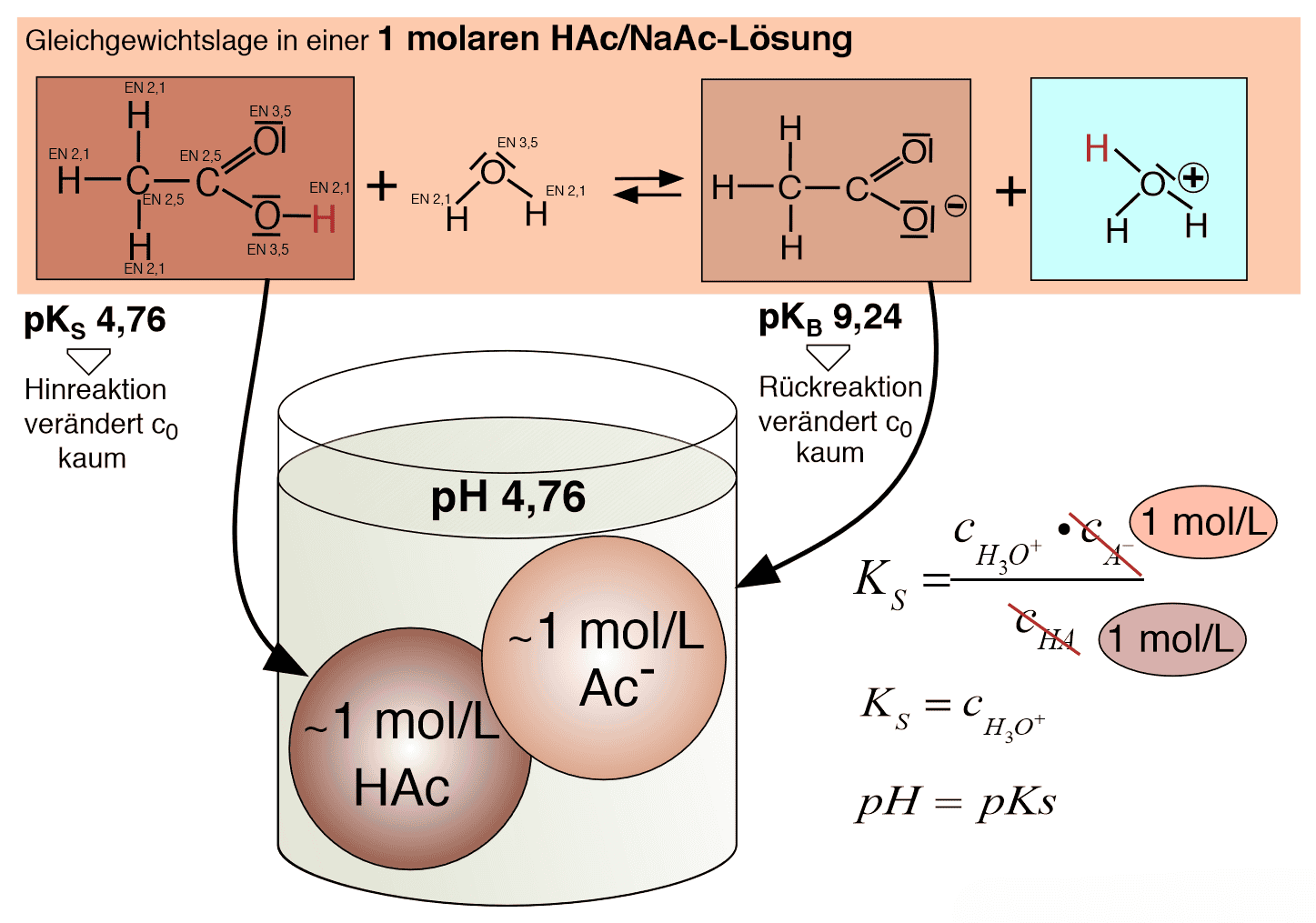
Ja, der pH-Wert lässt sich vorhersagen. Das Acetat-Ion des Salzes Natriumacetat ist die korrespondierende schwache Base zur schwachen Essigsäure. Da das Verhältnis beider Stoffe 1:1 ist, entspricht der pH-Wert der Lösung dem pKS-Wert der Säure, also 4,76.
Versuch 4
- 25 mL Essigsäure der Konzentration 1 mol/L und 25 mL Natriumacetat-Lösung der Konzentration 1 mol/L werden zusammen in ein Gefäß gegeben.
- Weitere 100 mL Wasser werden hinzugegeben.
- Einige Tropfen Universalindikator-Lösung hinzufügen und den pH-Wert mittels pH-Meter ermitteln.
Lässt sich der pH-Wert vorhersagen?
Selbstverständlich lässt sich der pH-Wert vorhersagen: Er entspricht erneut dem pKS-Wert der Essigsäure, also 4,76. Das liegt daran, dass die Zugabe von 100 mL Wasser die Konzentrationen beider Stoffe, Essigsäure und Natriumacetat, gleichermaßen senkt (Verdünnung). Ihre Konzentrationen sind zueinander also nach wie vor 1:1.
Hilfen zur Veranschaulichung
Weiteres
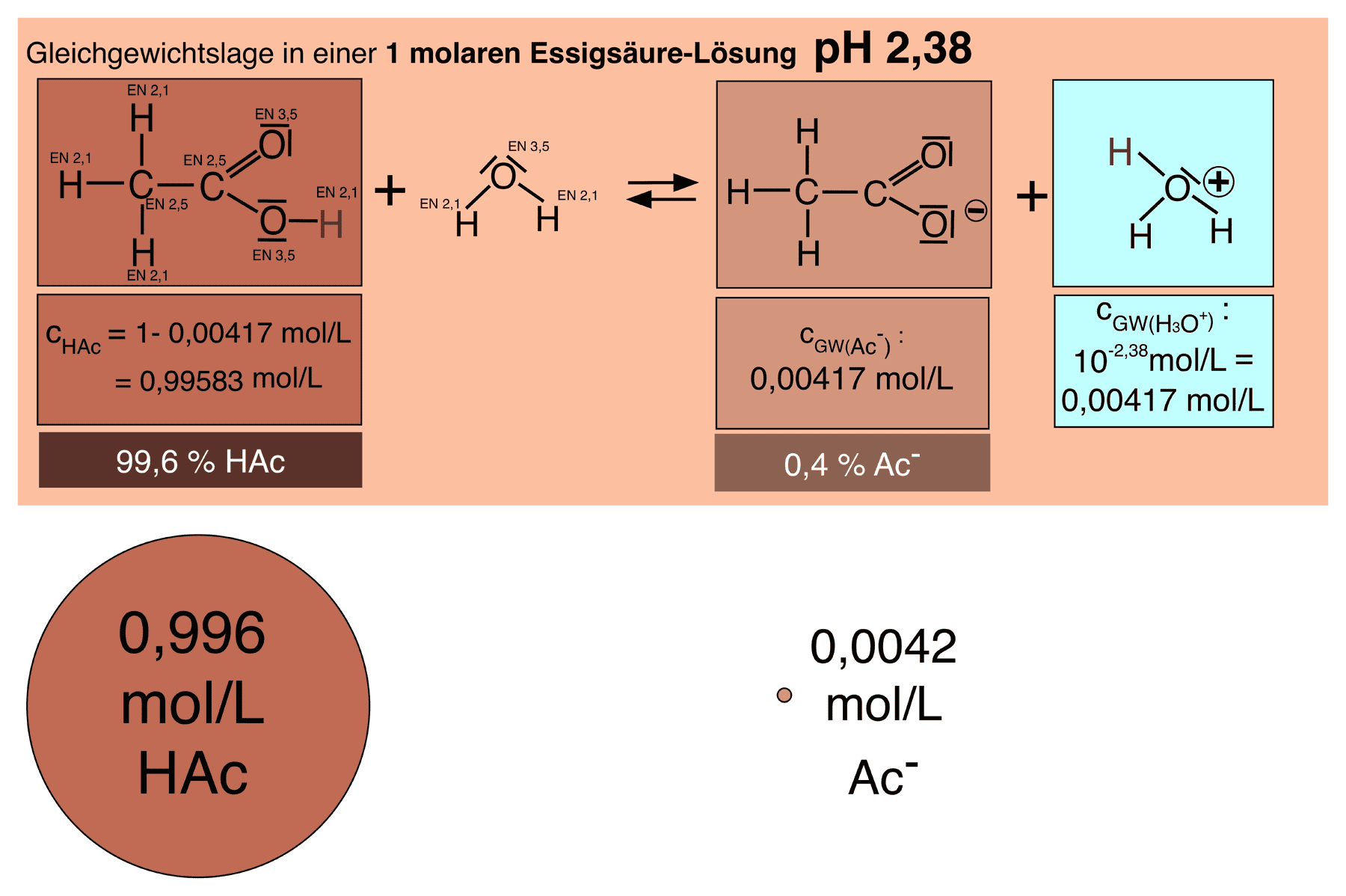
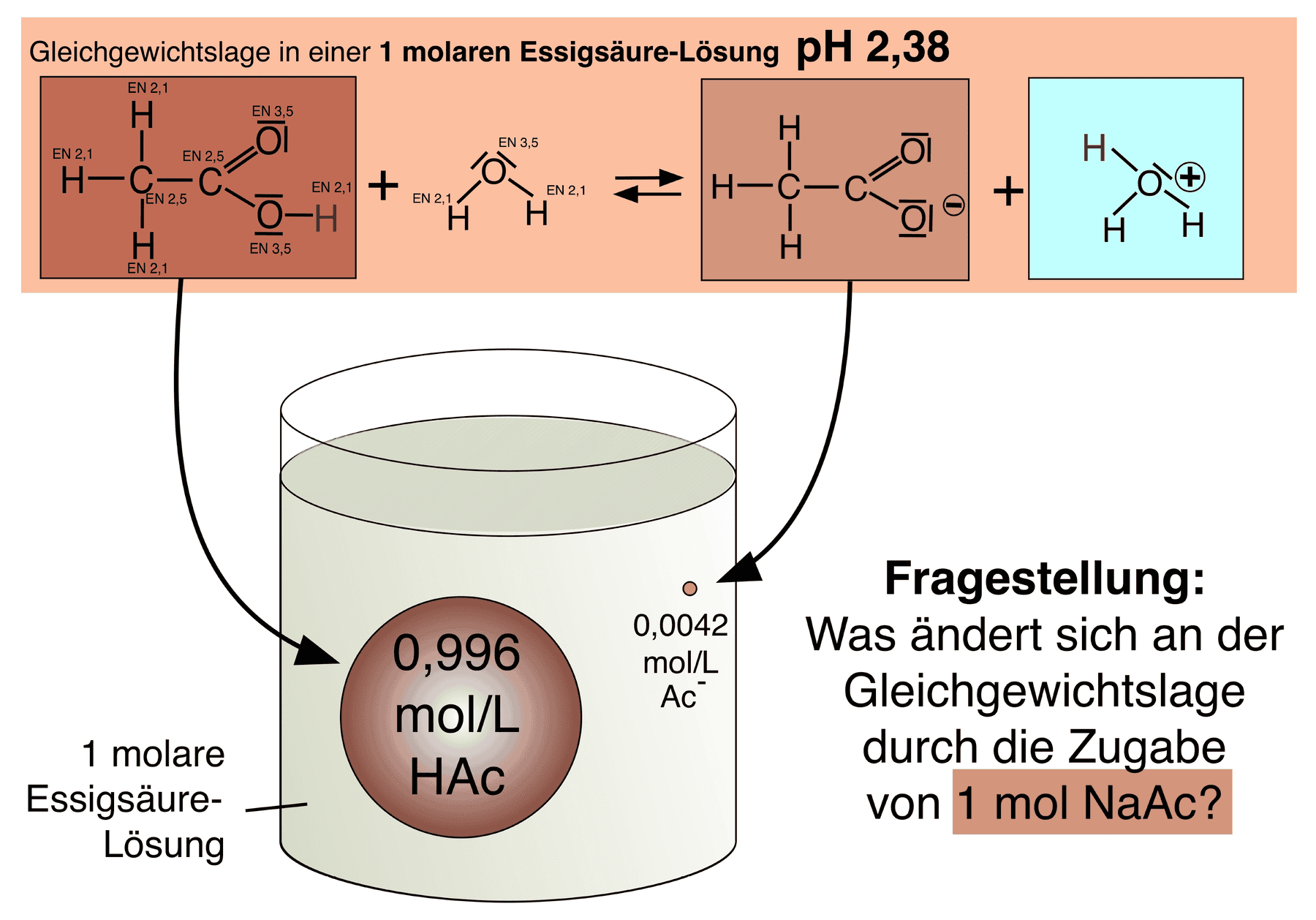
Skizzen zur Gleichgewichtslage verschiedener Lösungen.2