Aufgaben
- Führen Sie den Versuch V1 zunächst mit Salzsäure und bei genügend Zeit auch mit Natronlauge durch.
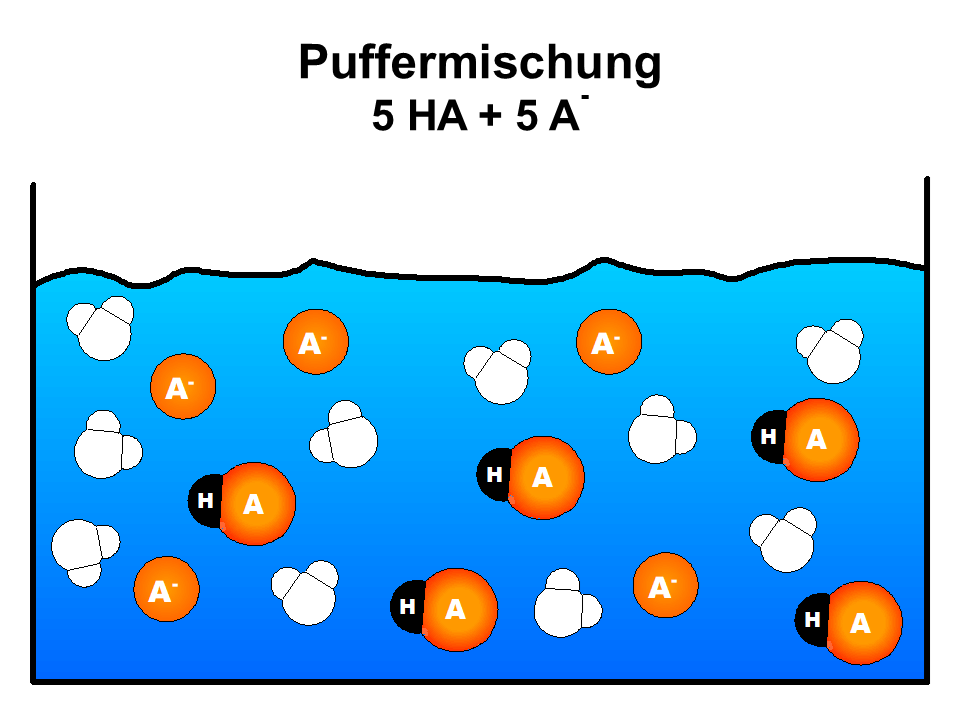
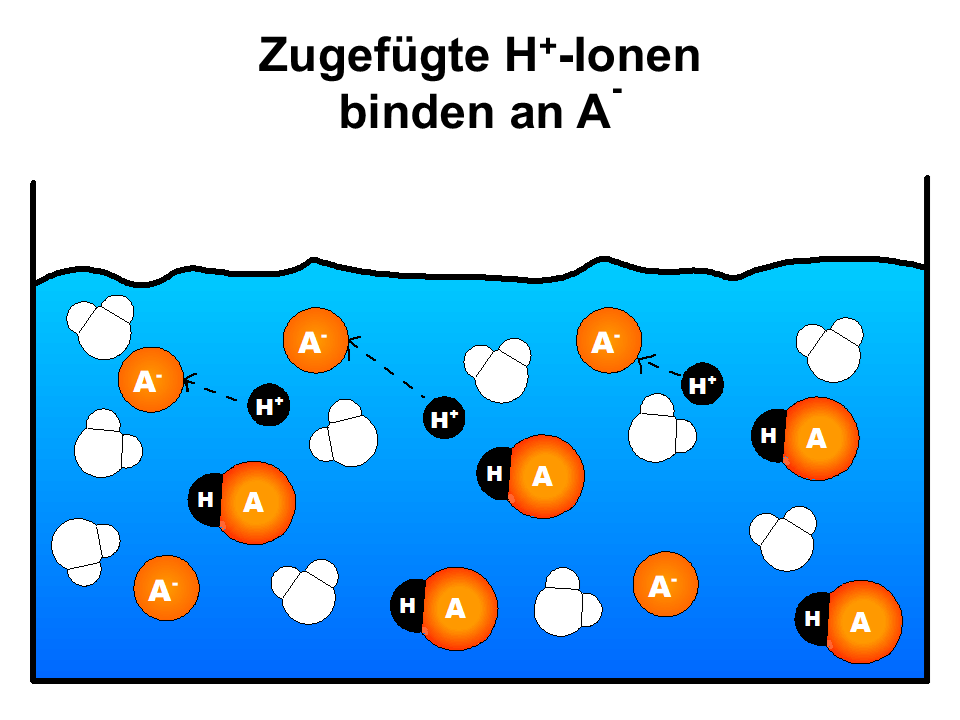
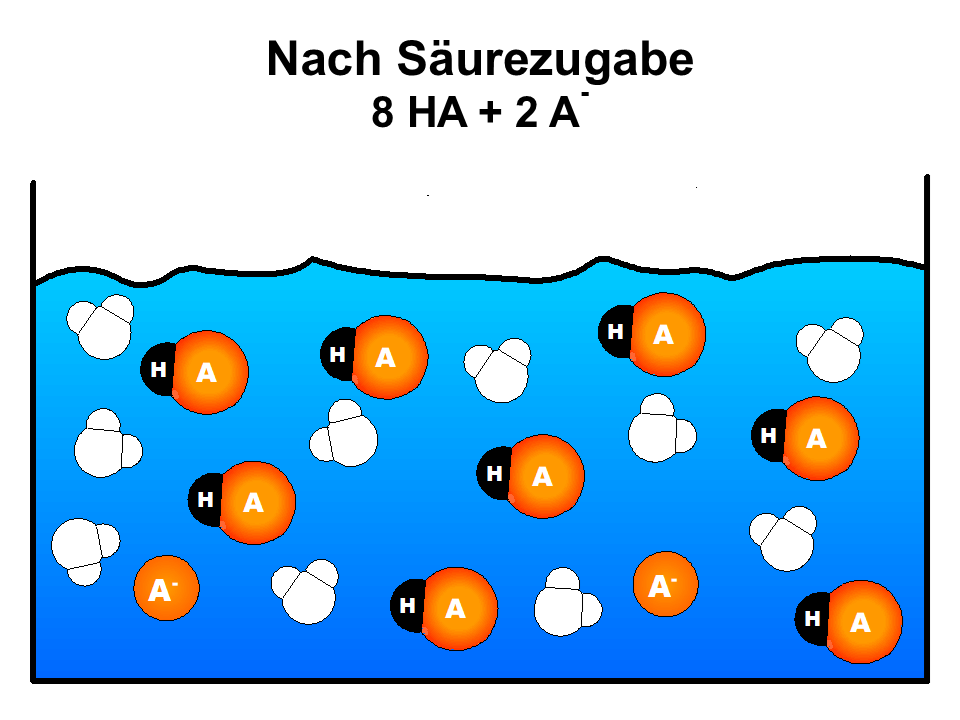
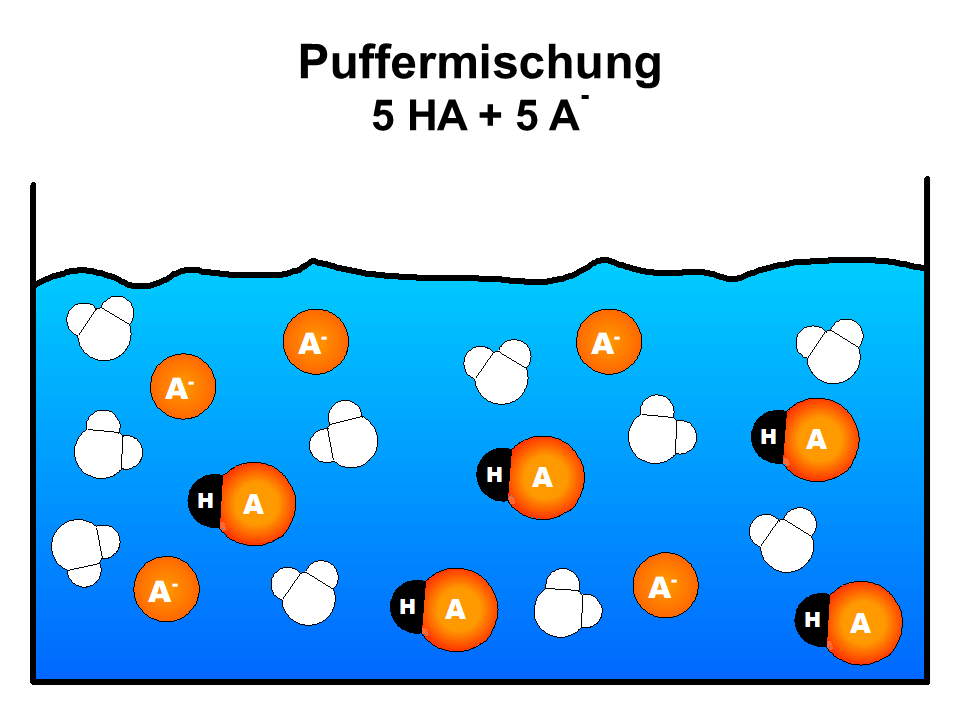
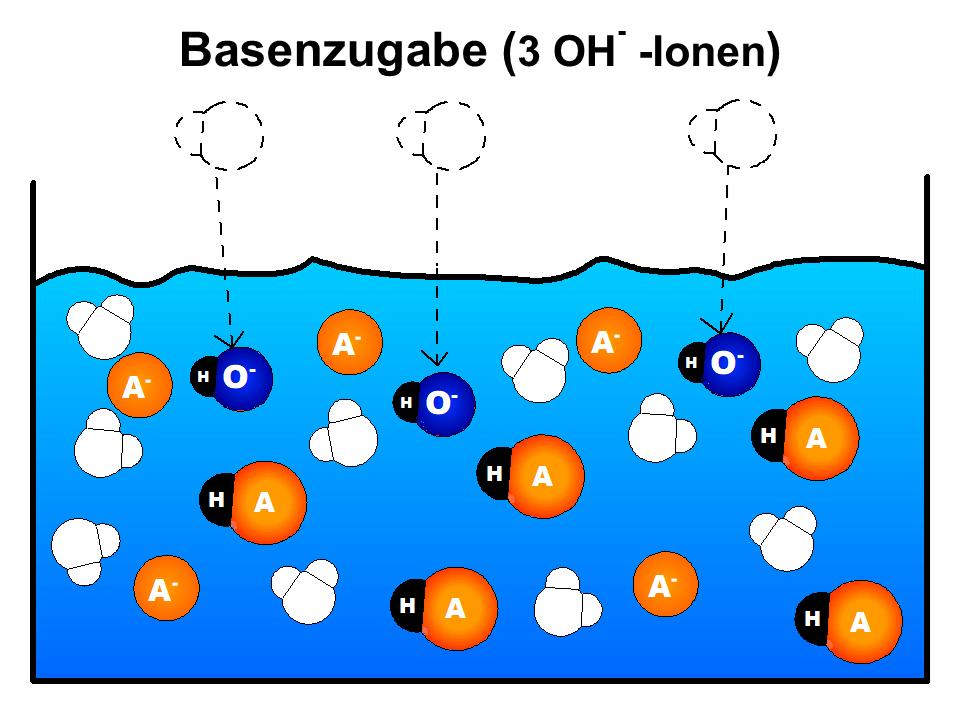
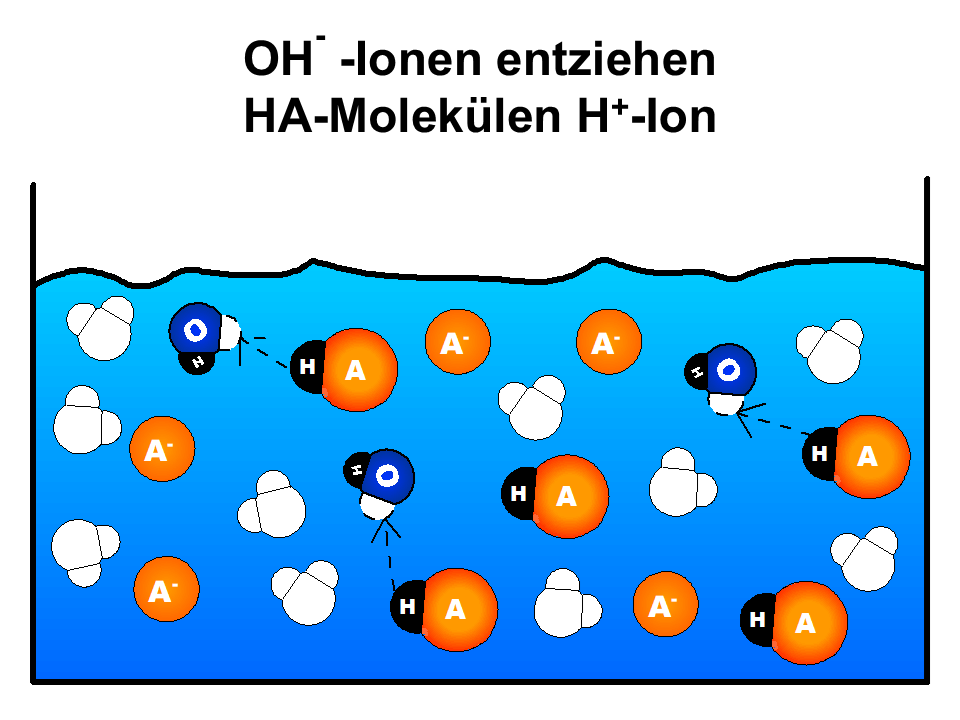
- Betrachten Sie das vereinfachte Teilchenmodell in M1 und verdeutlichen Sie sich mit ihrer Hilfe die prinzipielle Wirkungsweise von Puffern. Bereiten Sie sich auf eine kurze Präsentation vor.
- Das Teilchenmodell in M1 ist stark vereinfacht. Würde dies stimmen, wäre der pH-Wert der Lösung 7 und er würde sich bei Zugabe von Säure oder Lauge gar nicht ändern. Überlegen Sie, was das Modell nicht zeigt, was aber erklären würde, warum der pH-Wert am Anfang ungleich 7 ist und sich zunächst nur geringfügig ändert.
Lösungen
Die Wirkungsweise von Puffern beruht prinzipiell auf zwei Fällen:
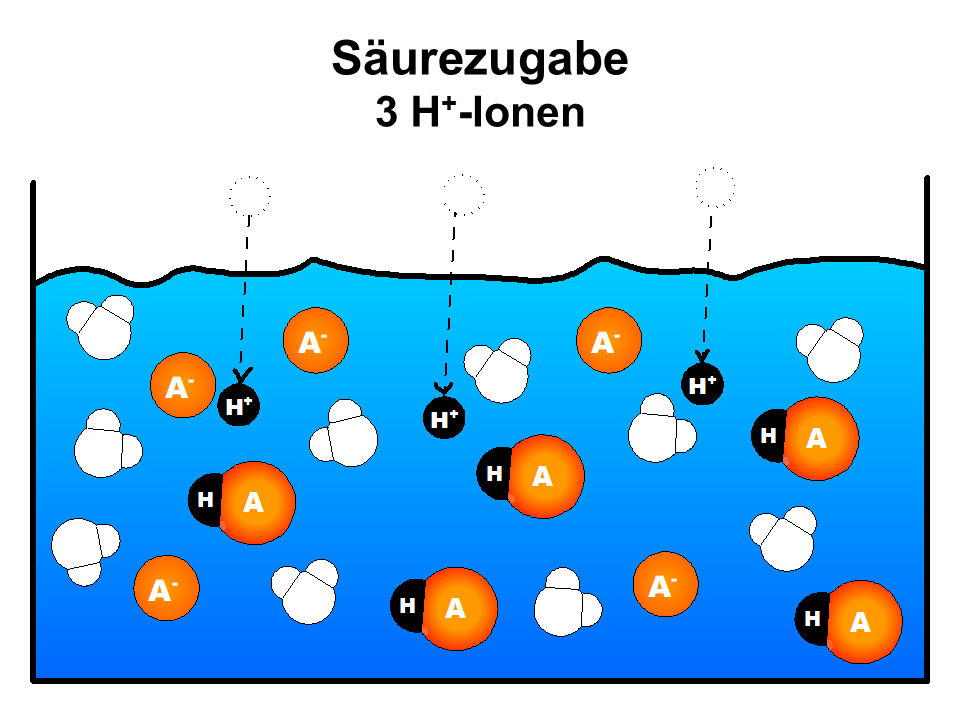
- Zugefügte Protonen werden von den im Puffer enthaltenen Base-Teilchen gebunden
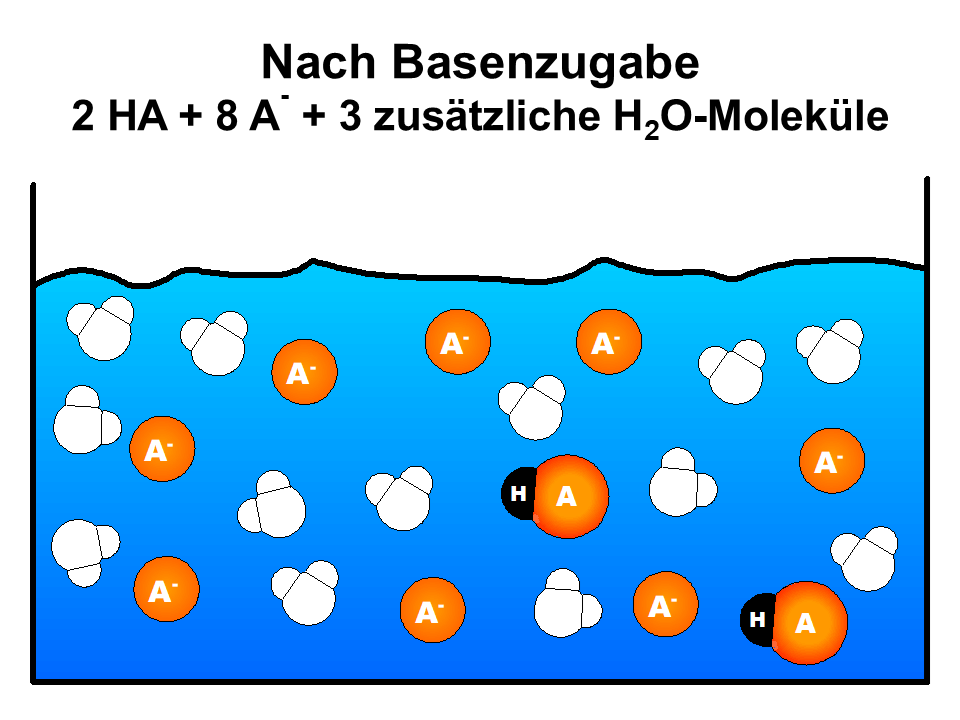
- Zugefügte Hydroxid-Ionen reagieren mit den im Puffer enthaltenen Säure-Teilchen zu Wasser
In beiden Fällen verändert sich so der pH-Wert kaum, weil die Wirkung der zugegebenen Säure- oder Base-Teilchen auf diese Art und Weise neutralisiert/abgepuffert wird.
Das Teilchenmodell in M1 ist zu grob. Es zeigt lediglich die Säure-Base-Reaktion qualitativ, verschweigt aber…
- … das Gleichgewicht zwischen der Puffer-Säure und ihrer korrespondierenden Puffer-Base.
- … die Abhängigkeit der Gleichgewichtslage der Protolysegleichgewichtsreaktion von der Säurestärke der Puffer-Säure (= pKS-Wert)
- … die Abhängigkeit des pH-Wertes von dem Mengenverhältnis des korrespondierenden Säure-Base-Paares des Puffers.
Deshalb ist der Anfangs-pH in der Regel ungleich 7 und bei kleiner Zugabe ändert er sich nur wenig, weil sich hauptsächlich das Verhältnis der Konzentrationen des korrespondierenden Säure-Base-Paares leicht verschiebt. Erst bei erschöpfter Komponente bricht die Pufferwirkung zusammen und der pH-Wert ändert sich stark.
Pufferwirkung eines Essigsäure-Acetat-Gemisches
Materialien
- Schutzbrille
- 5 50 mL Bechergläser
- Pipette
- Spatel
-
pH-Meter
- Optional
Chemikalien
-
Essigsäure 1 mol/L
- Je Gruppe 40 mL
- Salzsäure 1 mol/L
- Natronlauge 1 mol/L
-
Natriumacetat oder Natriumacetat-Trihydrat
- Je Gruppe werden 2,3 g bzw. 3,81 g (als Trihydrat) benötigt
- Universalindikator-Lösung
Aufräumen
Später alle Flüssigkeiten vereinen und über den Abguss entsorgen. Gegenstände spülen und an ihren Ursprung zurückstellen.
Aufbau
Skizze zum Aufbau.1
Durchführung
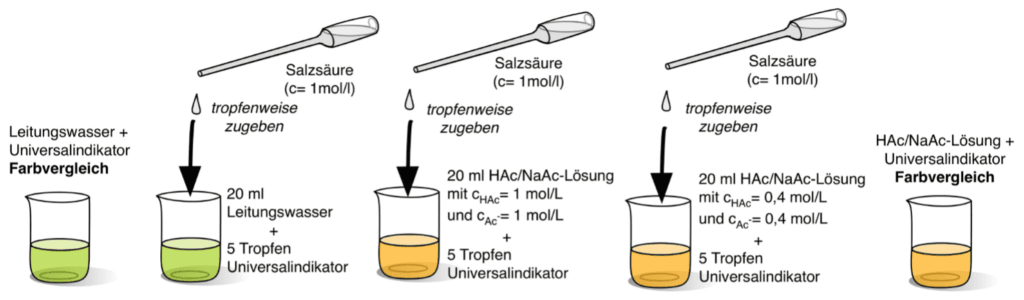
- Becherglas 1 + 2: 20 mL Leitungswasser + 5 Tropfen Universalindikator (Farbvergleich)
- Becherglas 2: Wie Becherglas 1
- Becherglas 3: 20 mL Essigsäure der Konzentration 1 mol/L + 1,64 g Natriumacetat (oder 2,72 g als Trihydrat) + 5 Tropfen Universalindikator
- Becherglas 4: 8 mL Essigsäure der Konzentration 1 mol/L + 12 mL dest. Wasser + 0,66 g Natriumacetat (oder 1,09 g als Trihydrat) + 5 Tropfen Universalindikator
- Becherglas 5: Wie Becherglas 3 (Farbvergleich)
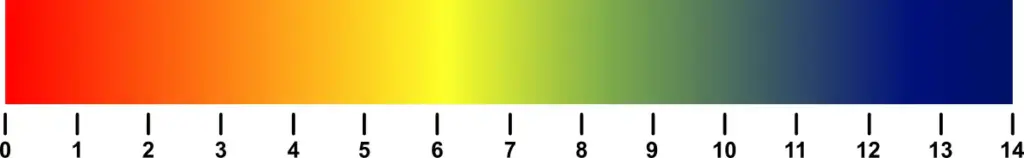
In den Bechergläsern 2 – 4 so lange dieselbe Anzahl an Tropfen Salzsäure (oder Natronlauge) portionsweise hinzugeben und den pH-Wert der Lösung erfassen, bis sich dieser merklich ändert. Die Messwerte gemäß der Vorlage tabellarisch notieren. Der pH-Wert kann mittels der Farbe des Universalindikators gemäß Abb. 1 optisch ermittelt werden oder auch zusätzlich digital mittels pH-Meter.
Hintergrund zu den Werten

Teilchenmodell
Weiteres
Stark vereinfachte Visualisierung der Pufferwirkung auf Teilchenebene.
Aufgaben zu M2
- Erläutern Sie mit Hilfe von M2, inwiefern man bei Kenntnis der Konzentrationen innerhalb der Pufferlösung den pH-Wert der Lösung berechnen kann.
- Geben Sie Beobachtungen aus V1 an, die man mit Hilfe von M2 erklären kann.
- Erklären Sie, warum man für einen Puffer eine schwache Säure benötigt, deren korrespondierende Base ebenfalls schwach ist.
Lösungen
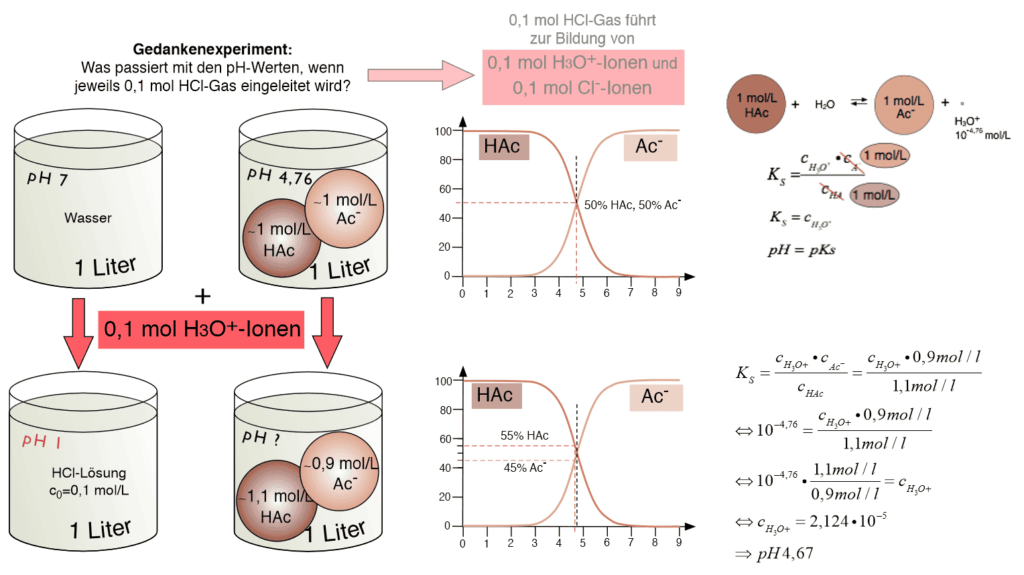
Bei Kenntnis der Konzentrationen innerhalb der Pufferlösung lässt sich der pH-Wert der Lösung mit Hilfe des Massenwirkungsgesetzes berechnen:
Die folgende Logarithmusregel führt zum letzten Umformungsschritt:
Ein Puffer kann nur dann wirken, wenn Säure und Base gleichzeitig in nennenswerter Menge nebeneinander existieren. Das ist nur bei schwachen Säuren und ihren korrespondierenden schwachen Basen der Fall, weil sie nicht vollständig reagieren/protolysieren, sondern ein Gleichgewicht bilden gemäß:
- Eine starke Säure würde nahezu vollständig zu H+ und A– dissoziieren – es bliebe kein HA mehr übrig.
- Eine starke Base würde alle Protonen sofort binden – das Gleichgewicht wäre zerstört.
Nur bei schwachen Säuren/Basen bleibt das Gleichgewicht erhalten, weil beide Formen in nennenswerter Menge gleichzeitig existieren. Dadurch kann sich das Gleichgewicht bei Zugabe von Protonen oder Hydroxid-Ionen verschieben und den pH stabil halten.
pH-Wert-Änderung des Puffers
Weiteres
Visualisierung zur Pufferwirkung: pH-Wert-Veränderung.1
Aufgaben zu M3
- Beschreiben Sie die Diagramme in M3. Geben Sie an, welche weitergehenden Aspekte die Diagramme im Vergleich zum einfachen Teilchenmodell in M1 berücksichtigen.
- Geben Sie Beobachtungen aus V1 an, die man mit Hilfe von M3 erklären kann.
Lösungen
Beschreibung
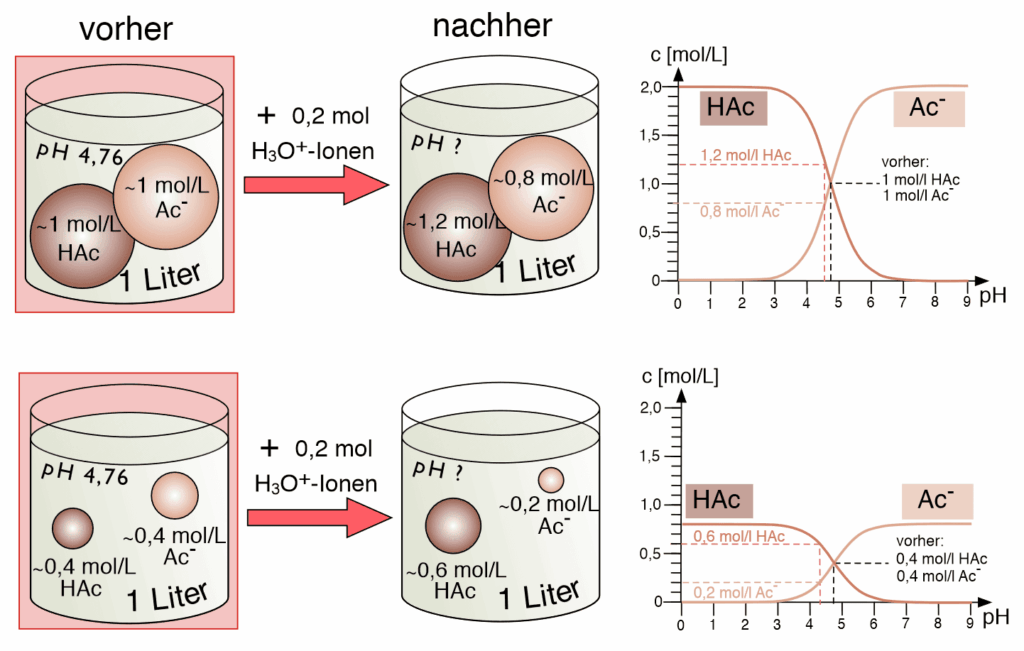
Die Diagramme beziehen sich auf zwei Pufferlösungen aus Essigsäure und Acetat unterschiedlicher Konzentration vor und nach der Zugabe von 0,2 mol Oxonium-Ionen.
- Im oberen Beispiel enthält die Lösung je 1 mol/L Essigsäure und Acetat. Nach Zugabe der Säure reagieren die Oxonium-Ionen mit Acetat zu Essigsäure HAc. Dadurch entstehen 1,2 mol/L HAc und 0,8 mol/L Ac–. Der pH-Wert sinkt nur geringfügig – der Puffer wirkt stark.
- Im unteren Beispiel enthält die Lösung eine deutlich geringere Konzentration an Essigsäure und Acetat, nämlich jeweils nur 0,4 mol/L. Nach derselben Säurezugabe entstehen 0,6 mol/L HAc und 0,2 mol/L Ac–. Der pH-Wert sinkt deutlich stärker – der Puffer wirkt schwächer.
Die Diagramme zeigen die Konzentrationsverläufe von HAc und Ac– in Abhängigkeit vom pH-Wert (und umgekehrt). Bei pH = 4,76 (pKS der Essigsäure) liegen beide Stoffe in gleicher Konzentration vor. Nach Zugabe der Säure verschiebt sich das Verhältnis der Konzentrationen des korrespondierenden Säure-Base-Paares entsprechend.
Weitergehende Aspekte
Im Gegensatz zum vereinfachten Teilchenmodell aus M1 berücksichtigen die Diagramme folgende Punkte:
- Chemisches Gleichgewicht zwischen HAc und Ac–
- Pufferkapazität (ein konzentrierterer Puffer hat eine stärkere Pufferwirkung).
Pufferkapazität
Weiteres
Visualisierung zur Pufferwirkung: Pufferkapazität.1