Aufgaben
- Erarbeite Dir mit Hilfe von M1 die Fakten zur Entdeckung, zu den stofflichen Eigenschaften und zur Verwendung der Edelgase. Stelle heraus, was sie so besonders macht.
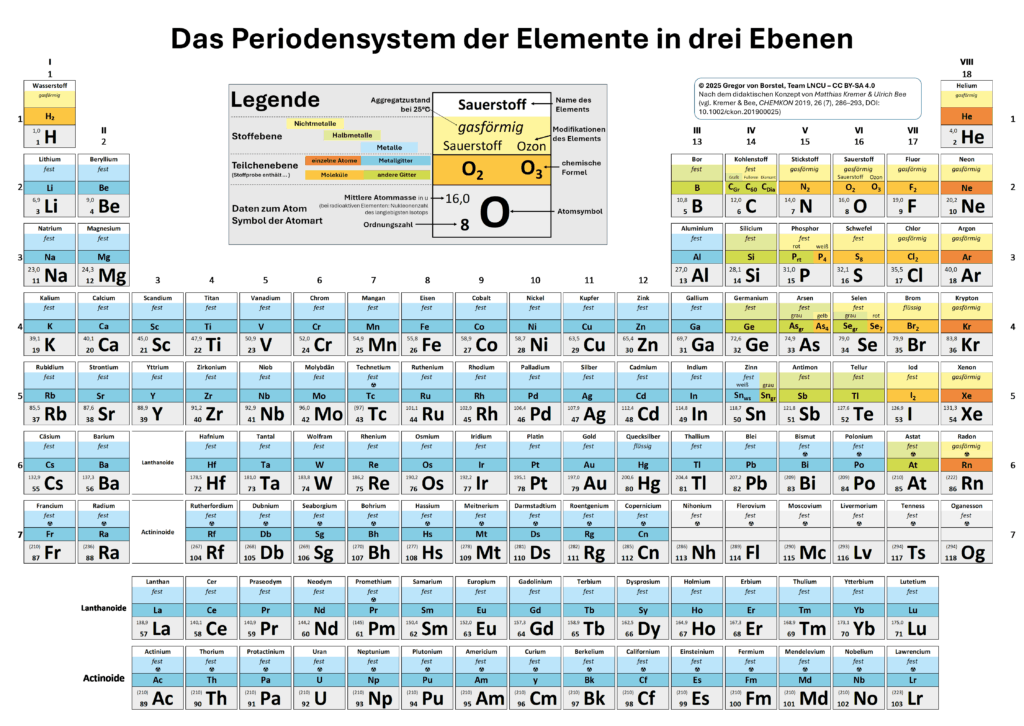
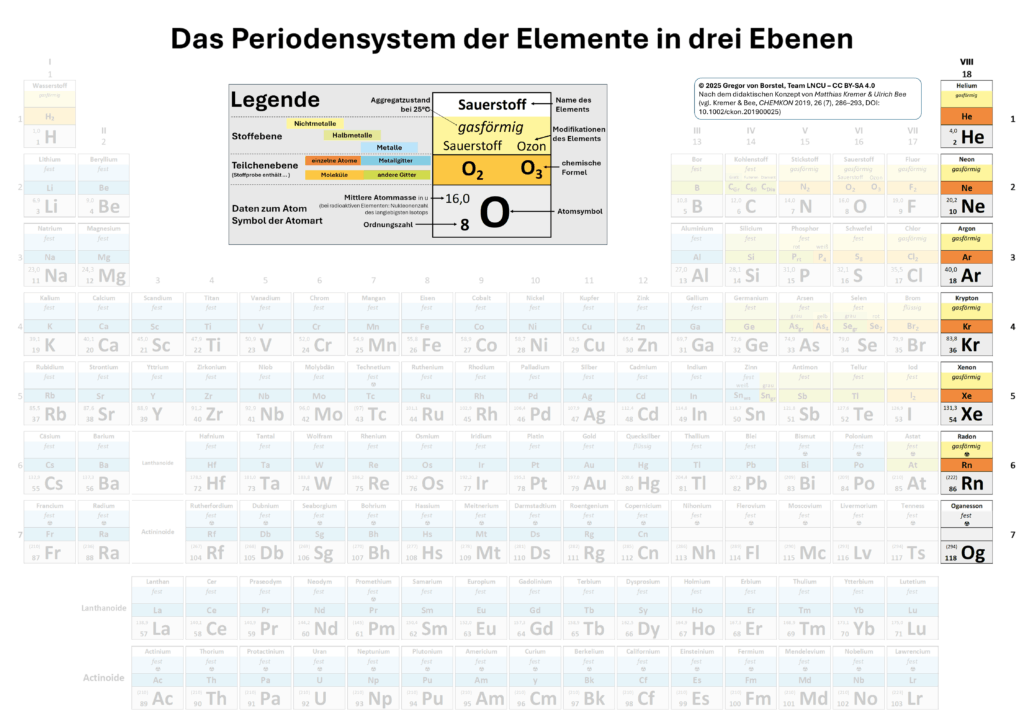
- Schaue in das PSE3 in M2, nutze die Legende und halte fest, was das Besondere der Zusammensetzung der Stoffproben aller Edelgase auf Teilchenebene ist.
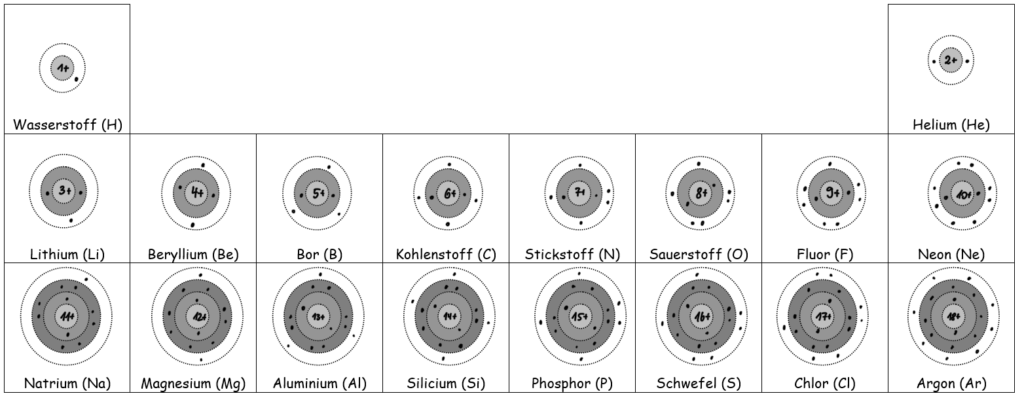
- Betrachte das Schalenmodell in M2 und stelle auch hier das Besondere an den Edelgasen heraus.
- Lade dir die Vorlage für den Steckbrief aus M2 herunter und fülle diese aus.
- Formuliere einen denkbaren Zusammenhang zwischen dem atomarem Aufbau, der Teilchenebene und Stoffebene.
Weitergedacht
- Erkläre, was man in dem Video zum Elektroschweißen mit und ohne Schutzgas sieht.
Entdeckung und Verwendung
Ein Wettlauf der Entdeckungen
Gehen wir noch einmal zurück in das Jahr 1894! Lord Rayleigh, ein Physiker, entdeckt etwas Merkwürdiges: Stickstoff aus der Luft wiegt mehr als Stickstoff aus chemischen Verbindungen. Ein kleiner Unterschied, doch er birgt ein großes Rätsel! Zusammen dem Chemiker William Ramsay wittert er eine bahnbrechende Entdeckung.
Ihre Suche ist alles andere als einfach. Das unbekannte Element ist chemisch inert, es geht mit nichts eine Verbindung ein. Herkömmliche Methoden versagen, also müssen sie kreativ werden. Mit der Spektroskopie, einer Technik, die Lichtmuster analysiert, gelingt es ihnen, das Gas zu identifizieren. Gemeinsam entdecken Rayleigh und Ramsay dann tatsächlich Argon! Doch die Fachwelt bleibt misstrauisch. Sogar der berühmte Dmitri Mendelejew zweifelt, weil dieses träge Gas nicht in sein Periodensystem zu passen scheint.
Die Konkurrenz zwischen den beiden Wissenschaftlern treibt sie an. Während Rayleigh sich nun auf die Untersuchung der Eigenschaften von Argon konzentriert, perfektioniert Ramsay seine und isoliert weitere Gase durch Luftverflüssigung: Neon, Krypton und Xenon.
Immer wieder angespornt durch ihre Rivalität schaffen beide Forscher es am Ende, eine völlig neue Gruppe im Periodensystem zu etablieren – die Edelgase!
Der 30.5.1898 – Das Edelgas Krypton wird entdeckt2
Edelgase = "inerte" Gase?
Verwendung von Argon und Helium.3
Helium ist sehr leicht und brennt nicht. Früher setzte man den noch leichteren Wasserstoff für Luftschiffe ein – wie bei der Hindenburg, die 1937 in Lakehurst (USA) explodierte, weil Wasserstoff leicht entzündlich ist. Heute verwendet man hier stattdessen Helium. Dies gilt auch für Ballons, Zeppeline oder als Kühlgas in technischen Geräten.
Argon ist schwerer als Luft und reagiert mit fast nichts. Es wird in Schutzgas-Schweißgeräten eingesetzt, damit das heiße Metall beim Schweißen nicht mit Sauerstoff reagiert und keine Funken oder Oxidschichten entstehen.
Argon, ein Schutzgas
Elektroschweißen mit und ohne Schutzgas Argon.4
Die Edelgase im PSE - eine Sonderstellung!
Ein genauerer Blick in das PSE
Das Schalenmodell und die Edelgaskonfiguration
Hier noch einmal ein Blick auf die Elektronenverteilung im Schalenmodell. Die besondere Verteilung – vor allem mit Blick auf die Valenzschale – bei Helium, Neon, Argon und auch den folgenden Edelgase Krypton und Radon, nennt man Edelgaskonfiguration.
Ausschnitt im Schalenmodell6
Steckbrief der Edelgase
Steckbrief – Vorlage zum herunterladen7