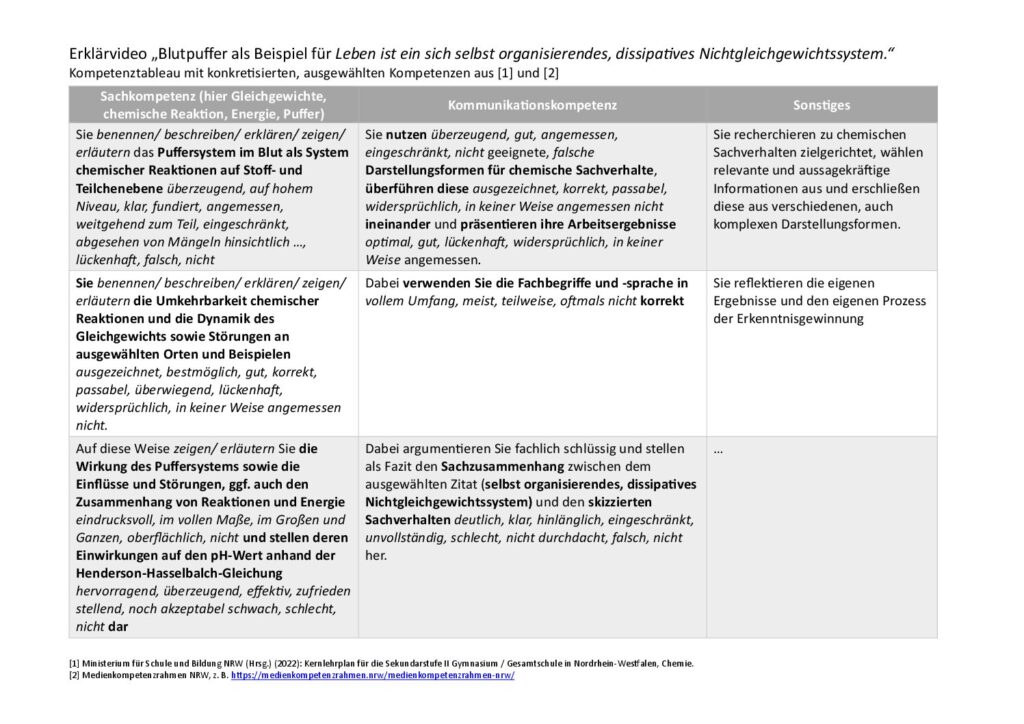
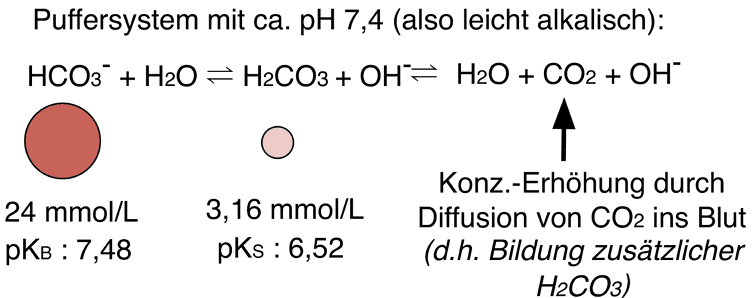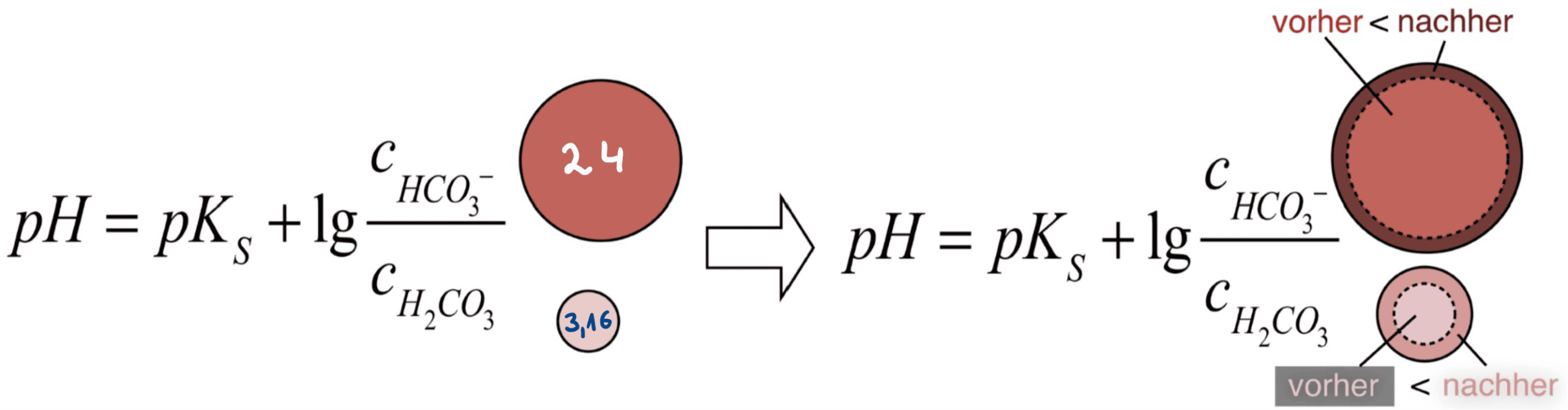Die Funktionsfähigkeit unseres Körpers hängt u.a. davon ab, dass der pH-Wert der Körperflüssigkeiten – und dazu gehört auch das Blut – in einem bestimmten Bereich gehalten wird.
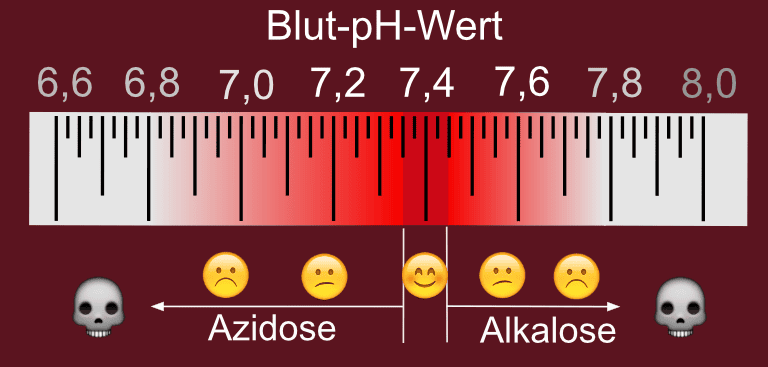
Der ideale Blut-pH-Wert liegt in einem Bereich von 7,35 bis 7,45. Da im Blut verschiedenste Stoffe (z. B. Kohlenstoffdioxid, Aminosäuren, siehe Abb. 1) transportiert werden, die sich auch auf den pH-Wert auswirken können, sind verschiedene Pufferkomponenten im Blut vorhanden.
Kritische Blut-pH-Werte sind verantwortlich für zwei medizinische Krankheitsbilder: Die Azidose und Alkalose. Beide Krankheitsbilder sind noch nicht lebensbedrohlich, aber sie belasten den Körper, weil dadurch vielfältige Stoffwechselprozesse nicht mehr optimal funktionieren (siehe Abb. 2).
Der Blut-Puffer
Weiteres
pH-Wert-Bereiche im Blut. 1
Schematische Darstellung ausgewählter Blutbestandteile. 1
Ein wichtiges Puffersystem des Blutes neben anderen ist das Kohlensäure/Hydrogencarbonat-System (H2CO3/HCO3–). Es macht etwa 75 % der Pufferkapazität aus. Folgende Gleichgewichte werden an den verschiedensten Stellen immer wieder gestört, z. B. beim Durchfluss des Blutes durch die Lunge, durch das Muskelgewebe, durch die Bauchspeicheldrüse (Pankreas) oder die Niere:
Weiteres
Das zweite Gleichgewicht stellt sich in wässrigen Lösungen nach Störungen ohne Katalysator zudem immer wieder nur sehr langsam ein. Im menschlichen Körper sorgt allerdings das Enzym Carboanhydrase dafür, dass die Gleichgewichtseinstellung enorm beschleunigt wird. An jedem Enzymmolekül kann die Reaktion bis zu 100000 Mal pro Sekunde stattfinden. Damit ist die Carboanhydrase eines der aktivsten bekannten Enzyme.
Betrachtet man die Gleichgewichte, so erkennt man, dass diese miteinander verknüpft sind:
Aufgaben
- Beschreiben Sie die Pufferwirkung des Kohlensäure/Hydrogencarbonat-Systems gegen Oxonium-Ionen oder Hydroxid-Ionen unter Angabe geeigneter Reaktionsgleichungen.
- Im Blut des Menschen liegt bei einem pH-Wert von 7,4 eine Hydrogencarbonat-Konzentration von 24 mmol/L vor. Berechnen Sie die Konzentration der Kohlensäure im Blut. Hinweis: pKS (HCO3–) = 10,4 | pKS(H2CO3) = 6,52
- Beurteilen Sie anhand des in A2 ermittelten Verhältnisses der Konzentrationen von Kohlensäure zu Hydrogencarbonat die Eignung dieses Puffersystems sowohl zum Abfangen von Säuren als auch von Basen.
- Speichern Sie Abb. 4 auf ihr Endgerät, ergänzen Sie diese sinnvoll mit Erläuterungen für die übrigen Organe analog zum Muskel in M3. Stellen Sie dabei unter Verwendung von M2 stets die Auswirkungen der Stoffwechselvorgänge auf das Kohlensäure/Hydrogencarbonat-Puffergleichgewicht und damit auf den Blut-pH-Wert argumentativ dar.
- Erstelle ein Erklärvideo unter Berücksichtigung der Punkte in M4.
Anregungen & Lösungen
Überlegen Sie sich, welcher Bestandteil des Puffers mit Hydroxid-Ionen und welcher Bestandteil mit Oxonium-Ionen reagiert.
Nutzen Sie für ihre Berechnung die Henderson-Hasselbalch-Gleichung. Überlegen Sie, welche Werte gegeben sind und welcher Wert gesucht wird. Formen Sie dann die Henderson-Hasselbalch-Gleichung zum gesuchten Wert um.
- Muskel: Das Puffersystem im Blut sorgt für einen leicht alkalischen pH-Wert von 7,4, weil Hydrogencarbonat mit einer Konzentration von 24 mmol/L im Vergleich zur Kohlensäure-Konzentration (c = 3,16 mmol/L) deutlich im Überschuss vorliegt. Das im Muskelgewebe erzeugte Kohlenstoffdioxid diffundiert ins Blut und erhöht dort die Konzentration der Kohlensäure. Nach dem Prinzip von Le Chatelier reagiert ein Teil davon zu zusätzlichem Hydrogencarbonat. Folglich wird die Gesamtkonzentration der Pufferkomponenten erhöht, die Pufferkapazität also gesteigert. (Das Puffersystem wird aufgeladen)
- Lunge: In den Lungenbläschen diffundiert CO2 aus dem Blut in die Atemluft und wird abgeatmet. Das Gleichgewicht reagiert so, dass nun vermehrt Kohlensäure zu Kohlenstoffdioxid reagiert. Diese wird also verbraucht/über die Lunge „entsorgt“. Die entsorgte Kohlensäure wird schließlich teilweise durch den Verbrauch von Hydrogencarbonat-Ionen ersetzt. Durch die Vorgänge in der Lunge wird also die Gesamtkonzentration der Pufferkomponenten gesenkt, die Pufferkapazität also erniedrigt.
- Niere: Bei einem zu niedrigen Blut-pH-Wert scheidet die Niere Oxonium-Ionen über den Urin aus und resorbiert gleichzeitig Hydrogencarbonat-Ionen zurück ins Blut. Diese reagieren im Blut teilweise zu zusätzlicher Kohlensäure, wodurch sich die Gesamtkonzentration der Pufferkomponenten im Blut erhöht. Die Pufferkapazität wird also gesteigert.
- Pankreas: Der Pankreas gibt zur Neutralisation der Magensäure große Mengen Hydrogencarbonat-Ionen in den Darm ab, weil die dort wirkenden Enzyme ihr Wirkoptimum im basischen pH-Bereich haben. Die dabei entstehenden Oxonium-Ionen werden ins Blut abgegeben. Dort reagieren die Oxonium-Ionen direkt mit der Pufferbase (Hydrogencarbonat). Der Blutpuffer muss hier also „aktiv“ arbeiten. Dies ist der einzige der hier beschriebenen Prozesse, der den Puffer direkt und akut verbraucht. Das Konzentrationsverhältnis von Pufferbase zu Puffersäure verändert sich, wodurch sich auch der pH-Wert des Blutes merklich ändert. Die Aktivität der Niere steuert hier jedoch gegen, die Hydrogencarbonat ins Blut abgibt.
Einflüsse auf den Blut-pH-Wert
Weiteres
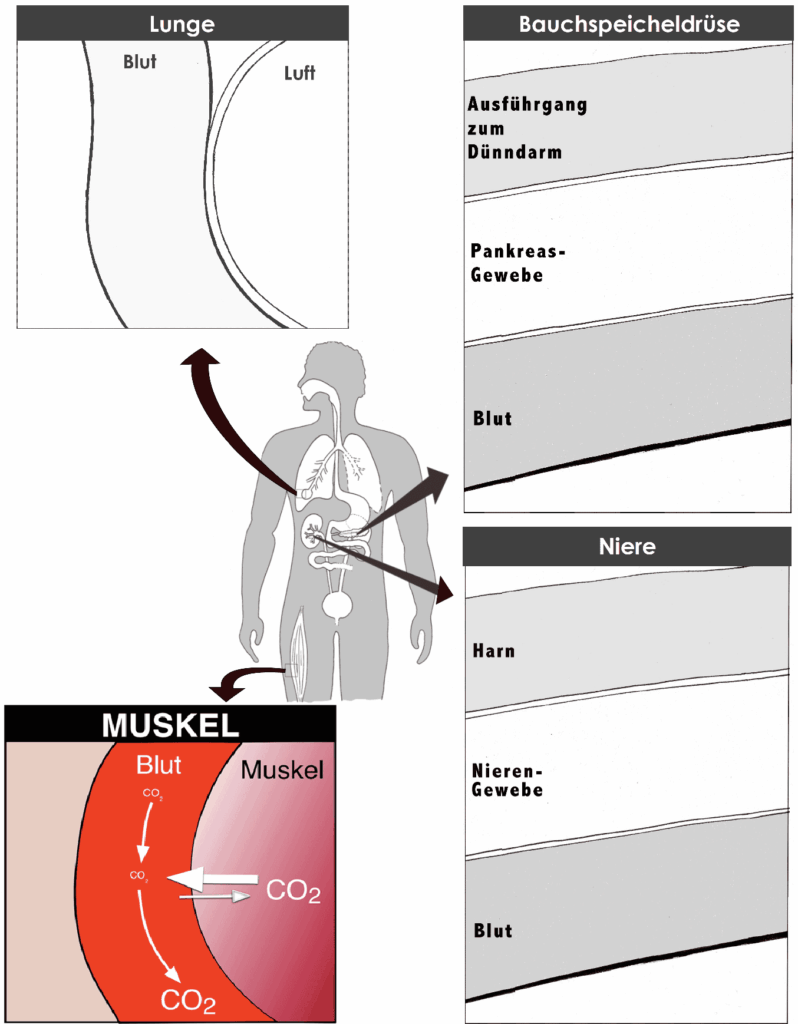
Abläufe an ausgewählten Stellen im Körper verdeutlichen die Störungen und die Notwendigkeit des Kohlensäure/Hydrogencarbonat-Puffers. Zugleich verringern oder erhöhen sie teilweise dessen Kapazität.
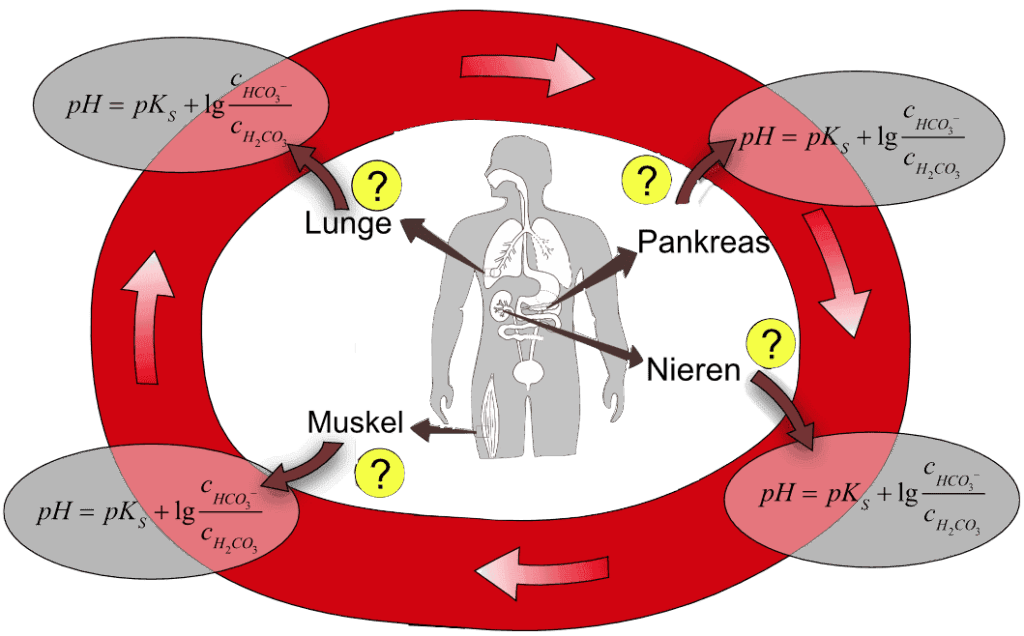
Beispiele für Einflüsse auf den Blut-pH-Wert. 1
Detaillierte Erläuterung am Beispiel der Muskeln
Weiteres
Vorlage zur Detaildarstellung für die Einflüsse auf den Blut-pH-Wert. 1
Weiteres
Das Puffersystem im Blut sorgt für einen leicht alkalischen pH-Wert von 7,4, weil Hydrogencarbonat mit einer Konzentration von 24 mmol/L im Vergleich zur Kohlensäure-Konzentration (c = 3,16 mmol/L) deutlich im Überschuss vorliegt:
Blick auf die Gleichgewichtslage im Muskel. 1
Das im Muskelgewebe erzeugte Kohlenstoffdioxid diffundiert ins Blut und erhöht dort die Konzentration der Kohlensäure. Ein Teil davon reagiert zu zusätzlichem Hydrogencarbonat. Folglich verändert sich das Konzentrationsverhältnis von Hydrogencarbonat zu Kohlensäure nur geringfügig. Der pH-Wert sinkt nach der Gleichung von Henderson und Hasselbalch ebenfalls kaum:
Henderson-Hasselbalch-Gleichung zur Veränderung des pH-Wertes. 2
Die Argumentation lässt sich übertragen und fortführen: In der Lunge, … in der Bauchspeicheldrüse, … in der Niere …
EIn Erklärvideo erstellen
Weiteres
Professor Harald Lesch hat einmal gesagt: „Leben ist ein sich selbst organisierendes, dissipatives Nichtgleichgewichtssystem“
- Übersetzen Sie diesen Satz zunächst einmal in eine sowohl für Sie selbst als auch für Lernende der Jahrgangsstufe unter Ihnen (NRW: Einführungsphase, Stufe 11, Kenntnis von Gleichgewichten sind vorhanden) verständliche Sprache, in dem Sie die verwendeten Begriffe ggf. recherchieren und dann umschreiben.
- Machen Sie sich bewusst, inwiefern das vereinfachte Modell des Blut-Puffer-Systems ein passendes Beispiel für diese Aussage ist.
- Erstellen Sie basierend auf Ihren Überlegungen in einer Kleingruppe ein Erklärvideo zu diesem Satz mit dem Beispiel „Blut-Puffer-System“. Nutzen Sie dabei gerne den „Legetrick-Stil“ bzw. die „Legetrick-Technik“.
Modellversuch zum Blutpuffer mit Mineralwasser
Materialien
- Schutzbrille
- 4 Spritzen a 50 mL
- 2 Dreiwegehähne
Chemikalien
- Mineralwasser
- Leitungswasser
- Kohlenstoffdioxid
- Universalindikator
- Natronlauge
Weiteres
Ein dem Kohlensäure/Hydrogencarbonat-Puffer des Blutes ähnliches System lässt sich aus Gerolsteiner Mineralwasser herstellen. Die Hydrogencarbonat-Ionen-Konzentration beträgt laut Etikett 1816 mg/L, was 29,77 mmol/L entspricht. Der pH-Wert beträgt etwa 6, d.h. die Konzentration der Kohlensäure ist deutlich größer als im Blut (ca. 100 mmol/L). Durch Zugabe von etwas Natronlauge kann der pH-Wert auf 7 angehoben werden. Abgesehen von den etwas höheren Konzentrationen der Pufferkomponenten liegt dann ein passables Puffermodell vor.
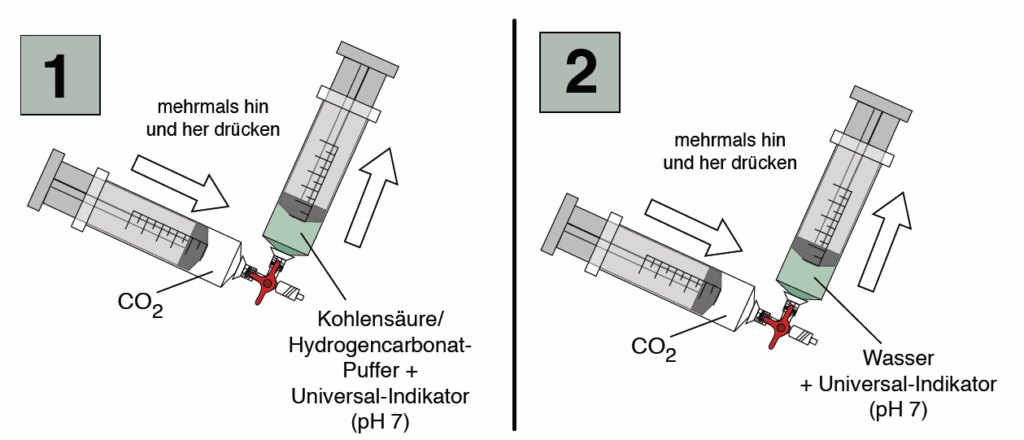
Aufbau
Aufbau des Versuchs 3
Durchführung
- Ca. 20 mL Mineralwasser werden in ein Becherglas gegeben und wenige Tropfen Universalindikator hinzugefügt, bis eine gut sichtbare Färbung eintritt. Sollten Sie schon über Indikatoren gesprochen haben, können Sie auch einen passenden Zweifarbenindikator auswählen.
- Nun gibt man tropfenweise Natronlauge hinzu, bis ein pH-Wert von ca. 7 erreicht ist.
- Die Modell-Puffer-Lösung wird in eine 50 mL Spritze aufgezogen (s. Abb. 7) und aus einer weiteren Spritze wird über einen Dreiwegehahn Kohlenstoffdioxid hinzugefügt. Der Inhalt kann zur besseren Durchmischung mehrfach hin- und hergeschoben werden.
- Zum Vergleich wird in einem weiteren Ansatz der Versuch analog mit Leitungswasser durchgeführt, dem lediglich Universalindikator hinzugefügt wurde.
Weitergedacht
- Enorm gefährlich ist die Bildung von Gasblasen im Blut, die zur Verstopfung von Blutgefäßen führen kann und medizinisch als Embolie bezeichnet wird. Diskutieren Sie in diesem Zusammenhang die Bedeutung der Carboanhydrase und die Bedeutung des leicht alkalischen pH-Wertes des Blutes.
- Erklären Sie, weshalb eine erhöhte Atem- und Herzschlagfrequenz bei einer verstärkten Muskelaktivität dazu beiträgt, den Blut-pH-Wert konstant zu halten.
- Bei einer sogenannten Hyperventilation atmen betroffene Personen durch hechelnde Atmung mehr Kohlenstoffdioxid aus als bei normaler Atmung. Benennen Sie die Auswirkung der Hyperventilation auf den Blut-pH-Wert und erklären Sie, wieso als Gegenmaßnahme ein Ein- und Ausatmen in eine Plastiktüte vorgeschlagen wird, bis sich die Atmung wieder normalisiert hat.
- Der Verzehr saurer Nahrung führt an verschiedenen Stellen zu einer Veränderungen des pH-Werts im Körper. Laut Quarks.de ist dies aber kein Grund zur Panik. 4.
- Erklären Sie basierend auf M2 und M3, weshalb bei der Aufnahme saurer Nahrung der pH-Wert des Urins sinkt, obwohl die aufgenommenen Säuren nicht direkt in den Urin gelangen.
- Dialysepatienten wird empfohlen, stark saure Nahrung möglichst zu meiden – begründen Sie diese Empfehlung!
- Anhaltende Durchfallerkrankungen, bei denen der Dünndarminhalt ständig ausgeschieden wird (nicht aber der Mageninhalt), führen zu einer Azidose des Blutes. Erklären Sie dieses Phänomen!
Lösungen
Das Enzym Carboanhydrase katalysiert die Reaktion von Kohlenstoffdioxid zu Kohlensäure und zurück. Dadurch stellt es sicher, dass Kohlenstoffdioxid nicht als Gas im Blut vorliegt, sondern sofort in die lösliche Form (Kohlensäure bzw. Hydrogencarbonat) überführt wird. Ohne dieses Enzym würde sich Kohlenstoffdioxid im Blut anreichern und Gasblasen bilden können, die Gefäße verstopfen (= Embolie). Die Carboanhydrase verhindert dies also, indem sie Kohlenstoffdioxid in Lösung hält.
Bei starker Muskelaktivität produzieren die Muskeln vermehrt Kohlenstoffdioxid, das im Blut zu Kohlensäure reagiert. Durch die erhöhte Atemfrequenz wird mehr Kohlenstoffdioxid abgeatmet, wodurch sich die Konzentration der Puffersäure (Kohlensäure) verringert. Ein Teil des Verlustes an Kohlensäure wird durch den Verbrauch von Hydrogencarbonat wieder ausgeglichen. Durch die erhöhte Herzschlagfrequenz zirkuliert das Blut schneller. Dadurch wird das in den Muskeln produzierte Kohlenstoffdioxid rascher zur Lunge transportiert, wo es abgeatmet werden kann. Gleichzeitig werden die Pufferstoffe schneller im Körper verteilt. Beide Mechanismen wirken hier zusammen, um die Säurelast durch den Eintrag von Kohlenstoffdioxid zu senken und das Puffersystem zu entlasten. So kann der Blut-pH-Wert trotz erhöhter Säureproduktion konstant gehalten werden.
Durch die Hyperventilation wird übermäßig viel Kohlenstoffdioxid abgeatmet. Da Kohlenstoffdioxid im Blut als Puffersäure (Kohlensäure) vorliegt, führt dies zu einer Verschiebung des Puffergleichgewichts: Kohlensäure wird verstärkt verbraucht. Der pH-Wert des Blutes steigt an. Es kommt zu einer so genannten respiratorischen Alkalose.
Gegenmaßnahme: Beim Ein- und Ausatmen in eine Plastiktüte atmet die Person ihre eigene ausgeatmete Luft mit erhöhter Kohlenstoffdioxid-Konzentration wieder ein. Der Partialdruck des Gases ist so verhältnismäßig hoch in der Lunge, wodurch weniger Kohlenstoffdioxid aus dem Blut in die Alveolarluft in der Lunge diffundiert. Die Kohlenstoffdioxid-Konzentration und damit die Konzentration der Puffersäure normalisieren sich im Blut wieder. Der pH-Wert sinkt in der Folge zurück in den normalen Bereich.
- Die mit der Nahrung aufgenommenen Säuren geben ihre Oxonium-Ionen ins Blut ab und werden dort durch die Pufferbase (Hydrogencarbonat) abgefangen/neutralisiert. Die verbrauchten Hydrogencarbonat-Ionen werden durch die Nierenaktivität wiederhergestellt, indem aktiv Oxonium-Ionen in den Urin und Hydrogencarbonat-Ionen ins Blut abgegeben werden.
- Bei Dialysepatienten sind die Nieren in ihrer Funktionsfähigkeit eingeschränkt. Die Ausscheidungs- und Regenerationsmechanismen der Niere zur Regulation des Säure-Base-Haushalts funktionieren hier ebenfalls nur eingeschränkt. Die Dialyse übernimmt jedoch nur die Entgiftungsfunktion der Nieren, kann jedoch nicht gezielt die Regulation des Säure-Base-Haushalts übernehmen. Durch den Verzehr starker Säuren würde sich die Säurelast im Blut erhöhen, eine Azidose droht. Folglich sollte man den Verzehr stark saurer Nahrung als Dialysepatient vermeiden.
Der Dünndarminhalt wird durch die Aktivität der Bauchspeicheldrüse (Pankreas) alkalisch gemacht, indem Hydrogencarbonat in den Darm und Oxonium-Ionen ins Blut transportiert werden. Dies geht mit einem Nettoverlust der Pufferbase einher. Der pH-Wert des Blutes sinkt, wodurch eine Azidose droht, wenn durch anhaltenden Durchfall dem Puffersystem keine Zeit gegeben wird, sich zu regenerieren.