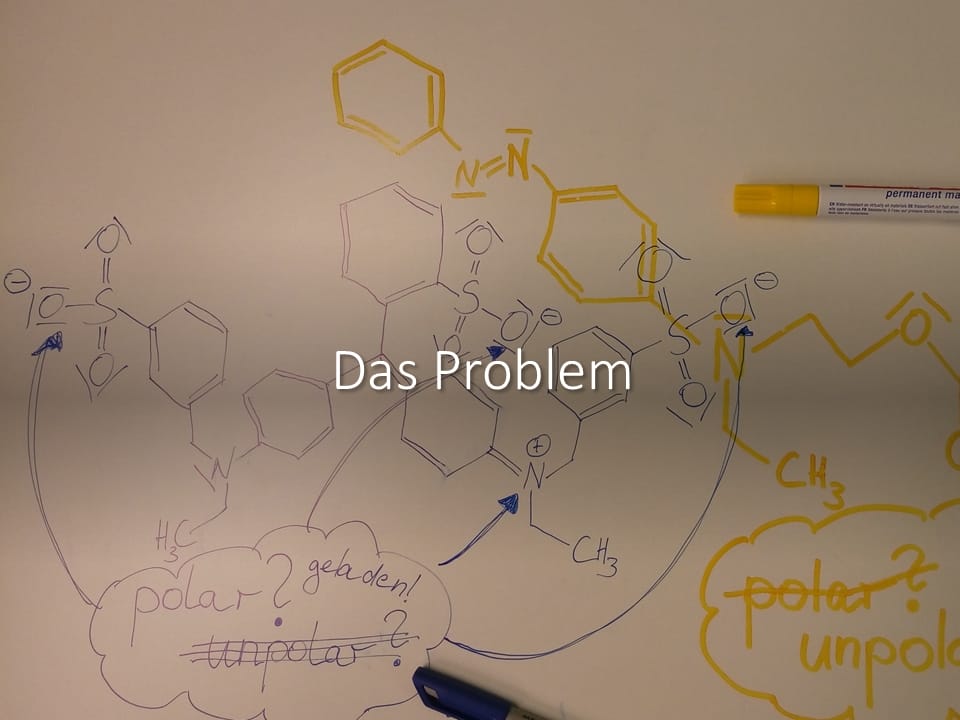
Eine Sprühflasche mit Universallösemittel?
Weiteres
Ein Universalreiniger wäre für „unser Problem“ echt praktisch, oder? Quasi „Sprüh, wisch & weg“! Ich habe da mal was entworfen.
Ein Reiniger für polare und unpolare Farbstoffe?3
Weiteres
Wenn ich es recht überlege, erscheint mir eine Sprühflasche mit Wasser und Heptan aber nicht ideal. Immer erst schütteln? Und dann Heptan! Aber vielleicht fallen euch ein oder mehrere andere Stoffe ein?
Aufgaben
Prüfen und erklären Sie, ob die Farbstoffe (permanent bzw. unpolar, non permanent bzw. polar) in Ethanol löslich sind:
- Führen Sie das Experiment entsprechend der Anleitung V1 durch und nutzen Sie ggf. Video 1.
- Notieren Sie ihre Beobachtungen und beantworten Sie die Versuchsfrage.
- Erstellen Sie für die Erläuterung zu den beiden „Augenblicksaufnahmen“ in M2 das jeweils passende Szenario auf Teilchenebene. Nutzen Sie die haptischen Modelle. Beschriften Sie ihre Abbildungen fachsprachlich korrekt.
Eignet sich Ethanol als das gesuchte Universallösemittel?
Materialien
- Schutzbrille
- Pinzette
- Schnappdeckelglas mit Deckel
- Kunststoffplättchen mit Farben
Chemikalien
- Ethanol
- gelber Farbstoff aus Permanentmarker
- blauer Farbstoff aus nonpermanent Folienstift
Entsorgung
Gefäß verschlossen bei der Lehrperson abgeben.
Ein Kunststoffplättchen wurde mit blauem und gelbem Farbstoff oben/unten bemalt.
Ethanol (ersatzweise Brennspiritus) wurde zuvor von der Lehrperson in ein Schnappdeckelglas eingefüllt.
Prüfen Sie nach jedem Arbeitsschritt, ob der Verschluss dicht sitzt.
Aufbau und Durchführung
- Öffnen Sie das Gefäß und geben Sie mit der Pinzette das Kunststoffplättchen hinein.
- Verschließen Sie das Gefäß sorgsam und beobachten Sie für einige Sekunden, ob etwas passiert.
- Schütteln Sie das Gefäß und beobachten Sie erneut.
Videografie des Versuchs4
Test in der Realität
Weiteres
Eignen sich Ethanol oder Brennspiritus tatsächlich? Wir haben es mal ausprobiert!
Weiteres
Funktioniert das wirklich?5
abschließende Aufgabe
- Vergleichen Sie ein Lösemittelgemisch aus Wasser/Heptan mit dem Lösemittel Ethanol. Benennen Sie dabei Gemeinsamkeiten, stellen sie vor allem aber auch unter Verwendung von Fachbegriffen die Unterschiede – auch auf Teilchenebene – heraus.