M1
Hintergrund & Zielsetzung
Weiteres
- Lerne das Verfahren der pH-metrischen Titration kennen und gebe zu einer Säure mehr Lauge hinzu, als es eigentlich notwendig wäre.
- Erfasse den pH-Wert während der Titration und erstelle daraus ein Diagramm mit charakteristischen Punkten.
Den Versuch 1 kann man mit einem beliebigen pH-Meter durchführen, auch ohne digitale Messwerterfassung! Dann notiert man diese tabellarisch und überführt sie dann in ein Diagramm. Wir verwenden hier eine digitale Messwerterfassung mit der Hilfe einer App auf dem iPad.
Wie können wir besser nachvollziehen, dass bei einer Säure-Base-Titration zu einem plötzlichen Umschlag kommt?
Und wie können wir Lösungen titrieren, die gefärbt oder getrübt sind?
Aufgaben
- Führen Sie V1 durch und notieren Sie ihre Messergebnisse tabellarisch (App oder handschriftlich). Erstellen Sie ein Diagramm aus den Messwerten und kennzeichnen Sie darin markante Punkte.
- Werten Sie ihr Diagramm mit Hilfe der Anregungen aus. Vergleichen Sie ihr Diagramm mit dem Diagramm der anderen Säure-Base-Titration und erklären Sie die Unterschiede.
Anregungen
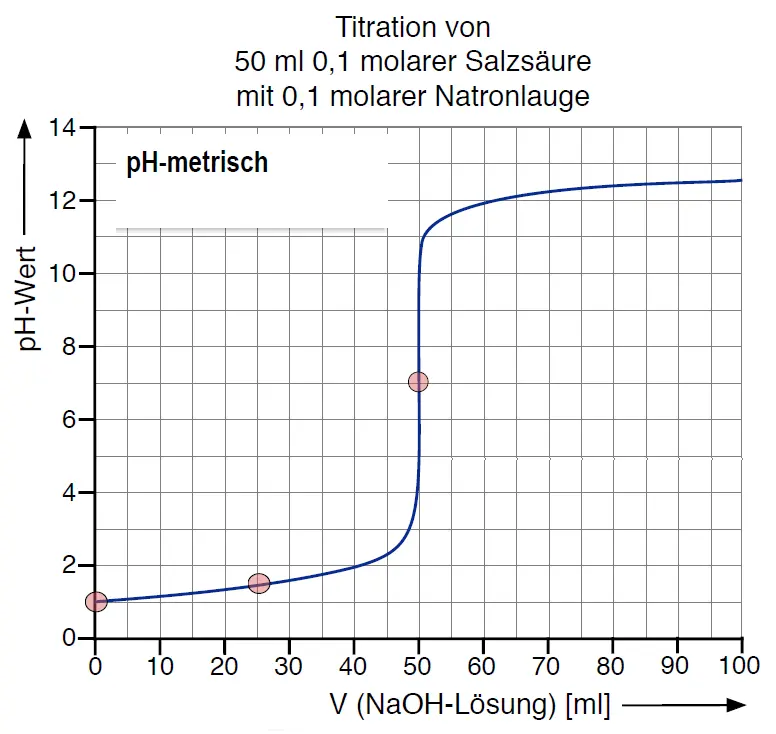
V1
pH-metrische Titration mit Messwerterfassung
Materialien
- Schutzbrille
-
Stativmaterial
- Stativ, Stativklemme, Stativmuffe
- Bürette
- Magnetrührer mit Rührfisch
- Messzylinder
- Erlenmeyerkolben oder Becherglas 150 mL
- Ggf. Trichter zum Befüllen der Bürette
-
Bluetooth pH-Meter
- mit Sparkvue-App auf dem iPad
Chemikalien
- Salzsäure mit fraglicher Konzentration
- Essigsäure mit fraglicher Konzentration
- Natronlauge 0,2 mol/L
- Wasser
Die Lehrperson weist ihrer Gruppe eine Säure unbekannter Konzentration zu, die Sie bitte mit Natronlauge bekannter Konzentration titrieren.
Weiteres
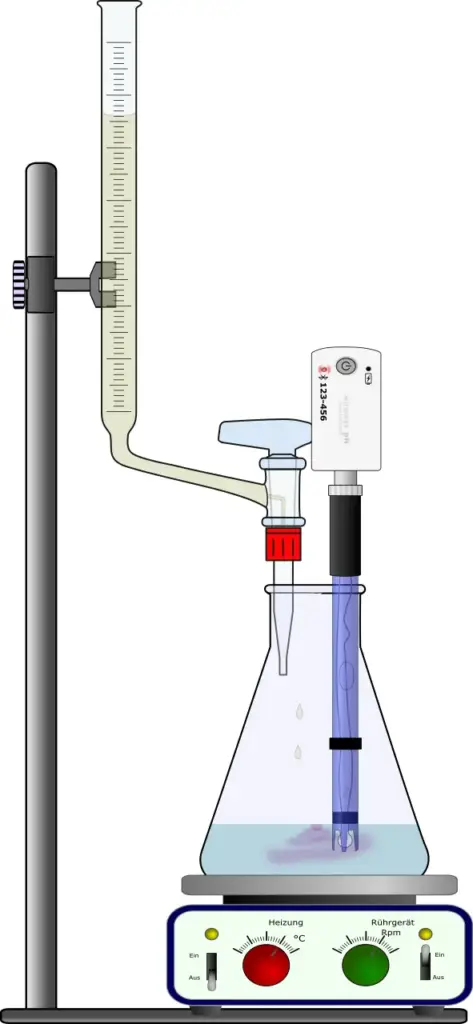
- Apparatur gemäß Abb. 1 aufbauen.
- Bürette ggf. mit Trichter oder einer Spritze von oben mit Natronlauge befüllen. Das Befüllen darf nie über Augenhöhe geschehen, da bei einem Unfall ernsthafte Augenschäden zu befürchten wären. Die Bürette wird zunächst absichtlich mit etwas mehr Natronlauge befüllt. Überschüssiges Volumen wird dann unten abgelassen.
- 50 mL Säure (Salzsäure oder Essigsäure) in den Erlenmeyerkolben geben. Ein Auffüllen und damit ein Verdünnen mit Wasser würde den Anfangs-pH-Wert beeinflussen. Dies wollen wir dieses Mal verhindern.
- pH-Meter in die Lösung eintauchen und so fixieren, dass er tief genug in die Lösung eintaucht und nicht mit dem Rührfisch in Berührung kommt.
- Den Magnetrührer einschalten und den pH-Wert der Salzsäure notieren.
- In 1 mL Schritten portionsweise Natronlauge zur Säure titrieren bis die gesamte Maßlösung verbraucht wurde. Nach jeder Zugabe den pH-Wert notieren.
- Die Lösung über den Abguss entsorgen.
Weiteres
Aufbau mit pH-Meter. 1
Weitergedacht
- Wählen Sie für die pH-metrische Titration von Salz- und Essigsäure mit Natronlauge jeweils einen geeigneten Indikator mit Hilfe von Abb. 3 in M2 begründet aus.
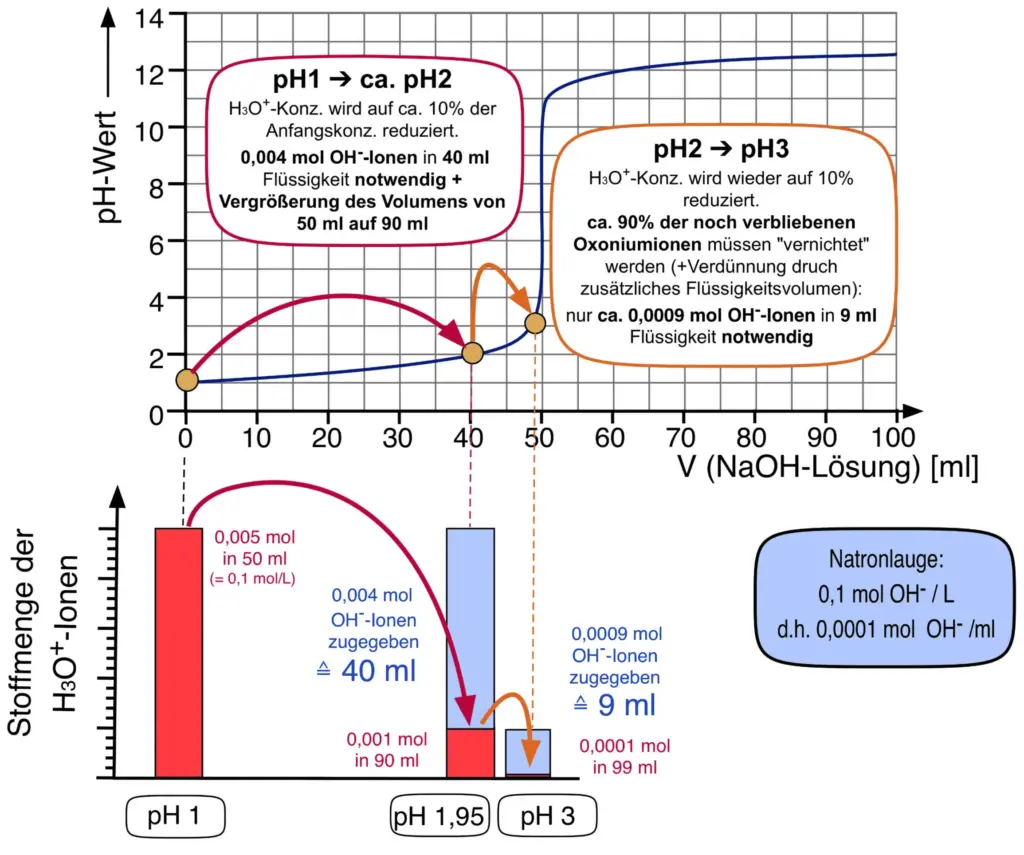
- Erläutern Sie das Zustandekommen des „pH-Sprungs“ mit Hilfe von Abb. 2 in M2.
Lösungen
Anfangsphase
- Zu Beginn liegt eine hohe Oxonium-Ionen-Konzentration vor.
- Die ersten Tropfen Natronlauge neutralisieren nur einen kleinen Anteil der Oxonium-Ionen. Da die Konzentration dieser so hoch ist, hat dies nur einen geringen Effekt auf den pH-Wert.
- Um Beispielsweise den pH-Wert von 1 auf 2 zu steigern muss die Oxonium-Ionen-Konzentration auf 10 % ihrer Anfangskonzentration gesenkt werden. Dies erfordert beachtliche Mengen an Hydroxid-Ionen zur Neutralisation.
- Für den nächsten Schritt (pH 2 zu 3) muss wiederum die verbliebene Konzentration auf 10 % sinken, was jedoch weniger Hydroxid-Ionen erfordert, da die Ausgangskonzentration jetzt deutlich niedriger ist.
Vor dem Äquivalenzpunkt
- Je näher man dem Äquivalenzpunkt kommt, desto geringer wird die verbleibende Oxonium-Ionen-Konzentration.
- Die Folge: Jetzt neutralisiert die gleiche Menge an Hydroxid-Ionen einen größeren prozentualen Anteil der noch vorhandenen Oxonium-Ionen.
- Kurz gesagt: Eine prozentuale Reduktion der Oxonium-Ionen-Konzentration führt zu einer linearen pH-Erhöhung. Je kleiner die Ausgangskonzentration, desto größer der pH-Effekt pro zugegebener Portion an Hydroxid-Ionen.
Am Äquivalenzpunkt
- Am Äquivalenzpunkt sind Säure und Base stöchiometrisch äquivalent.
- Kurz vor dem Äquivalenzpunkt ist die Oxonium-Ionen-Konzentration sehr sehr klein.
- Ein einziger Tropfen an Hydroxid-Ionen reicht nun aus, um die restlichen Oxonium-Ionen zu neutralisieren und eine messbare Hydroxid-Ionen-Konzentration zu erzeugen.
- Ein winziger Überschuss führt also zu einem abrupten Sprung des pH-Wertes um mehrere Einheiten.
Nach dem Äquivalenzpunkt
- Nach dem pH-Sprung liegt ein Überschuss an Hydroxid-Ionen vor.
- Die Zugabe weiterer Hydroxid-Ionen erhöht deren Konzentration nur noch allmählich, der pH steigt daher wieder langsam an.
- Für eine Titration von Salzsäure mit Natronlauge empfiehlt sich ein pH-Indikator, dessen Umschlagsbereich am pH-Wert des Äquivalenzpunktes liegt, also bei pH = 7, zum Beispiel Bromthymolblau.
- Für eine Titration von Essigsäure mit Natronlauge empfiehlt sich ein pH-Indikator, dessen Umschlagsbereich am pH-Wert des Äquivalenzpunktes liegt, also bei pH = 9,24, zum Beispiel Thymolblau.