Ein warmer Tag am Meer
Weiteres
Betrachten wir gemeinsam die Bilder1 in Galerie 1, halten zwischendurch aber mal an ….
Wasser, Sauerstoff und Stickstoff – Stoffe und Teilchen.2
… und überlegen, welche generelle Aussagen wir über die Anziehungskräfte zwischen Stickstoff-, Sauerstoff- und Wassermolekülen – jeweils unter ihresgleichen – machen können.
Weiteres
Die heutige Frage ist: warum ziehen sich Wassermoleküle untereinander besonders stark an?
Die Erklärung dafür finden wir in einer Verschiebung der Ladungen in den Elektronenpaarbindungen und der Gestalt der Wassermoleküle.
Werfen wir einmal nacheinander einen Blick darauf.
Aufgaben
- Erstellte mit Hilfe von M2 eine Argumentationskette, warum sich Wassermoleküle untereinander stark anziehen. Nutze die Begriffe Elektronegativität, Differenz der Elektronegativität, polare Bindung, Dipol, Dipol-Dipol-Wechselwirkung.
- Wenn Du noch Zeit hast, dann erkläre mit Hilfe von M3, warum ein Wassermolekül eine gewinkelte Form haben muss.
Hilfen und Lösungen
Beginne vielleicht so:
- Um Wasser zum Sieden zu bringen, braucht man viel Energie.
- Das liegt daran, dass sich Wassermoleküle stark anziehen.
- Das liegt daran, dass die Moleküle Dipole …
- …
Oder beginne so:
- Schaut mal ein Wassermolekül genauer an, stellt man fest, dass die Bindungselektronen …
- Das liegt an der sogenannten Elektronegativität …
- … wenn , … dann …
Bestimme mit Hilfe des Periodensystems die Werte der Elektronegativitäten für Wasserstoff (H) und Sauerstoff (O).
Wo diese zu finden sind, erklärt die Legende.
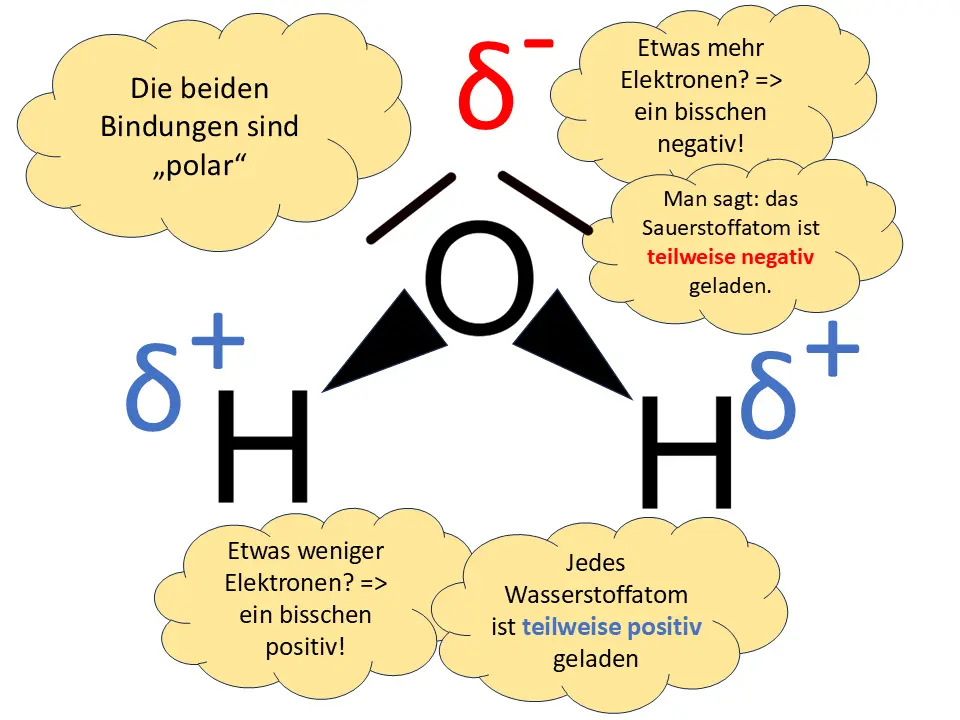
Ist die Differenz der Elektronegativitäten > 0,4? Dann ist die Bindung polar. Die Elektronen sind teilweise zum elektronegativeren Partner verschoben. Diese ist leicht negativ geladen.
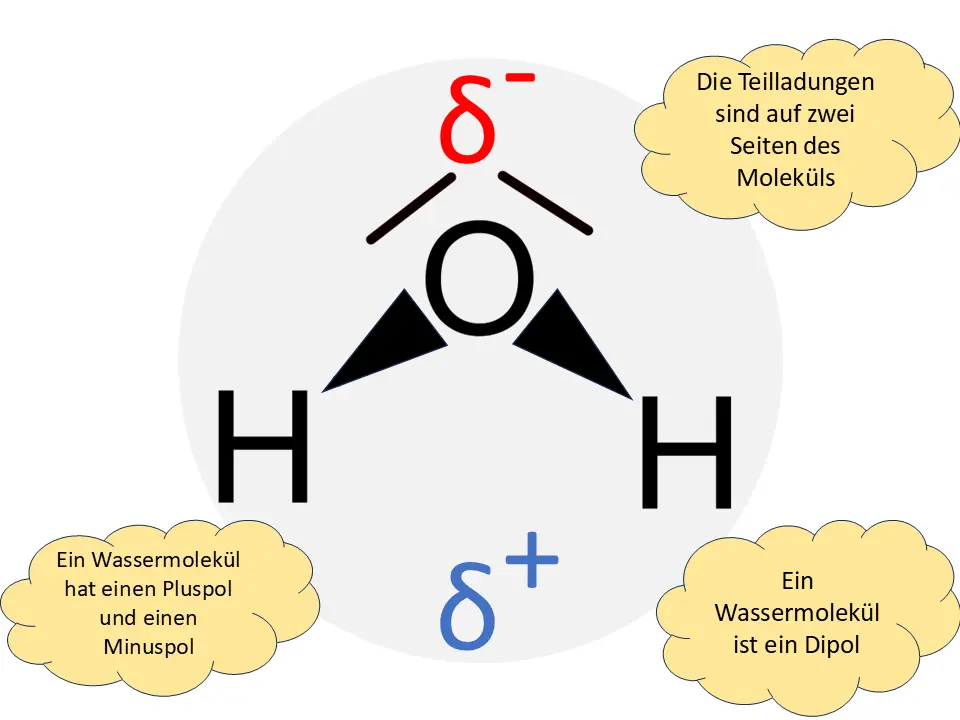
Gibt es polare Bindungen und sind diese so verteilt, dass eine Seite des Moleküls leicht negativ und die andere positiv ist?
Dann ist das Molekül ein Dipol.
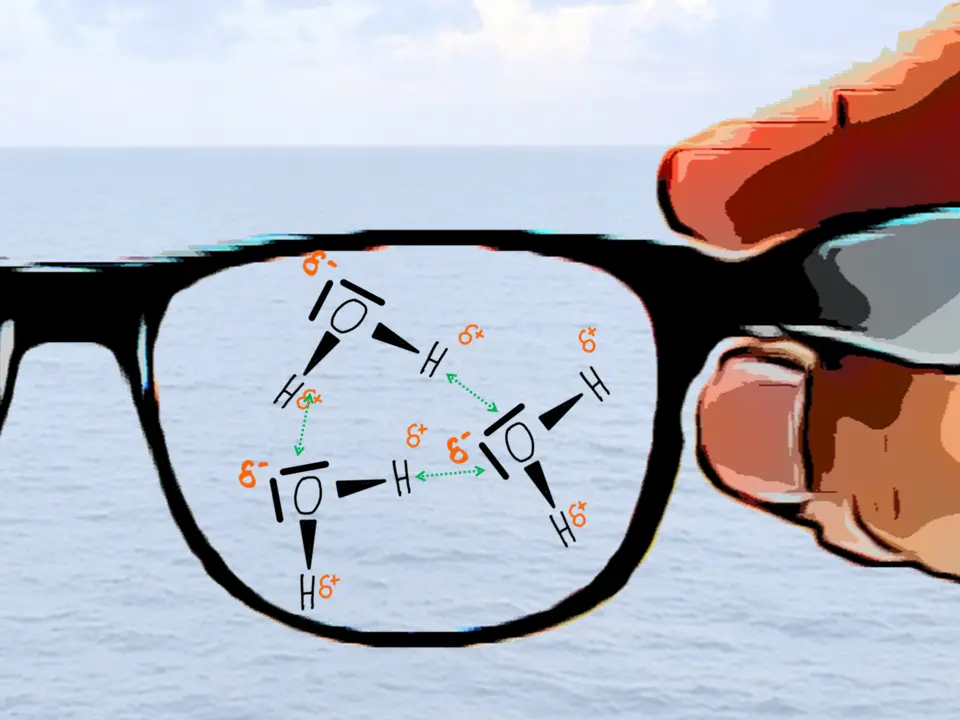
Aufgrund der gewinkelten Form des Wassermoleküls und der deutlich höheren Elektronegativität des Sauerstoffatoms im Vergleich zum Wasserstoffatom kommt es zu einer unsymmetrischen Ladungsverteilung.
Das Sauerstoffatom ist negativ partiell geladen (δ-), die beiden Wasserstoffatome sind positiv partiell geladen (δ+). Dadurch hat das Molekül ein positives und ein negatives Ende. Aus diesem Grund sind Wassermoleküle permanente Dipole.
Wassermoleküle sind Dipole.3
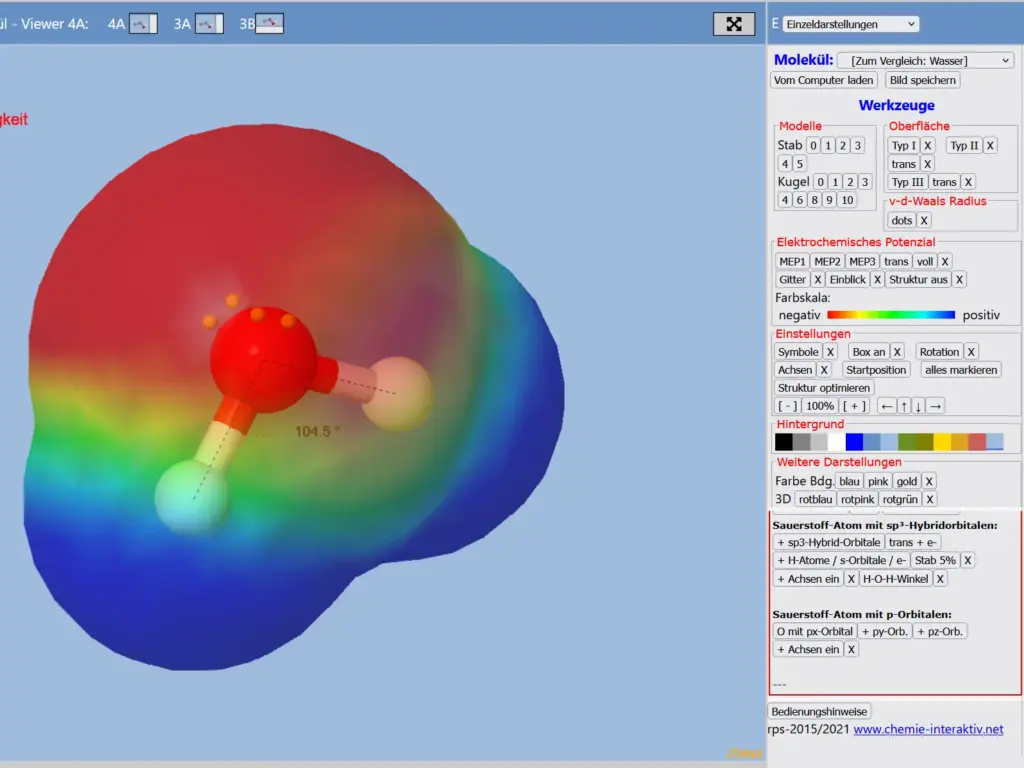
Elektronendichteverteilung und resultierende Teilladungen – link zum Molekülviewer von R.-P. Schmitz4
Geht auf die Seite.
- wähle beim Molekül in der Stoffliste „Wasser“ aus,
- schalte unter Elektrochemisches Potential „MEP1“ und „trans“ an.
- Wähle unter Zusatzfunktionen „Freie Elektronen“ aus.
Wo genau sind die Elektronen im Wassermolekül?
Eine polare Elektronenpaarbindung
In einigen Molekülen sind die Elektronen in Elektronenpaarbindungen nicht immer genau in der Mitte zwischen den beteiligten Atomen.
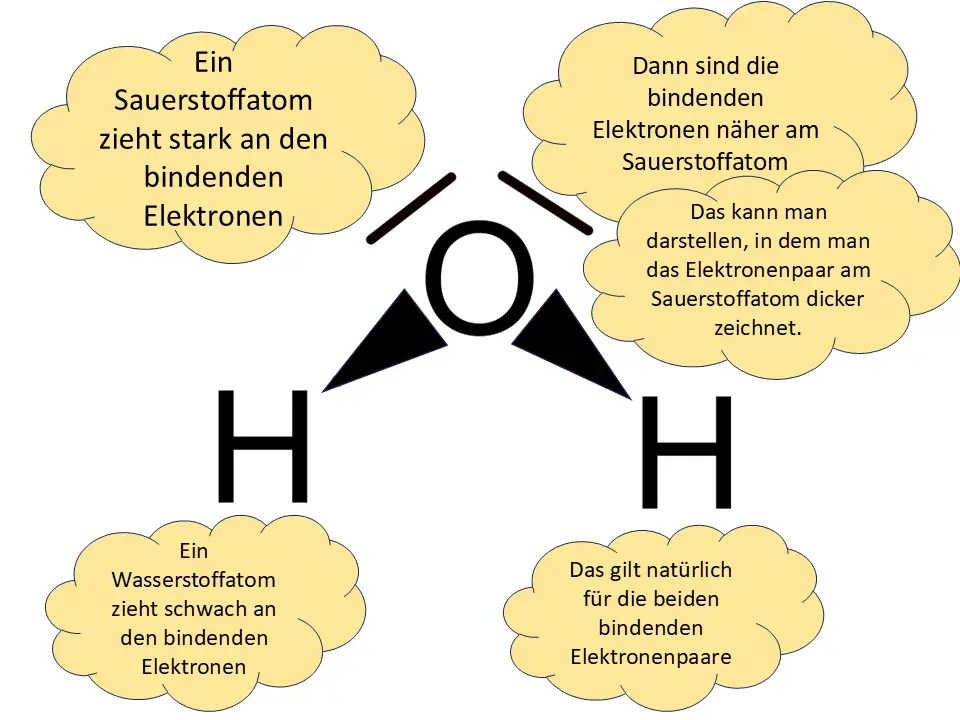
Einige Atome ziehen stärker an den Elektronen.
Das hat zur Folge, dass die Elektronen näher zu diesen Atomen hinrücken.
Schauen wir uns das mal für das Wassermolekül an.
Im Wassermolekül sind die Bindungselektronen nicht gleich verteilt.3
Wann kommt es zu solchen polaren Bindungen?
Ganz einfach: wie stark ein Atom an den Elektronen einer Bindung zieht, ist eine Eigenschaft, die man Elektronegativität nennt.
Sauerstoff hat eine deutlich höhere Elektronegativität als Wasserstoff.
Wenn es dir hilft, kannst du dir die daraus resultierende Verschiebung der Elektronen wie ein Seilziehen vorstellen.
Eine „vermenschlichte“ Analogie: das Sauerstoffatom zieht die Bindungselektronen zu sich.5
Die Elektronegativität
Die Elektronegativität wurde bereits für nahezu jedes Element bestimmt. Es ist eine Größe ohne Einheit. Der maximale Wert beträgt 4.
Schau mal in das erweiterte PSE3. Wo findest du Elemente mit hohen Werten für die Elektronegativität? Wo stehen die Elemente mit niedrigen Werten?
Welche Elemente haben gar keine Werte zugeschrieben bekommen? Warum könnte dies so sein?
Das PSE3 mit Werten für die Elektronegativität.3
Je größer die Elektronegativität eines Elements ist, desto stärker zieht ein Atom dieses Elements an den Elektronen der Elektronenpaarbindung.
Das macht sich natürlich nur immer dann bemerkbar, wenn die beteiligten Atome verschieden große Elektronegativitäten haben.
Vereinfacht kann man sagen: Eine Bindung ist polar, wenn ein Bindungspartner die Elektronen deutlich stärker anzieht. Die Differenz der Elektronegativitäten (ΔEN) sollte dazu ungefähr größer als 0,4 sein.
Molekülgestalt und Dipolmoment
Nun wird es interessant! Wenn ein Molekül mindestens eine polare Bindung beinhaltet und zudem seine Gestalt so ist, dass dadurch eine Seite teilweise positiv und die andere teilweise negativ ist, dann hat das ganze Molekül zwei elektrische Pole.
Solche Moleküle nennt man „Dipole“.
Man sagt fachsprachlich korrekt: „Da solche Moleküle ein permanentes Dipolmoment besitzen, können sich ihre partiell positiv und negativ geladenen Bereiche gegenseitig anziehen.“ Diese Anziehung nennt man „Dipol-Dipol-Wechselwirkungen“.
Die Molekülgestalt ist vorgegeben
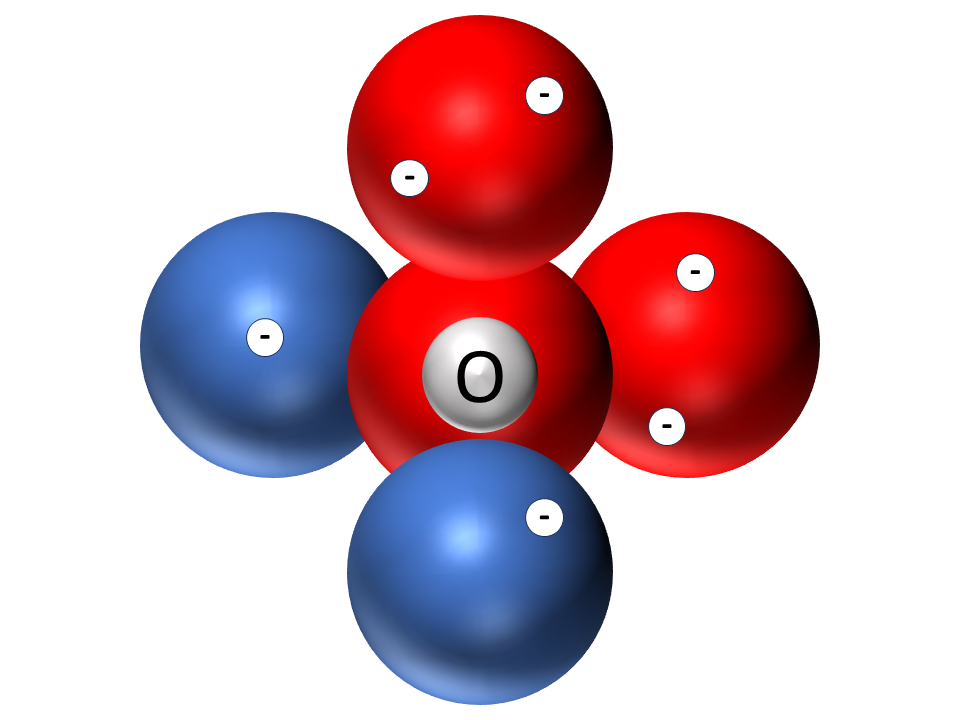
Erinnere dich an das Kugelwolkenmodell
Das Elektronenpaarabstoßungs-Modell
Das Elektronenpaarabstoßungs-Modell (EPA-Modell)7 besagt, dass dies nun auch in den Molekülen gilt, die sich aus den Atomen bilden.
Moleküle haben folglich zwangsläufig eine bestimmte Gestalt. Das Wassermolekül ist z. B. gewinkelt.
Das kannst Du sehr gut in folgender Simulation sehen.
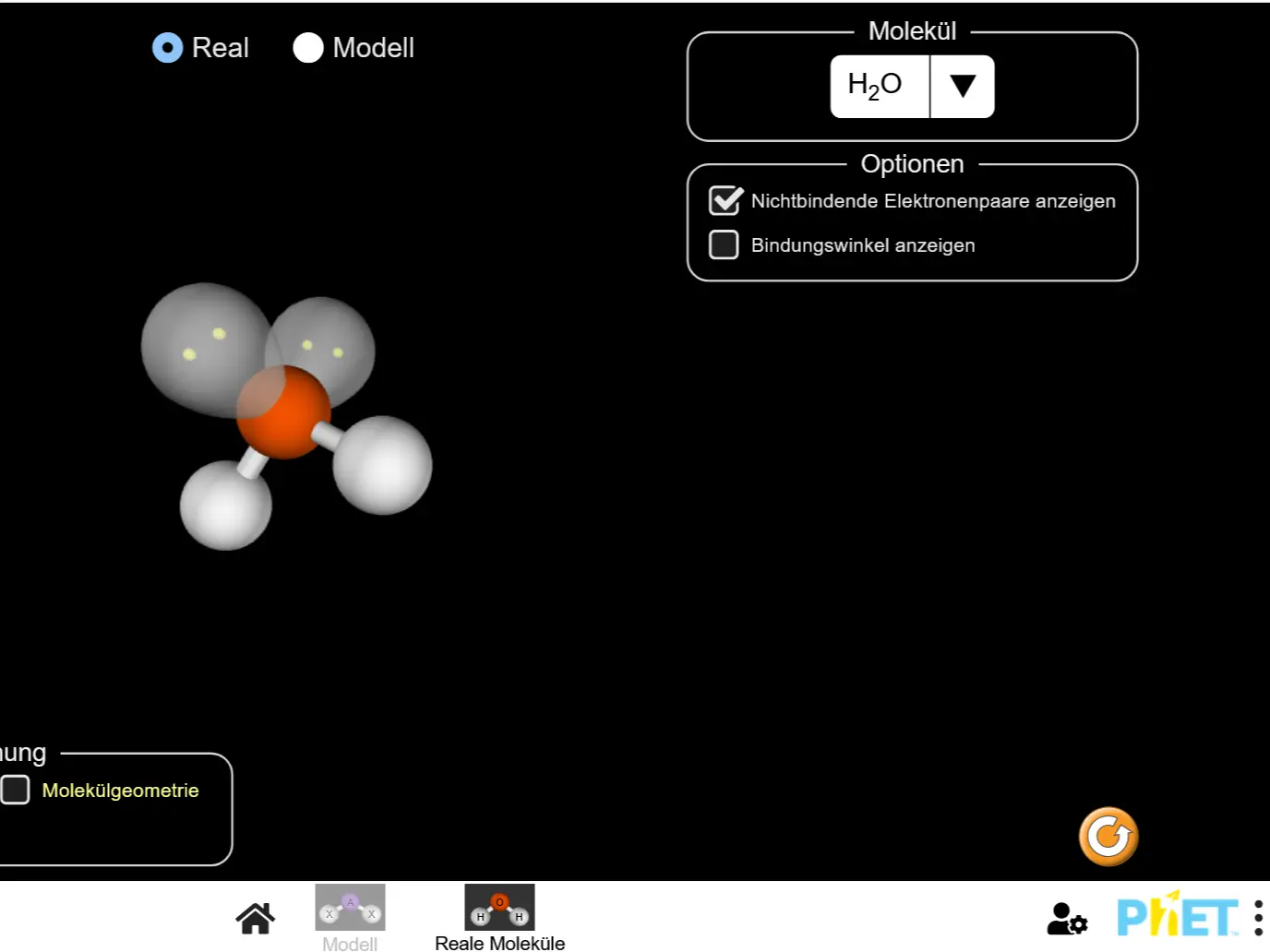
Molekülgeometrie nach dem EPA Modell – link zur Simulation bei PhET.8
Geht auf die Seite, teste verschiedene Einstellungen. Erkläre, was du siehst und welche Bedeutung einzelne Symbole oder die gewählten Darstellungen haben.
abschließende Aufgaben
- Entscheide, ob Stickstoffmoleküle (N2), und Sauerstoffmoleküle (O2) Dipole sind. Begründe deine Entscheidung.
- Gehe zurück zum Anfang: Erläutere nun, warum die Erde bei einer mittleren Temperatur von 16,5°C an vielen Stellen mit flüssigem Wasser bedeckt ist, umgeben von einer dünnen Schicht überwiegend aus gasförmigem Stickstoff und gasförmigem Sauerstoff.
Lust auf mehr?
- Sind folgende Moleküle Dipole? Fluorwasserstoff (HF), Ammoniak (NH3), Methanal (CH2O) oder Kohlenstoffdioxid (CO2)