Aufgaben
- Fassen Sie die Kernaussagen in M1 und M2 stichpunktartig zusammen.
- Berechnen Sie die Konzentrationen der Ionen in einer gesättigten Calciumcarbonat- und Bariumnitrat-Lösung.
- 0,00188 g Silberchlorid (AgCl) lösen sich in einem Liter dest. Wasser bei 25 °C. Wie groß ist das Löslichkeitsprodukt? M(AgCl) = 143,32 g/mol
Rückblick: Die Fällungstitration
Weiteres
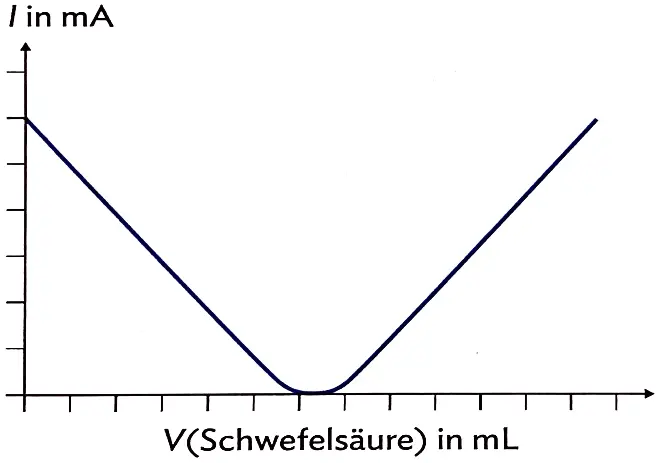
Titrationskurve einer Fällungstitration einer Bariumhydroxid-Lösung mit Schwefelsäure.1
Ein Sonderfall der Leitfähigkeitstitration ist die Fällungstitration. Ein Beispiel hierfür ist die Titration von Bariumhydroxid-Lösung mit Schwefelsäure. Bei der Titration sinkt die Leitfähigkeit bis zum Äquivalenzpunkt fast auf Null ab, da neben der Neutralisation der Hydroxid-Ionen das Salz Bariumsulfat entsteht, welches schwer löslich ist und aus der Lösung ausfällt. Somit sinkt die Ionenkonzentration am Äquivalenzpunkt fast auf null ab:
Weiteres
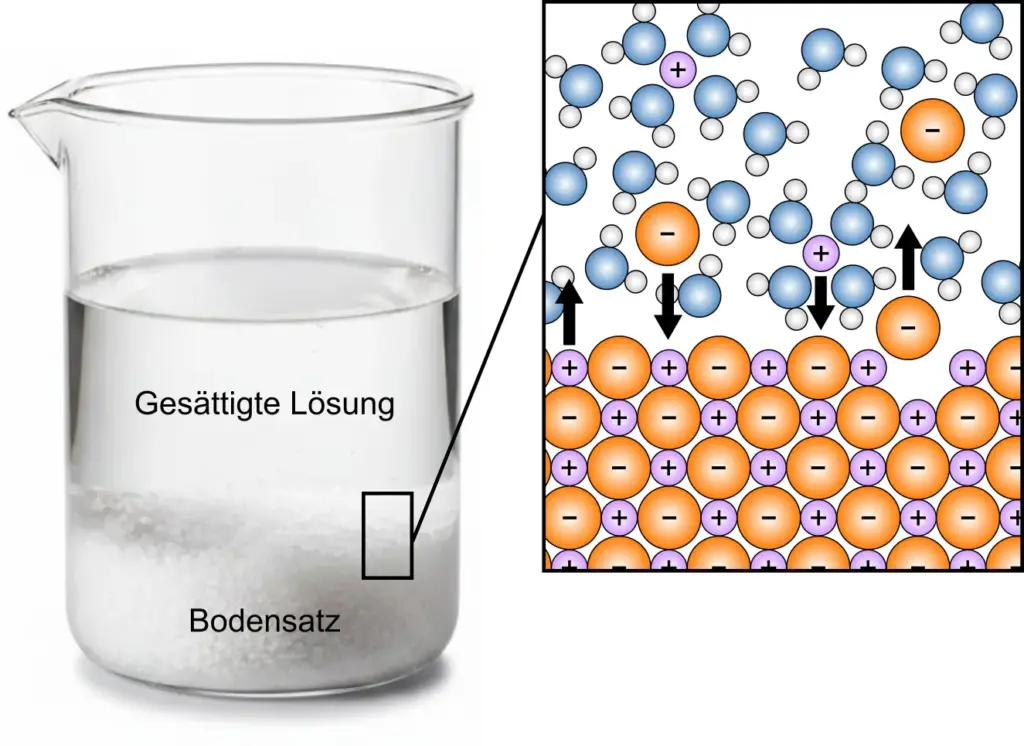
Aber warum fallen einige Salze in Lösungen aus, während andere Salze gut wasserlöslich sind? Grundsätzlich müssen beim Lösen von Salzen Ionen aus dem Ionengitter des Salzes gelöst werden, indem die Ionenbindungen zwischen den Ionen überwunden und die Ionen hydratisiert werden. Bei der Rückreaktion wird das Salz aus der Lösung ausgefällt, indem sich hydratisierte Ionen unter Freisetzung der Wasser-Moleküle wieder zu einem Ionengitter zusammenlagern. In einer gesättigten Salzlösung mit einem Bodensatz aus ungelöstem Salz besteht an der Phasengrenze ein Gleichgewicht zwischen der Lösungs- und Fällungsreaktion, nachfolgend vereinfacht dargestellt:
Vorgänge in einer gesättigten Salzlösung mit Bodensatz an der Phasengrenze zwischen Bodensatz und gesättigter Lösung. Man beachte die Ausrichtung der Wassermoleküle um die gelösten Ionen in der Teilchendarstellung. 2
Das Löslichkeitsprodukt
Weiteres
In einer gesättigten Lösung mit Bodensatz besteht ein dynamisches Gleichgewicht zwischen der Hin- und Rückreaktion, wodurch die Konzentration der Ionen in der Lösung konstant bleibt. Die Ionenkonzentration und damit die Lage des Gleichgewichts lässt sich jedoch nach dem Prinzip von LE CHATELIER beeinflussen, indem beispielsweise die Temperatur verändert wird.
Die Lage des Gleichgewichts lässt sich durch das so genannte Löslichkeitsprodukt KL beschreiben. Es ist ein Maß für die Löslichkeit eines Salzes bei einer gegebenen Temperatur. Es kann mit Hilfe des Massenwirkungsgesetzes (MWG) hergeleitet werden. Für das Auflösen und Fällen von Bariumsulfat gilt demnach:
Für die Konzentrationen der gelösten Sulfat- und Barium-Ionen ist es jedoch irrelevant, wie viel fester Bodensatz, also festes Bariumsulfat, sich im Reaktionsgefäß befindet. Seine Konzentration lässt sich also als konstant ansehen. Sie kann somit in die Gleichgewichtskonstante K einbezogen werden, wodurch sich eine neue Konstante KL ergibt, das so genannte Löslichkeitsprodukt:
Beispielrechnung
In einem Experiment wurde die Konzentration gelöster Barium-Ionen in einer gesättigten Bariumsulfat-Lösung bei 20 °C ermittelt. Gemäß der Löslichkeitsgleichgewichtsreaktion entstehen beim Auflösen des Salzes ein Sulfat- und ein Barium-Ion. Folglich sind die Konzentrationen der Ionen identisch. Sie lassen sich in die Formel einsetzen:
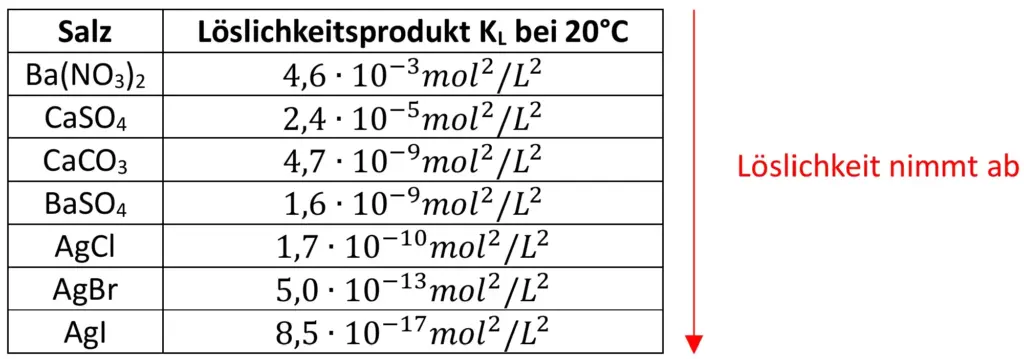
Somit ist KL ein Maß für die Löslichkeit eines Salzes bei gegebener Temperatur. Je größer KL ist, desto mehr Ionen befinden sich in der gesättigten Lösung, desto besser löst sich das Salz. Die Löslichkeitsprodukte von Salzen unter Standardbedingungen sind in Formelsammlungen angegeben:
Fällungsreaktionen sind nicht nur bei Titrationen von Belang, sondern nehmen auch im Rahmen von Nachweisreaktionen für bestimmte Ionen einen hohen Stellenwert im Labor ein.
Phänomene zum Löslilchkeitsprodukt
- Gibt man in eine Silberchlorid-Lösung konzentrierte Natriumchlorid-Lösung, ist eine weiße Trübung der Flüssigkeit zu beobachten. Die Konzentration der Silber-Ionen sinkt etwas. Erklären Sie dieses Phänomen.
- Cyanid-Ionen bilden mit Silber-Ionen die recht stabilen [Ag(CN)2]–-Komplex-Ionen. Nach der Zugabe von gut löslichem KCN wird der Bodenkörper in übersättigter Silberchlorid-Lösung deutlich kleiner. Erklären Sie dieses Phänomen.
- Tropft man wenige Tropfen Silbernitrat-Lösung in destilliertes Wasser, ist keine Veränderung zu beobachten. Tropft man es dagegen in Leitungswasser oder gar in Salzwasser, ist eine schwache bis starke Trübung zu erkennen. Erklären Sie dieses Phänomen.
Lösungen
Silberchlorid (AgCl) ist ein schwerlösliches Salz. In einer gesättigten Lösung besteht ein dynamisches Gleichgewicht zwischen dem festen Bodenkörper und den gelösten Ionen:
Das dazugehörige Löslichkeitsprodukt KL ist bei einer bestimmten Temperatur konstant:
Wenn Sie nun konzentrierte Natriumchlorid-Lösung (NaCl) hinzufügen, führen Sie der Lösung eine große Menge an Chlorid-Ionen (Cl–) zu.
Störung des Gleichgewichts: Die Konzentration der Chlorid-Ionen steigt schlagartig an.
Überschreitung des Löslichkeitsprodukts: Das Produkt aus c(Ag+) und der neuen, hohen c(Cl–) ist nun deutlich größer als die Konstante KL.
Das Prinzip von Le Chatelier: Nach dem Prinzip vom kleinsten Zwang versucht das System, der Störung (der hohen Chlorid-Konzentration) auszuweichen. Reaktion: Um den Wert von KL wieder zu erreichen, muss das System die Konzentration der Ionen senken. Dies geschieht, indem Ag+-Ionen mit den überschüssigen Cl–-Ionen zu festem Silberchlorid reagieren.
Die weiße Trübung: Das neu gebildete, feste Silberchlorid fällt als feiner Niederschlag aus. Diese suspendierten Feststoffpartikel nehmen wir als weiße Trübung wahr.
Sinken der Silber-Ionen-Konzentration: Da die Ag+-Ionen für die Bildung des Niederschlags verbraucht werden, sinkt ihre Konzentration in der Lösung.
In der gesättigten Silberchlorid-Lösung (mit Bodenkörper) besteht folgendes Gleichgewicht:
Es befinden sich also immer einige freie Silber-Ionen in der Lösung. Wenn Cyanid-Ionen (CN–) hinzugefügt werden, reagieren diese mit den freien Silber-Ionen zu einem sehr stabilen Komplex, dem Dicyanidoargentat(I)-Ion:
Da dieser Komplex chemisch sehr stabil ist (hohe Komplexbildungskonstante), liegt das Gleichgewicht extrem weit auf der rechten Seite. Das bedeutet, dass fast alle freien Silber-Ionen „weggefangen“ und im Komplex gebunden werden. Durch die Komplexbildung sinkt die Konzentration der freien Silber-Ionen in der Lösung massiv ab. Das ursprüngliche Löslichkeitsprodukt ist nun unterschritten. Das System ist nicht mehr im Gleichgewicht.
Um den Verlust an freien Silber-Ionen auszugleichen, verschiebt sich das Löslichkeitsgleichgewicht nach rechts (gemäß dem Prinzip vom kleinsten Zwang/ Prinzip von Le Chatelier): Festes Silberchlorid vom Bodenkörper geht in Lösung und zerfällt in Silber- und Chlorid-Ionen. Die neu entstandenen Silber-Ionen werden sofort wieder von den Cyanid-Ionen abgefangen und komplex gebunden. Ergebnis: Dieser Prozess setzt sich so lange fort, wie Cyanid-Ionen vorhanden sind oder bis der gesamte Bodenkörper aufgelöst ist. Da das Silber im Komplex „maskiert“ ist und nicht mehr für das Löslichkeitsgleichgewicht zur Verfügung steht, löst sich der Bodenkörper auf.
Zusammenfassend: Die hohe Stabilität des Silber-Cyanid-Komplexes entzieht der Lösung die Silber-Ionen, wodurch das schwerlösliche Silberchlorid gezwungen wird, sich nachzulösen.
Destilliertes oder demineralisiertes Wasser wurde von fast allen gelösten Ionen gereinigt. Wenn Sie Silbernitrat (AgNO3) hinzufügen, lösen sich die Silber-Ionen (Ag+) und die Nitrat-Ionen (NO3–) einfach im Wasser auf:
Da keine Reaktionspartner vorhanden sind, mit denen die Silber-Ionen ein schwerlösliches Salz bilden könnten, bleibt die Lösung klar und farblos.
Leitungswasser enthält gelöste Mineralstoffe. Je nach Region sind darin auch geringe Mengen an Chlorid-Ionen enthalten. Sobald die Silber-Ionen auf diese Chlorid-Ionen treffen, kommt es zur Bildung von Silberchlorid (AgCl):
Da Silberchlorid in Wasser extrem schwerlöslich ist, bilden sich winzige Feststoffpartikel. Da die Chlorid-Konzentration im Leitungswasser meist gering ist, entsteht nur eine leichte, milchige Trübung. Bei Salzwasser fällt die Trübung umso stärker aus.