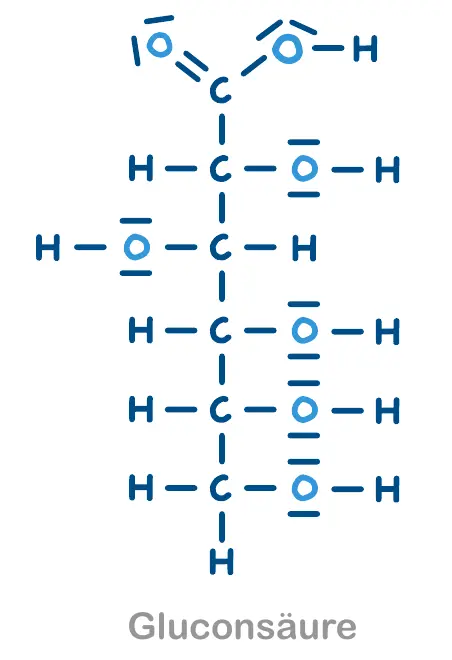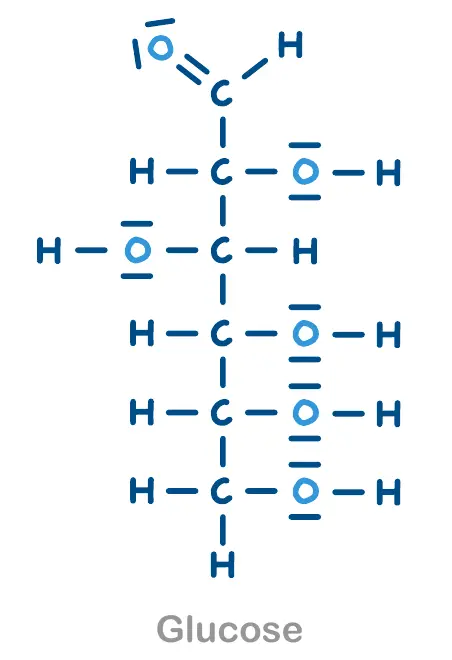Eine Produktionsart von Weihnachtskugeln
Weiteres
Wussten Sie, dass der glänzende Silberspiegel im Inneren einer Weihnachtskugel großindustriell meist durch ein chemisches Verfahren erzeugt wird?
Ja, aber nur bei hochwertigen Weihnachtskugeln aus Glas. Günstige Weihnachtskugeln werden meist mit Aluminium von außen bedampft, das dann nur silbrig aussieht. Echtes Silber kommt hier dann nicht zum Einsatz.
Ich habe mal gelesen, dass man für die Versilberung Zucker benötigt, aber warum, weiß ich nicht so genau.
Weiteres
Ein Weihnachtsbaum mit silbernen Kugeln. 1
Aufgaben
- Führen Sie die Tollensprobe gemäß V1 durch.
- Werten Sie V1 mit M2 aus, indem Sie…
- die zugrunde liegende Redoxreaktionsgleichung von Silbernitrat mit Glucose notieren,
- die Oxidationszahl jedes Atoms in der Reaktionsgleichung notieren,
- den Ort der Oxidation und Reduktion durch Beschriftung und Pfeile kennzeichnen.
- Geben Sie die funktionelle Gruppe des Ausgangsstoffes an, die sich durch Silbernitrat oxidieren lässt.
Die Tollensprobe
Materialien
- Schutzbrille
- Abzug
-
1 sehr sauberes Reagenzglas
- Neu oder gut reinigen: Spülmittel → gründlich spülen → mit dest. Wasser nachspülen → abtropfen lassen
- Pipetten
-
600 mL Becherglas
- dient als gemeinsames Wasserbad
- Wasserkocher
- Watte - angefeuchtet
Chemikalien
-
Silbernitrat-Lösung 0,1 mol/L
- Hinterlässt bräunlich/schwarze Flecken auf der Haut!
- Natronlauge 2 mol/L
- konz. Ammoniak-Lösung
- Glucose-Lösung 10 %
Sicherheitshinweise
- Konzentrierter Ammoniak bildet stechende, reizende Dämpfe, sodass die ihre Zugabe unter dem Abzug erfolgen muss!
- Silbernitrat hinterlässt braun/schwarze Flecken auf der Haut. Ihr Kontakt mit der Haut und den Augen ist daher strengstens zu vermeiden.
- Die Tollens-Reagenzlösung darf nicht aufbewahrt werden. Beim Austrocknen können sich gefährliche, empfindliche Silberverbindungen bilden. Zudem sind Silbernitrat-Lösungen umweltschädlich und gehören nicht in den Abguss. Sie werden am Ende des Versuchs in einem Sammelbehälter gesammelt und später fachgerecht entsorgt.
Durchführung
- 3 mL Silbernitrat-Lösung in ein Reagenzglas geben.
- 5 Tropfen Natronlauge hinzugeben. Es bildet sich eine weißliche Trübung.
- Unter dem Abzug tropfenweise konzentrierte Ammoniak-Lösung zugeben und dabei schwenken, bis die Lösung wieder klar wird.
- 2 mL Glucose-Lösung hinzugeben.
- Das Reagenzglas mit feuchter Watte sehr locker verschließen und im Abzug in ein Wasserbad auf ca. 80 °C für einige Minuten erwärmen.
- Dabei ab und zu beobachten.
Ein mögliches Ergebnis.2
Entsorgung
- Lösungen im Behälter für Schwermetallsalze sammeln.
- Das Reagenzglas sehr sorgfältig mit Wasser spülen.
Hinweise zur Auswertung
Es lässt sich in weiteren Versuchen zeigen, dass bei diesem Versuch…
- Glucose zu Gluconsäure reagiert
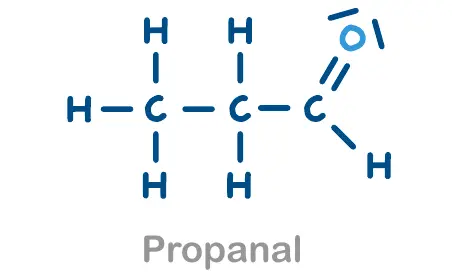
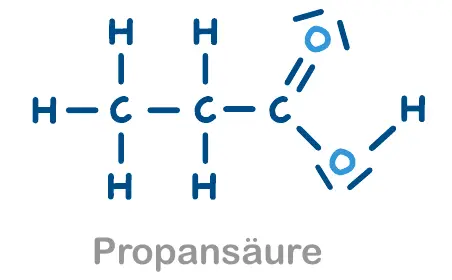
- Propanal zu Propansäure reagiert
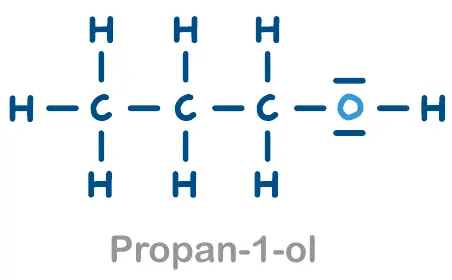
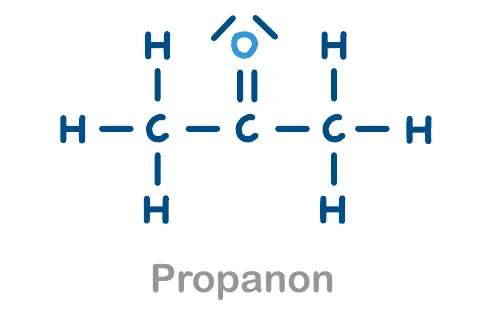
- Propanon nicht reagiert
- 1-Propanol nicht reagiert
Weiteres
Silbernitrat ist ein Salz, dass in Wasser Silber- und Nitrat-Ionen bildet. Nur die Silber-Ionen nehmen an der Redoxreaktion bei der Tollensprobe teil.
Weiteres
Warum reagiert Glucose, obwohl sie meist in einer „Ringform“ vorliegt? Ein kleiner Anteil ist in Wasser offenkettig und trägt dann eine Aldehydgruppe (–CHO). Diese ist für die Reduktion entscheidend.
Strukturformeln
Verschiedene Strukturformeln zur Auswertung. Die Glucose ist hier in der offenen Form dargestellt. 3
Die Auswertung weiter gedacht
- Wir haben die sogenannte Tollensprobe unter dem Fokus der Versilberung betrachtet. Nehmen Sie abschließend noch einmal den fachlichen Blickwinkel ein und erklären Sie, inwiefern es sich um eine Redoxreaktion und eine Nachweisreaktion handelt.
- Recherchieren Sie, welche Redoxreaktionen Grundlage der häufig alternativ genutzten Benediktprobe und Fehlingprobe sind.