Aufgaben
- Gemeinsamkeiten innerhalb einer Elementfamilie finden (arbeitsteilige Gruppenarbeit)
- Stelle in einer Übersicht heraus, was die Elemente der Elementfamilie der Alkalimetalle (M1 Gruppe A) oder der Elementfamilie der Halogene (M2 Gruppe B) jeweils für gemeinsame Eigenschaften haben.
- Öffne das PSE³ und mache dich mit der Darstellung vertraut (M3, auch die Legende lesen) und benenne die jeweils noch nicht genannten restlichen Mitglieder der Elementfamilien der Alkalimetalle (Gruppe A) und Halogene (Gruppe A).
- Betrachte noch einmal das Schalenmodell in M3 und formuliere, was jeweils das einzige Gemeinsame am Aufbau aller Atome der Alkalimetalle (Gruppe A) bzw. der Erdalkalimetalle ist (Gruppe A).
- Informiert euch über eure Ergebnisse (Gruppe A + B zusammen) und haltet dann in Stichworten nur die wesentlichen Unterschiede der Eigenschaften (Stoffebene) und des Aufbaus (Atomebene) aller Alkalimetalle im Vergleich zu allen Halogenen fest.
Typische Vertreter der Elementfamilie der Alkalimetalle
Unter einer Schutzflüssigkeit aufbewahrt
Lithium und Natrium gehören zur sogenannten Elementfamilie der Alkalimetalle. Alle Mitglieder dieser Elementfamilie haben einige Ähnlichkeiten:
Es sind silbrig glänzende, weiche Metalle, die man mit einem Messer schneiden kann. Beobachte einmal, was geschieht, wenn man sie anschneidet. Schon an der Luft reagieren sie. Deshalb werden Natrium und Lithium unter einer Schutzflüssigkeit gelagert, damit sie nicht mit Sauerstoff oder Wasser aus der Luft reagieren.
Schneiden von Lithium2
Schneiden von Natrium2
Reaktion mit Wasser
Alkalimetalle reagieren teils äußerst heftig mit Wasser. Für die folgenden beiden Videos siehst du, dass bei dieser Reaktion ein Gas entsteht. Deshalb bewegen sich Lithium oder Natrium auf dem Wasser. Wir haben außerdem noch eine Substanz hinzugegeben3, welche anzeigt, dass eine sogenannte alkalische Lösung entsteht.
Lithium reagiert mit Wasser2
Natrium wird in Wasser gegeben2
Natrium wird auf feuchtes Papier gegeben und kann sich nicht fortbewegen4
Innerhalb der Familie gilt: Je weiter unten ein Alkalimetall im Periodensystem steht, desto reaktiver ist es. Kalium reagiert mit Wasser noch heftiger als Natrium, Cäsium sogar so stark, dass es nur unter strengsten Sicherheitsbedingungen untersucht werden kann.
➡️ Wichtig: Alkalimetalle sind so reaktiv, dass sie in der Natur gar nicht „elementar“ vorkommen. Man findet sie nur in Verbindungen, zum Beispiel in Salzen. Für Experimente im Labor oder für technische Anwendungen müssen sie gezielt hergestellt werden.
Typische Vertreter der Elementfamilie der Halogene
Auf den ersten Blick verschiedene Nichtmetalle
Zur Elementfamilie der Halogene gehören unter anderem Fluor, Chlor, Brom und Iod. Alle vier Stoffe unterscheiden sich auf den ersten Blick zunächst deutlich im Aussehen und Aggregatzustand:
- Fluor ist bei Raumtemperatur ein blassgelbes Gas,
- Chlor ein gelbgrünes Gas,
- Brom liegt als rotbraune Flüssigkeit vor und
- Iod ist ein grauschwarzer, fester Stoff, der beim Erwärmen violette Dämpfe bildet.
Brom einfüllen5
Erwärmen von festem Iod6
Chlorgas ist äußerst gefährlich! Es wurde als tödliches Gas im 1 Weltkrieg eingesetzt.
Vorsicht: Im Haushalt kann es versehentlich entstehen, wenn man alkalische Badreiniger und saure Badreiniger vermischt. Folgendes Experiment zeigt dies, sollte aber unter keinen Umständen zu Hause nachgemacht werden!
Herstellung von Chlor im Labor4
Wirkung von Chlorgas auf eine Blüte5
Sehr reaktive "Salzbildner"
Halogene haben auch viele gemeinsame Eigenschaften: u. a. reagieren sie besonders gut mit Metallen und es bilden sich dabei Salze7 . Die Reaktionen z. B. von Chlor oder Brom mit Metallen verlaufen oft heftig und unter starker Energieabgabe.
Brom reagiert mit Aluminium5
Chlor regiert mit Eisen2
Es zeigt sich ein klarer Trend innerhalb der Familie:
Fluor ist das reaktivste Halogen überhaupt – es reagiert mit fast allen anderen Stoffen sehr schnell und so heftig, dass man in der Schule nicht damit arbeiten darf. Iod steht weiter unten in der Familie im Periodensystem und ist deutlich weniger reaktiv, zeigt aber weiterhin die für Halogene typischen Reaktionen und wird u. a. daher in Desinfektionsmitteln eingesetzt.
➡️ Wichtig: Wegen ihrer hohen Reaktivität kommen Halogene in der Natur gar nicht elementar vor. Man findet sie fast ausschließlich in Verbindungen, zum Beispiel in Salzen. Um elementares Chlor oder Brom im Labor oder in der Industrie zu nutzen, müssen sie gezielt und aufwendig hergestellt werden.
Das Schalenmodell und das Periodenystem der Elemente
Ein genauerer Blick in das PSE
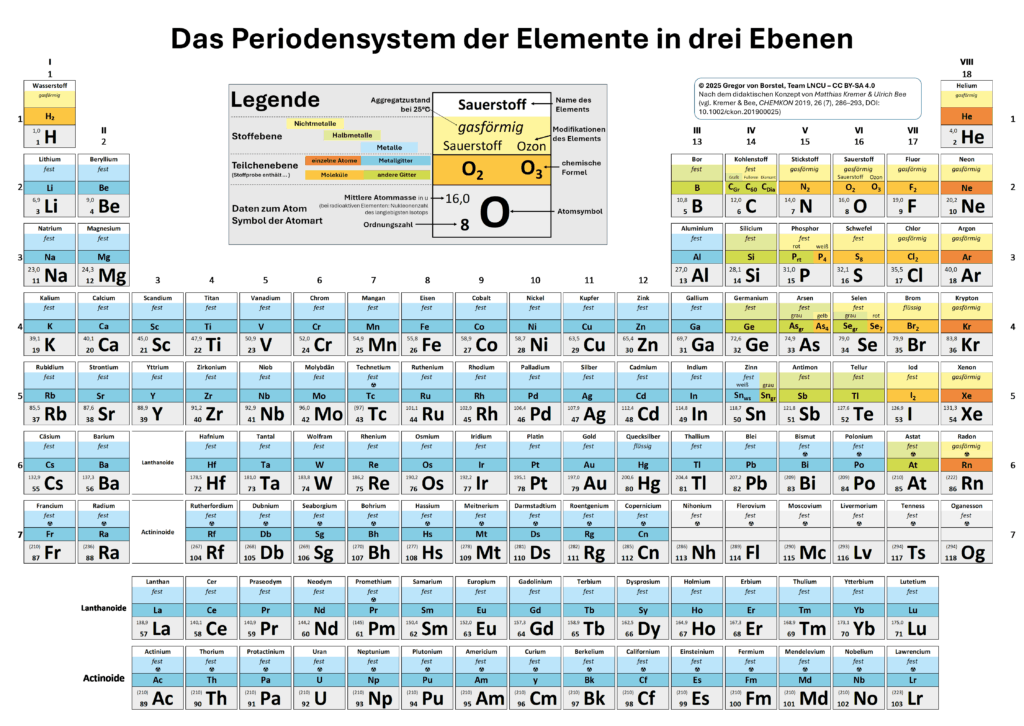
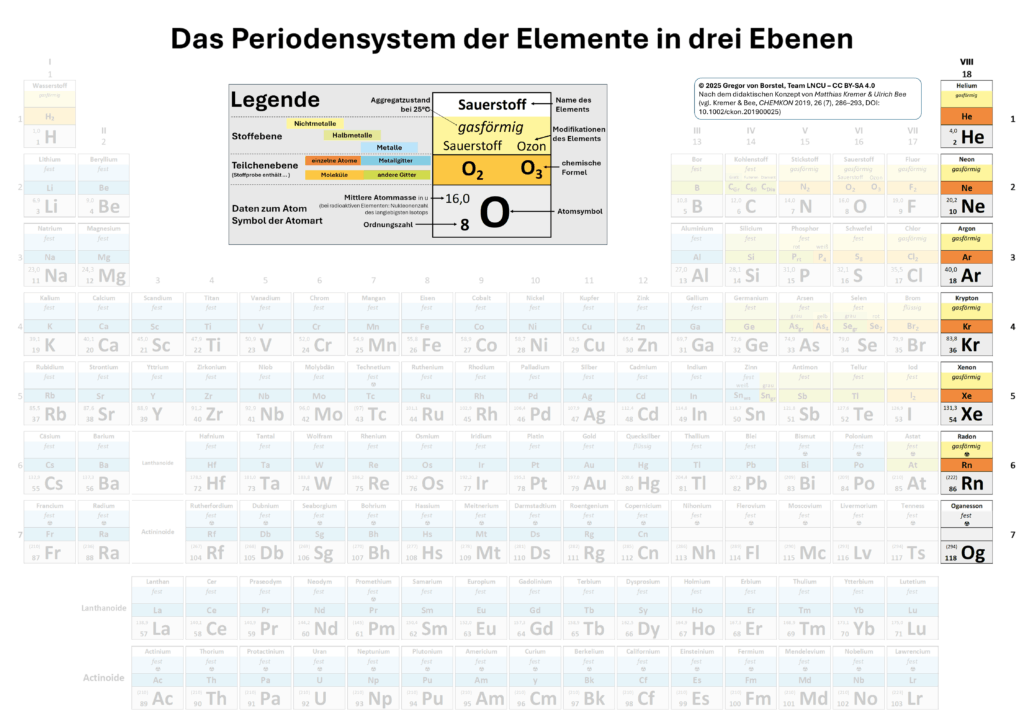
Das PSE in drei Ebenen8
Das Periodensystem der Elemente in drei Ebenen (PSE3) zeigt viele Informationen zu allen Elementen gleichzeitig auf drei miteinander verknüpften Ebenen: der Atomebene, der Teilchenebene und der Stoffebene.
Da wir es nun häufiger benötigen, haben wir es auf einer eigenen Seite hinterlegt und erklärt. Vielleicht machst du dir ein Lesezeichen?
Die Periodizität der Eigenschaften von elementaren Stoffen, die man ja bereits zu Mendelejews Zeiten kannte, ist kein Zufall. Wir wissen nun durch den Blick in die Atom, woher sie stammt!
Noch einmal ein Blick auf das Schalenmodell
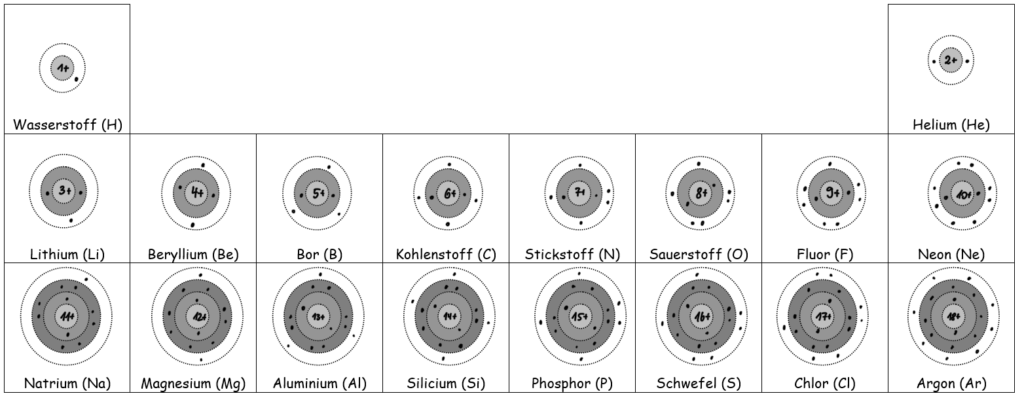
Hier noch einmal ein Blick auf die Elektronenverteilung im Schalenmodell.
Ausschnitt im Schalenmodell9
Formuliere noch einmal für dich: Was könnte allen Elementen einer Familie auf atomarer Ebene gemeinsam sein?