Wasserstoffbrücke – ein besonderer Fall der Anziehung zwischen Dipolen
"Gewöhnliche" Dipole
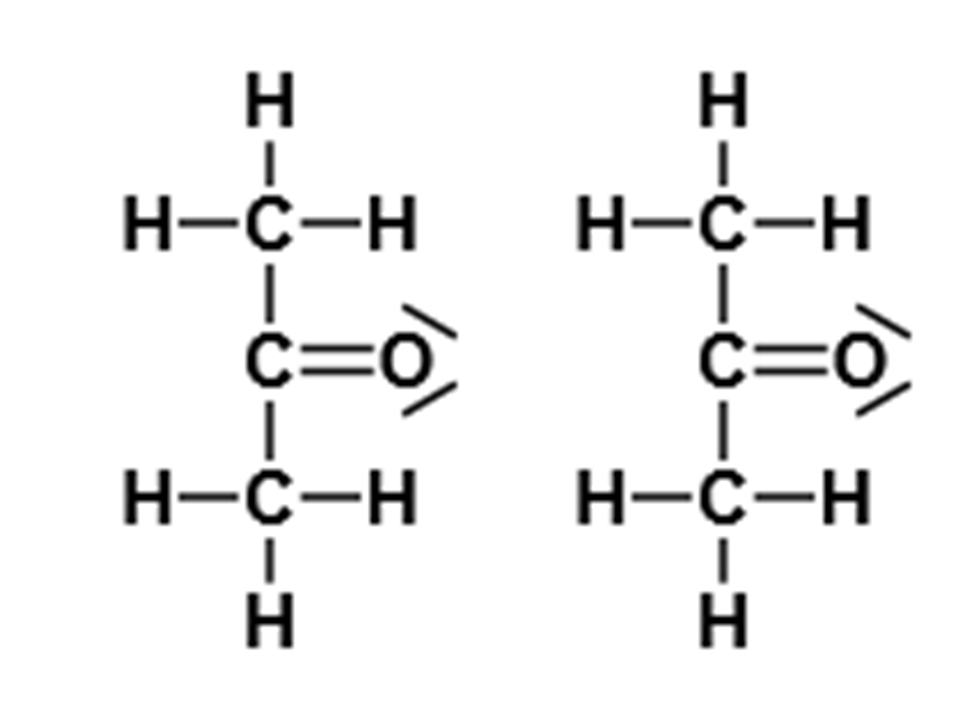
Bisher haben wir nur Wassermoleküle als permanente Dipole kennen gelernt. Im Folgenden betrachten wir einmal ein anderes Beispiel: Propanon-Moleküle. Sie sind etwas größer und jedes Propanon-Molekül bildet einen permanenten Dipol.
Ehrlich gesagt sind Propanon-Moleküle ganz „klassische“ Dipole. Wir hätten also auch am Beispiel von Propanon den Begriff und das Konzept der Dipol-Dipol-Wechselwirkung kennenlernen können.
Strukturformeln von zwei Propanon-Molekülen1
Erkennst du es? An einen Kohlenstoffatom ist ein Sauerstoffatom gebunden. Dort sind der Elektronenpaarbindungen polar!
Die Bindungen zwischen Kohlenstoffatomen und Wasserstoffatomen hingegen sind kaum polar. Dafür reicht die Differenz der Elektronegativitäten der beiden nicht aus.
Wassermoleküle sind nicht irgendwelche Dipole
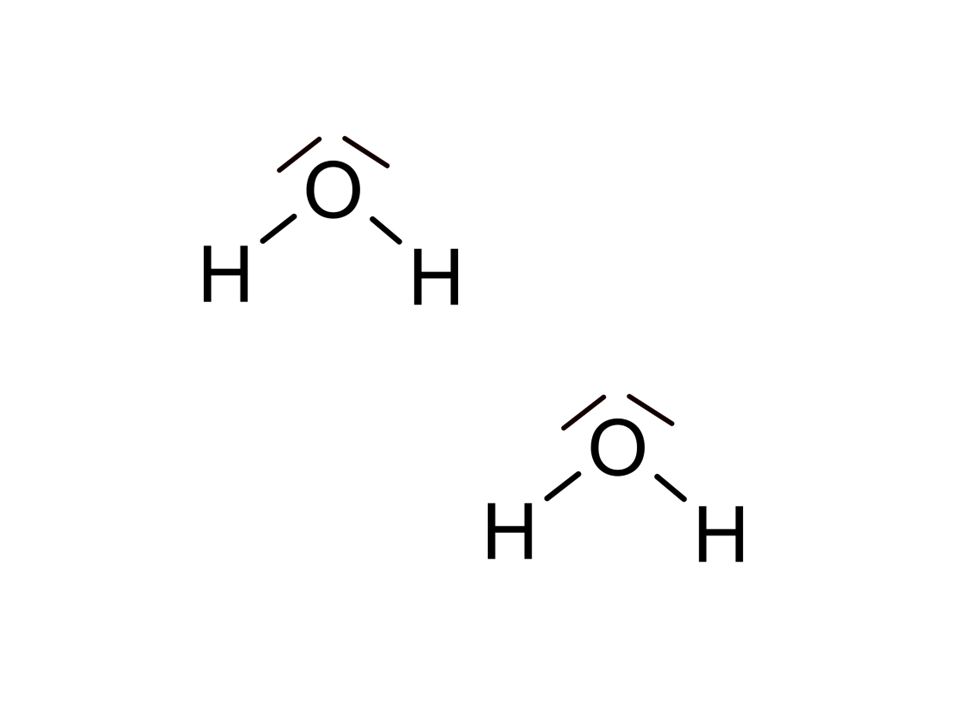
Wir haben gelernt: Wasser-Moleküle sind permanente Dipole. Das ist auch korrekt, denn es bedeutet, dass die Elektronen im Molekül dauerhaft ungleich verteilt sind. Der Sauerstoff zieht die Elektronen stärker an als die Wasserstoffatome. Dadurch entsteht im Wassermolekül eine positive Seite (bei den Wasserstoffatomen) und eine negative Seite (beim Sauerstoffatom). Zwischen solchen Dipolmolekülen wirken Dipol-Dipol-Wechselwirkungen. Beim Wasser gibt es dabei aber einen ganz besonderen Sonderfall: die Wasserstoffbrücke.
Was ist das Besondere im Wassermolekül
Wir vergessen oft, was das Besondere am Wasserstoffatom ist, wenn wir als Symbol den Buchstaben H schreiben. Schau noch einmal in das PSE³ – woraus besteht ein Wasserstoffatom?
Das Wasserstoff-Atom ist extrem klein und besitzt keine weiteren Elektronen, die es abschirmen könnten.
Wenn ein Wasserstoff-Atom an ein sehr stark elektronegatives Atom wie Sauerstoff gebunden ist, liegt seine positive Ladung damit fast „frei“.
Dieses stark polarisieret Wasserstoffatom kann also auf eine besonders starke Weise ein freies Elektronenpaar eines benachbarten Sauerstoffatoms anziehen. Man kann es sich so vorstellen, als ob das Elektronenpaar eine Brücke baut. Dies nennt man Wasserstoffbrücke. Das gibt es nur in Molekülen mit Wasserstoff-Atomen.
Wo kommt die Wasserstoffbrücken vor?
Ein Molekül muss ein ein äußerst stark positiv polarisiertes Wasserstoffatom2 enthalten! Diese besondere Wechselwirkung entsteht damit nur, wenn Wasserstoff (H) an sehr stark elektronegative Atome gebunden ist:
-
- Sauerstoff (O) → z. B. im Wassermolekül (H2O)
- Stickstoff (N) → z. B. Ammoniakmolekül (NH3)
- Fluor (F) → z. B. Fluorwasserstoffmolkeül (HF)
Bei Chlorwasserstoff (HCl) tritt sie nicht auf, weil Chlor schon nicht mehr stark genug an den bindenden Elektronen zieht.
Am Nachbarmolekül muss es ein freies Elektronenpaar geben.
Wie stark ist die Wasserstoffbrückenbindung?
Ihr Stärke beträgt ca. 1/10 der Stärke einer echten Elektronenpaarbindung. Damit sind sie viel stärker als andere Dipol-Dipol-Wechselwirkungen, an denen kein Wasserstoffatom beteiligt ist.
Besonderheiten im Wasser
Ein Wassermolekül kann mehrere Wasserstoffbrücken gleichzeitig eingehen:
- Die beiden Wasserstoffatome können Brücken zu anderen Wassermolekülen bilden.
- Die freien Elektronenpaare des Sauerstoffatoms können ebenfalls Wasserstoffbrücken anziehen.
So entsteht ein Netzwerk aus Wassermolekülen, das den starken Zusammenhalt und letztlich die hohe Wärmekapazität von Wasser erklärt. Das bedeutet, dass es viel Energie braucht, um die Temperatur von Wasser zu erhöhen und das Wasser erst bei verhältnismäßig hohen Temperaturen siedet.

Noch einmal genauer hingeschaut.3
Wir merken uns
Wasserstoffbrücken sind besonders starke Anziehungskräfte zwischen Wassermolekülen und ein Sonderfall der Dipol-Dipol-Wechselwirkungen. Sie erklären, warum Wasser trotz der geringen Größe der Wassermoleküle bei Raumtemperatur flüssig ist.
Aufgaben
- Zeichne zwei Propanon-Moleküle und zwei Wasser-Moleküle links und rechts nebeneinander oder lade dir Abb. 1 und Abb. 2 herunter und lege sie nebeneinander ab.
- Erstelle aus den Bildern die Grundlage einer Erläuterung der Begriffe Dipol-Dipol-Wechselwirkung (Abb. 1) im Vergleich zur Wasserstoffbrücke (Abb. 2) vor, indem du
- in die Abbildungen Markierungen und Symbole für polare Elektronenpaare, Teilladungen oder Anziehungskräfte zeichnest,
- in Gedanken- oder Sprechblasen die wichtigsten Begriffe dazu für dich notierst.
- Bereite dich damit auf einen vergleichenden Vortrag zu Wasserstoffbrücken vs. normalen Dipol-Dipol-Wechselwirkungen vor. Stelle dabei heraus: Was macht die Einzigartigkeit der Wasserstoffbrücke aus?
Weitergedacht
- Wassermoleküle sind Dipole – ohne Zweifel! Für wie sinnvoll oder störend erachtest du es im Rückblick auf deinen Lernprozess, dass wir mit diesem Spezialfall angefangen hatten, ohne ihn als solchen zu benennen?
Die Meere werden immer wärmer
Die Meere speichern und transportieren viel Wärme
Die Meere sind sehr gute Wärmespeicher. Das liegt an den Wasserstoffbrücken zwischen den Wassermolekülen: Um Wasser zu erwärmen, muss viel Energie aufgenommen werden. Dadurch können die Ozeane enorme Wärmemengen speichern, ohne sich schnell stark zu erhitzen.
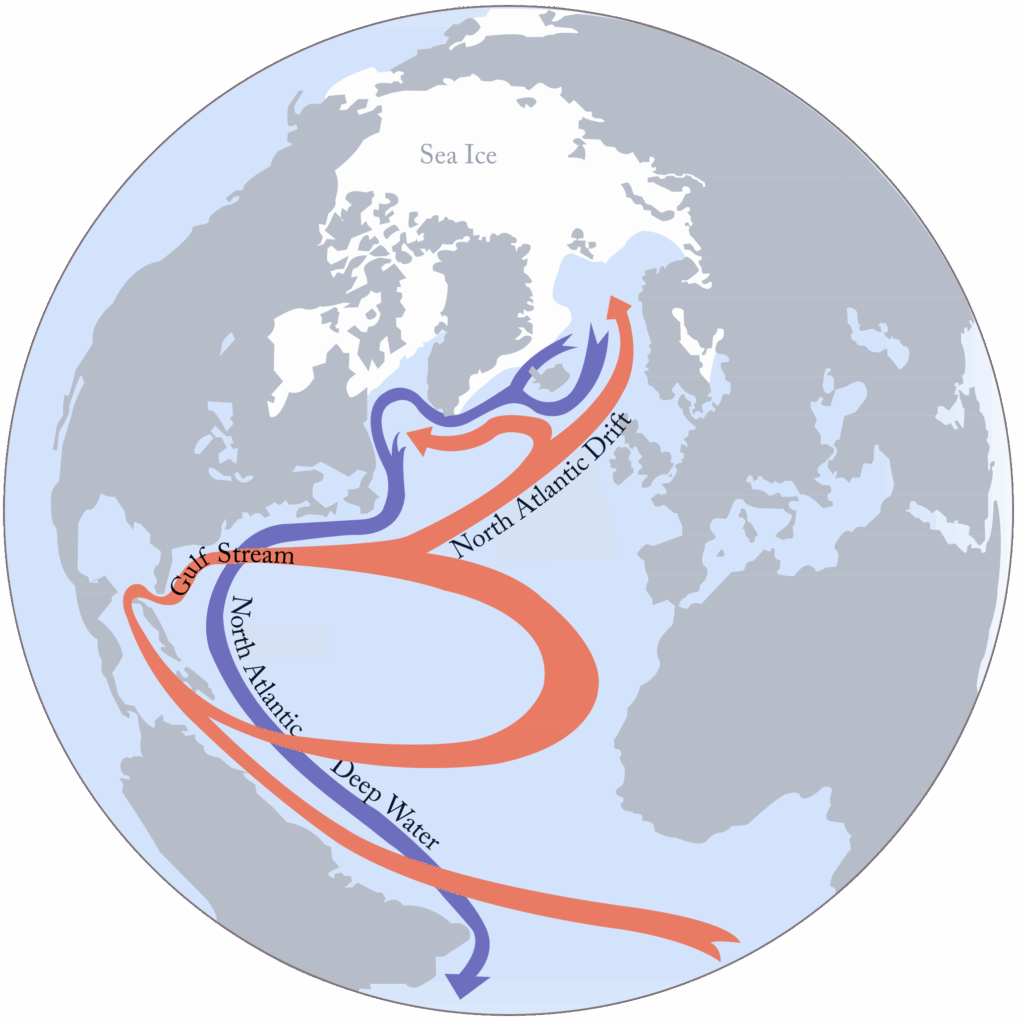
Davon profitieren wir Menschen z. B. in Deutschland besonders durch den Golfstrom. Diese Meeresströmung transportiert warmes Wasser aus den Tropen in Richtung Europa. Sie sorgt dafür, dass es bei uns milder und feuchter ist, als es auf derselben geografischen Breite eigentlich zu erwarten wäre.
Schema der Atlantikströmungen (stark vereinfacht). In rot die relativ warme Oberflächenströmung, in blau die kalte Tiefenströmung. Der nordwärtige Oberflächenstrom und der südwärtige Tiefenstrom ergeben zusammen die Umwälzbewegung des Atlantik (Atlantic Meridional Overturning Circulation, AMOC), populär auch als Golfstromsystem bekannt. 4
Für alle, die es genau wissen wollen: Die Wärmekapazität von Wasser
Folgendes ist interessant. Du kannst es aber überspringen, ohne das der Rest dann für dich unverständlich wird.
Die spezifische Wärmekapazität gibt an, wie viel Wärmeenergie benötigt wird, um 1 Kilogramm eines Stoffes um 1 Kelvin zu erwärmen. Sie wird berechnet sich nach der Formel:
- Q = zugeführte Wärmeenergie (in Kilojoule, kJ)
- m = Masse des Stoffes (in Kilogramm, kg)
- ΔT = Temperaturänderung (in Kelvin oder Grad Celsius)
Wasser hat hohe Wärmekapazität etwa 4,19 kJ/(kg·K), Ethanol zum Beispiel nur eine von etwa 2,6 kJ/(kg·K)
Was bedeutet das aber? Nun, ein typischer Energieriegel enthält etwa 800 kJ Energie. Stellen wir uns vor, wir verbrennen in komplett. Die enthaltene Energiemenge reicht dann aus, um 10 Liter Wasser (das entspricht etwa 10 kg) um knapp 20 °C zu erwärmen.
Würde dieselbe Energiemenge auf 10 Liter (etwa 7,9 kg) Ethanol übertragen, steigt dessen Temperatur um fast 40 °C.
Also etwa doppelt so stark wie bei Wasser.
Nun droht Ungemach!
Im Zuge des vom Menschen verursachten Klimawandels erwärmen sich die Ozeane jedoch immer stärker. Sie nehmen einen Großteil der zusätzlichen Wärme aus der Atmosphäre auf und waren 2025 so warm wie noch nie! Das hat gravierende Folgen: Erwärmtes Wasser dehnt sich aus, der Meeresspiegel steigt, und marine Lebensräume verändern sich. Viele Meerestiere, etwa Korallen oder kälteangepasste Arten, geraten unter starken Stress oder sterben ab.
Besonders gefährlich ist, dass es im Klimasystem sogenannte Kipppunkte gibt. Durch das Abschmelzen von Eis gelangt viel Süßwasser in den Nordatlantik. Dadurch könnte sich der Golfstrom abschwächen oder im Extremfall stark verändern. Für Europa hätte das massive Konsequenzen: kältere Winter, häufigere Extremwetterereignisse und veränderte Niederschlagsmuster.
Zusätzlich liefern wärmere Ozeane mehr Energie für die Atmosphäre. Das kann heftigere Stürme, stärkere Regenfälle und längere Hitzeperioden begünstigen. Was das für uns bereits heute bedeutet und in der Zukunft noch bedeuten kann, zeigt sehr eindrucksvoll die ZDF Doku Ozeane.
Weiteres
Die Fähigkeit der Meere, Wärme zu speichern, ist also einerseits ein Schutzmechanismus für das Klima – wird dieser Speicher jedoch überlastet, kann er zu einem zentralen Risiko für Mensch und Natur werden.
Weitergedacht
- Erläutere, warum große Gewässer wie Meere und Seen das Klima ihrer Umgebung beeinflussen. Gehe dabei auf Energieaufnahme, die langsame Erwärmung und verzögerte Abkühlung ein.
- In einer Diskussion sagt jemand: „Wenn sich die Meere durch den Klimawandel erwärmen, ist das gut für uns – Wasser kann ja viel Wärme aufnehmen und wieder abgeben.“ Nimm begründet Stellung, indem du erklärst,
- warum die hohe Wärmekapazität des Wassers zunächst stabilisierend auf die Temperatur der Erde wirkt,
- und warum die Erwärmung dennoch langfristig auch problematisch sein kann.
Wasserstoffbrücken in der DNA – Präzision im Inneren der Zelle
In der DNA finden wir auch Wasserstoffbrücken
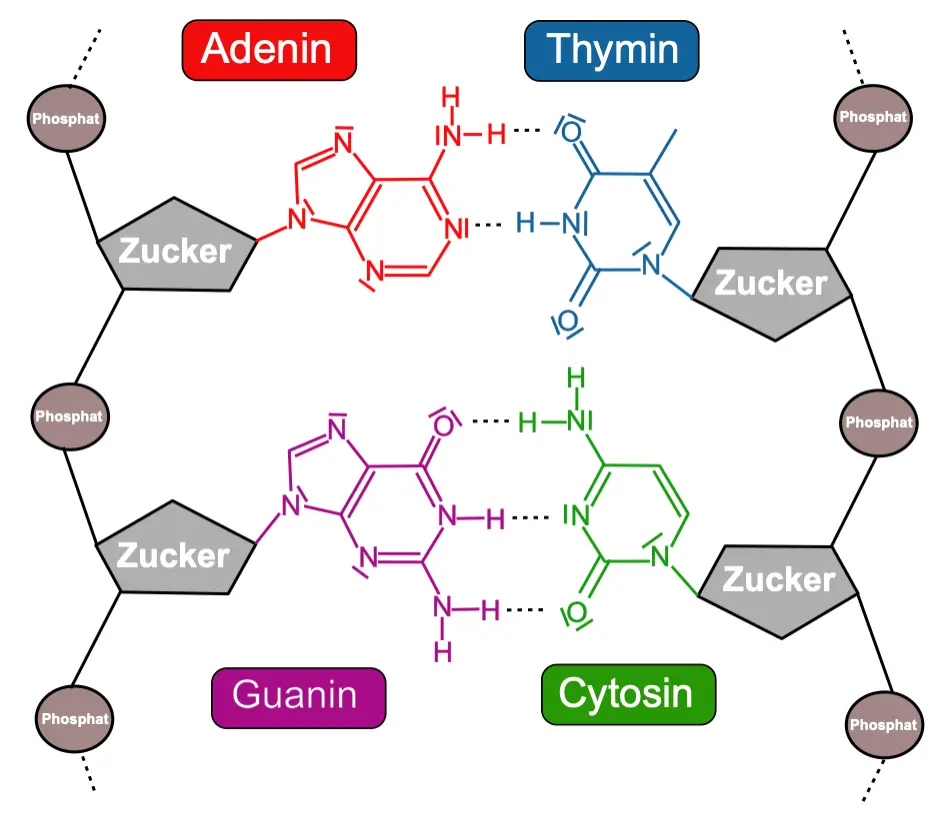
Wasserstoffbrücken spielen auch in der DNA eine zentrale Rolle. Die DNA besteht aus zwei langen Ketten, die wie eine verdrehte Leiter aufgebaut sind. Die „Sprossen“ dieser Leiter bestehen aus Basenpaaren:
- Adenin paart sich mit Thymin,
- Cytosin paart sich mit Guanin.
Was hält die beiden Stränge zusammen?
Die Basen sind nicht durch starke Elektronenpaarbindungen5, sondern durch Wasserstoffbrücken miteinander verbunden. Dabei entstehen zwischen Adenin und Thymin zwei, zwischen Cytosin und Guanin drei Wasserstoffbrücken.
Das Geniale daran
Diese besondere Bindungsart ist entscheidend:
Wasserstoffbrücken halten die DNA stabil zusammen, lassen sich aber bei Bedarf wieder lösen. So können sich die beiden DNA-Stränge beim Ablesen oder bei der Verdopplung trennen, und es lagern sich automatisch die passenden, „komplementären“ Basen an.
Auf diese Weise wird der genetische Bauplan mit sehr hoher Genauigkeit immer wieder kopiert.
Weitergedacht
In jeder Zelle unseres Körpers befindet sich die DNA. Sie enthält die Information dafür, wie unser Körper aufgebaut ist und funktioniert.
Damit neue Zellen entstehen oder Bauanleitungen für Proteine aus der DNA herausgelesen werden können, muss diese Information sehr zuverlässig weitergegeben werden. Dazu werden die beiden Stränge der DNA vorübergehend getrennt, und an jeden Strang lagern sich neue Bausteine an. Entscheidend ist dabei: Fast immer wird genau die richtige Base eingebaut. Der Grund dafür liegt in der Art der Wasserstoffbrücken, die die Basen miteinander bilden.
- Sieh dir die Strukturformeln der vier DNA-Basen Adenin (A), Thymin (T), Guanin (G) und Cytosin (C) genau an.
Beschreibe, welche Atome oder Atomgruppen an den Basen an der Bildung von Wasserstoffbrücken beteiligt sind. - Erkläre, warum Adenin nur mit Thymin und Guanin nur mit Cytosin stabile Wasserstoffbrücken ausbilden kann. Begründe, warum diese spezielle Passform der Basen dazu führt, dass beim Aufbau neuer DNA-Abschnitte nahezu immer die korrekt komplementäre Base angelagert wird.