Bearbeiten Sie die Aufgaben mit Hilfe der Zusatzinformationen in M1.
Aufgaben
- In einem Liter destilliertes Wasser lösen sich bei 25 °C 0,0018 g Silberchlorid. Wie groß ist das Löslichkeitsprodukt?
- In einem Liter destilliertes Wasser lösen sich bei 25 °C 0,0065 g Silberphosphat. Wie groß ist das Löslichkeitsprodukt?
- Zu einer wässrigen Lösung aus Natriumchlorid, Natriumbromid und Natriumiodid wird Silbernitrat-Lösung zugegeben. Stellen Sie eine begründete Vermutung zum Ergebnis dieser Zugabe auf.
- Eine Lösung enthält 0,1 mol/L Natriumchlorid und 0,1 mol/L Natriumchromat. Fällt bei Zugabe von Silbernitrat zuerst Silberchlorid oder Silberchromat aus?
- Tritt eine Fällung ein, wenn man 10 mL einer Lösung von Silbernitrat der Konzentration 0,1 mol/L mit 10 mL einer Kochsalzlösung der Konzentration 0,0001 mol/L vermischt?
- Wie viel Gramm Silberchlorid löst sich in einem Liter …
- destilliertes Wasser?
- einer 0,01 molaren Natriumchlorid-Lösung?
- Wie viel Gramm Bleichlorid lösen sich in 200 mL …
- destilliertes Wasser?
- Salzsäure mit einer Konzentration von 0,1 mol/L?
- Gegeben ist das Löslichkeitsprodukt von Calciumfluorid bei 25 °C.
- Wie groß ist die Konzentration der Calcium- und Fluorid-Ionen in der gesättigten Lösung?
- Wie viel Gramm Calciumfluorid lösen sich in 100 mL dest. Wasser bei 25 °C.
- Manche Salze haben eine größere Löslichkeit in Wasser, als nach dem Löslichkeitsprodukt zu erwarten wäre, z.B. Bariumcarbonat.
- Stellen Sie eine begründete Vermutung für dieses Phänomen am Beispiel von Bariumcarbonat auf.
- Machen Sie einen begründeten Vorschlag, wie sich die Löslichkeit von Bariumcarbonat steigern ließe.
Lösungen
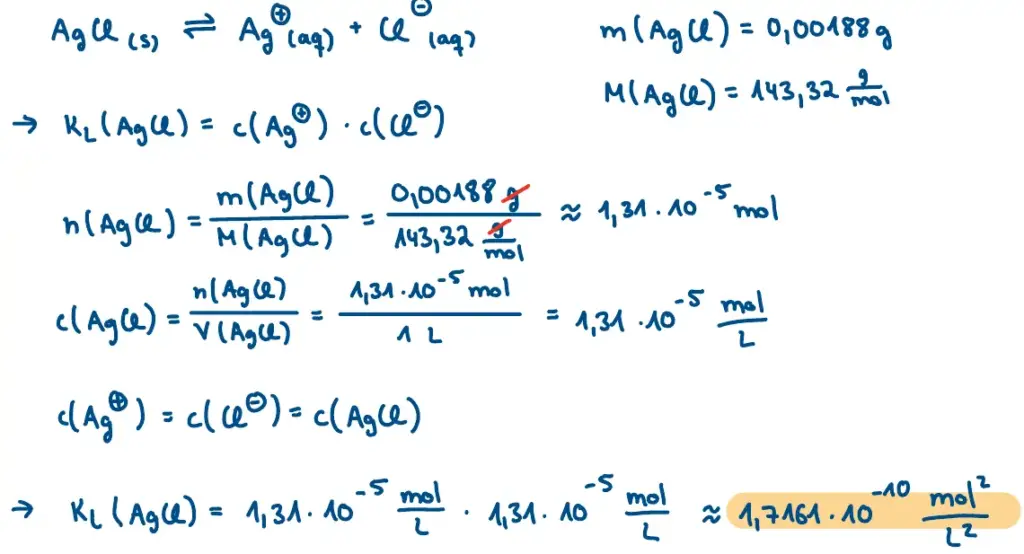
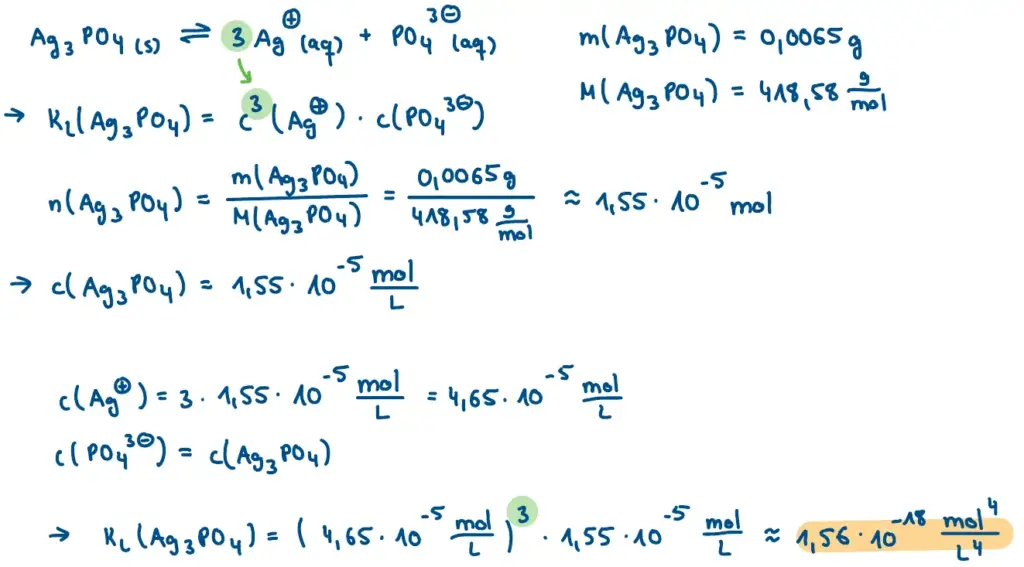
Die Zugabe von Silbernitrat bewirkt eine Ausfällung schwerlöslicher Silberhalogenide, wobei zuerst Silberiodid ausfällt, weil es das kleinste Löslichkeitsprodukt aufweist. Bei weiterer Zugabe von Silbernitrat fällt im Anschluss Silberbromid und dann Silberchlorid aus. Es findet also eine Fällung nacheinander statt, beginnend bei Silberiodid über Silberbromid zu Silberchlorid.
Um zu bestimmen, welches Salz zuerst ausfällt, müssen wir berechnen, welche Silberionen-Konzentration jeweils benötigt wird, um das Löslichkeitsprodukt des jeweiligen Salzes zu überschreiten.
Das Salz, das die geringere Menge an Silberionen benötigt, um auszufallen, wird zuerst als Feststoff ausfallen.
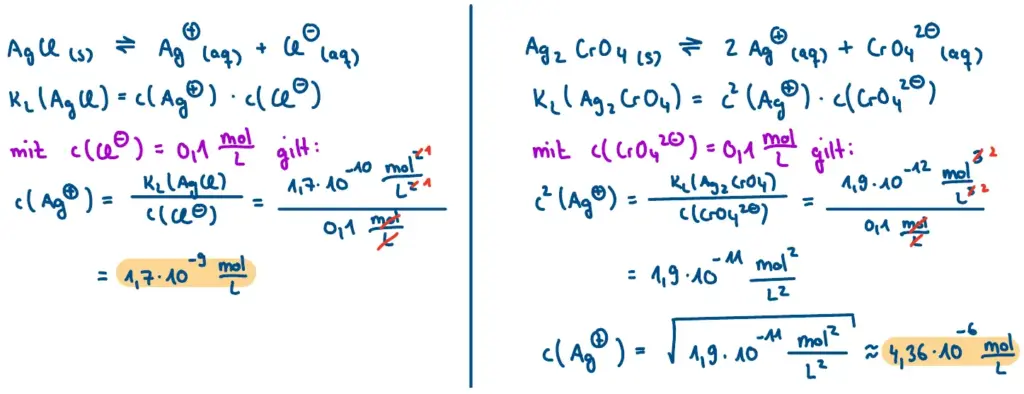
Es fällt zuerst Silberchlorid aus!
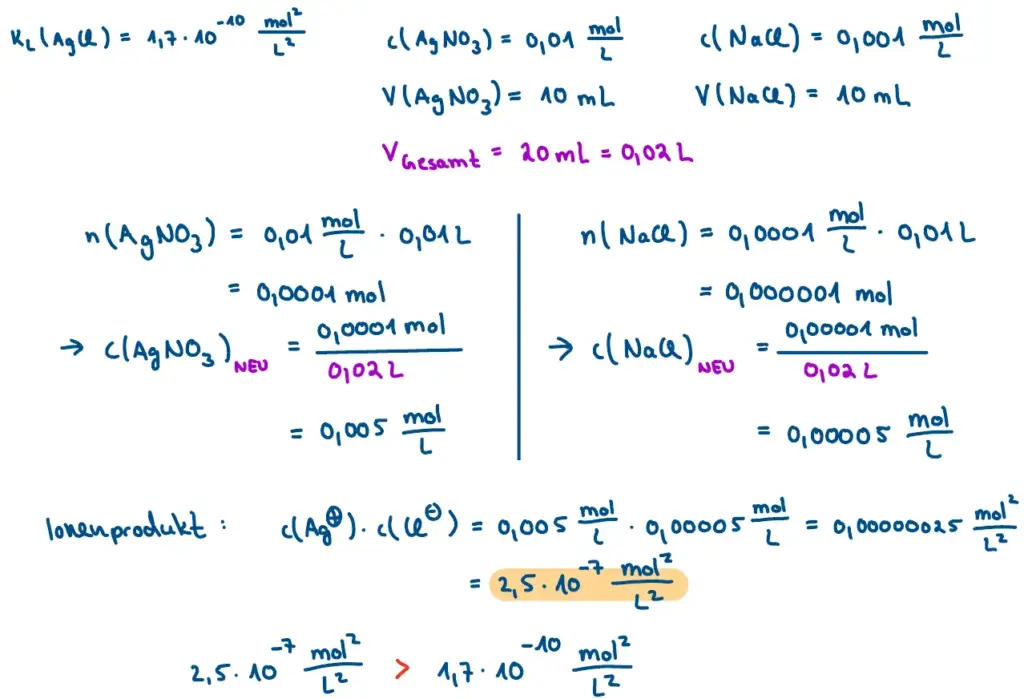
Das Ionenprodukt überschreitet den Wert von KL. Somit kommt es zu einer Fällung von Silberchlorid.
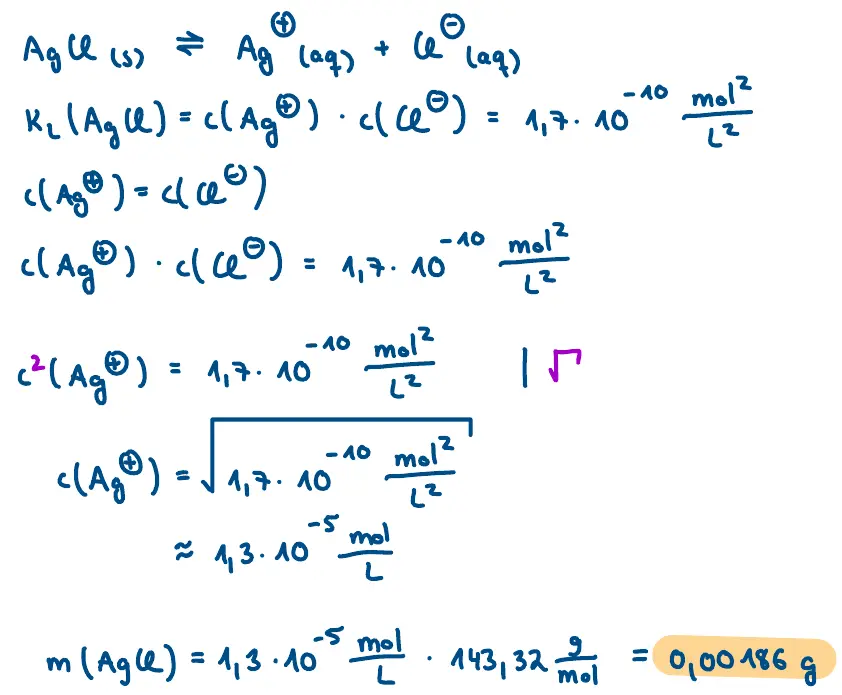
b).
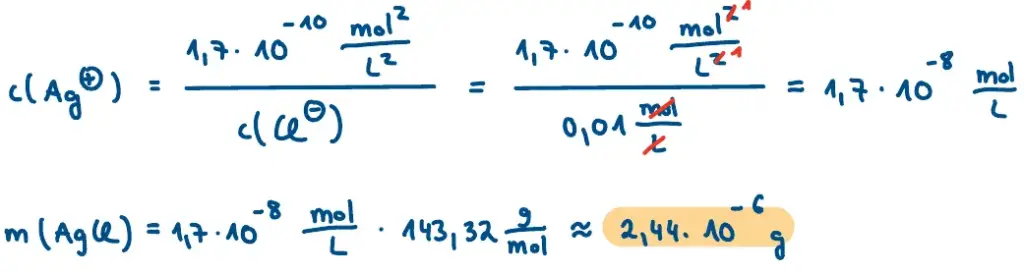
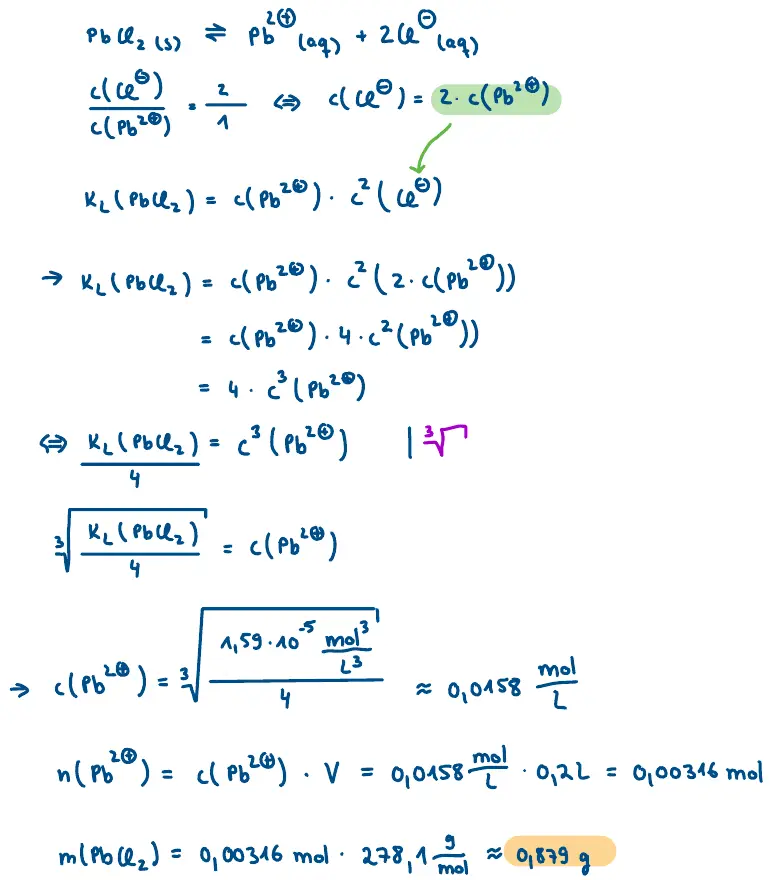
b).
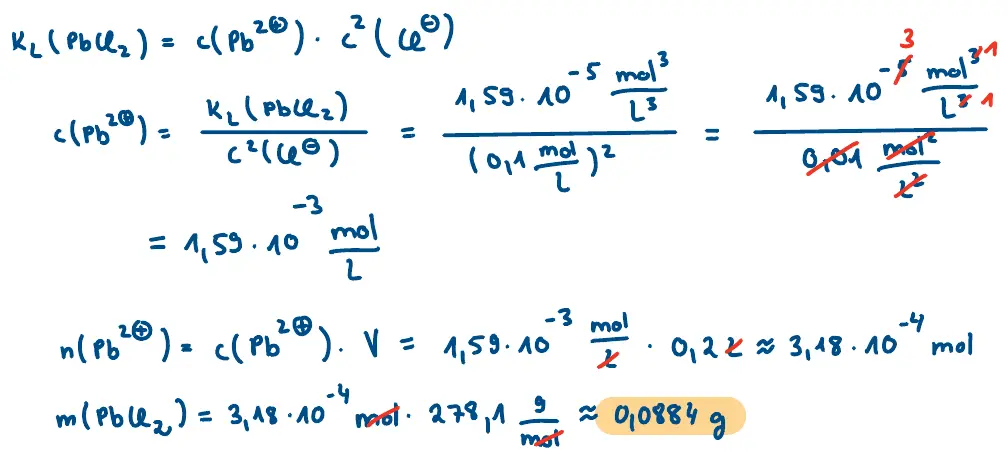

b).
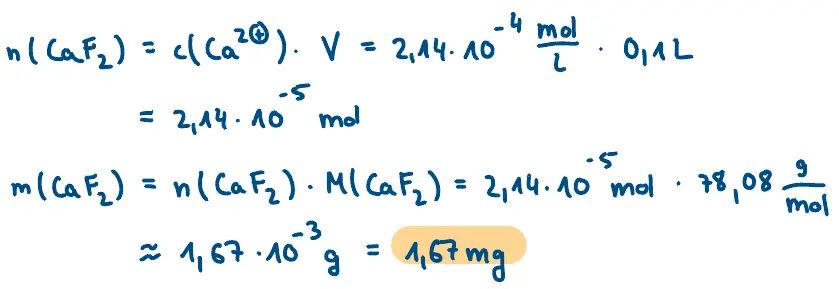
- Bariumcarbonat bildet in wässriger Lösung Barium- und Carbonat-Ionen
- Carbonat-Ionen reagieren basisch mit Wasser zu Hydrogencarbonat-Ionen. Dadurch wird die Konzentration an Carbonat gemindert.
- Das Lösungsgleichgewicht wird auf die Seite der Produkte verschoben, d.h. mehr Carbonat wird.
- Es geht also mehr Bariumcarbonat in Lösung bzw. Bariumcarbonat zeigt eine bessere Löslichkeit.
- Eine verbesserte Löslichkeit kann durch die Zugabe von Säure erwirkt werden, die ebenfalls die Konzentration an Carbonat-Ionen senkt.
