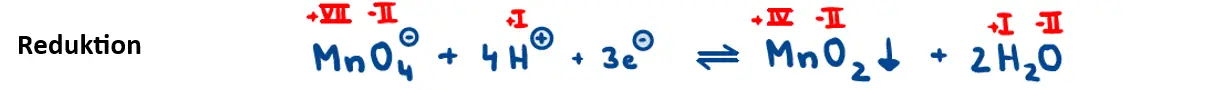Die Redoxtitration ist eine weitere Konzentrationsbestimmungsmethode, bei der jedoch das Prinzip der Redoxreaktion genutzt wird, um die unbekannte Konzentration eines oxidierbaren oder reduzierbaren Stoffes in einer Lösung zu ermitteln. Die Maßlösung, welche portionsweise zur Analyselösung zugeführt wird, enthält entweder ein Reduktions- oder ein Oxidationsmittel.
Kaliumpermanganat ist beispielsweise ein starkes Oxidationsmittel und besitzt als Feststoff und in Lösung eine intensiv violette Färbung. Trifft die Lösung auf einen oxidierbaren Stoff, wird Kaliumpermanganat selbst reduziert, wodurch seine charakteristische Färbung verloren geht.
Genau! Der Äquivalenzpunkt ist dann erreicht, wenn beim Zuführen der Maßlösung zur Analyselösung keine Farbänderung durch eine Redoxreaktion mehr stattfindet und die Analyselösung die violette Farbe der Maßlösung annimmt.
Aufgaben
- Führen Sie den nachfolgenden Versuch V1 durch und werten Sie ihn aus, indem Sie…
- die Versuchsbeobachtung in Hinblick auf die Anwesenheit bestimmter Ionen deuten und hieraus ableiten, welcher Bestandteil in der Analyselösung oxidiert wird.
- das zugrundeliegende Redoxschema inklusive aller Teilgleichungen notieren. Siehe hierzu die Tipps in M1 und M2.
- das Verhältnis der Stoffmengen von Eisen(II)sulfat zu Kaliumpermanganat mit Hilfe der Redoxgleichung ableiten.
- die Stoffmenge von Eisensulfat(II) in der Analyselösung gemäß des Stoffmengenverhältnisses berechnen.
- die Stoffmenge an Eisen(II)sulfat in Gramm umrechnen und mit ihrer Einwaage vergleichen.
Manganometrie - Redoxtitration einer Eisen(II)sulfat-Lösung
Materialien
- Schutzbrille
- 250 mL Becherglas (2x)
- Bürette
-
Stativmaterial
- Stativ, Stativmuffe, Stativklemme
- Glasstab
Chemikalien
- Kaliumpermanganat
- konz. Schwefelsäure
-
Kaliumhexacyanoferrat(II)
- Gelbes Blutlaugensalz
- dest. Wasser
-
Natriumthiosulfat-Lösung
- dient zur "Entschärfung" überschüssiger Kaliumpermanganat-Lösung
Vorbereitung
- Herstellung einer 0,02 molaren Kaliumpermanganat-Lösung: Lösen Sie 0,316 g Kaliumpermanganat-Lösung in 100 mL dest. Wasser auf (ausreichend für vier 25 mL Büretten).
- Herstellung der Analyselösung: Lösen Sie 0,556 g Eisen(II)sulfat-7-Hydrat in 100 mL dest. Wasser auf. Die Menge ist so gewählt, dass Sie mit 25 mL Maßlösung auskommen werden. Geben Sie noch 3 mL konzentrierte Schwefelsäure hinzu.
Durchführung
- Stativ aufbauen, Bürette daran befestigen und diese mit der vorbereiteten Kaliumpermanganat-Lösung auffüllen.
- Analyselösung vorlegen und in 1 mL Schritten die Maßlösung portionsweise hinzufügen. Nach jeder Zugabe mit einem Glasstab umrühren.
- Die Titration ist beendet, wenn beim Zuführen der Maßlösung die Analyselösung eine blasse lila/rot-Färbung erhält, die beim Umrühren nicht mehr verschwindet.
- Notieren Sie das Volumen an verbrauchter Maßlösung.
- Geben Sie eine Spatelspitze gelbes Blutlaugensalz zur Analyselösung.
Entsorgen und Aufräumen
-
Die Bürette zur Analyselösung entlassen. Im Anschluss mit Natriumthiosulfat-Lösung und dann mit dest. Wasser spülen. Zur Analyselösung 0,1 g Natriumthiosulfat-Lösung geben.
-
Die vereinigte Lösung in den Entsorgungsbehälter für Schwermetalle geben.
-
Alle verunreinigten Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
Kaliumpermanganat als Oxidationsmittel
Weiteres
Der Verlauf einer Redoxtitration mit Kaliumpermanganat ist pH-Wert-abhängig. Liegt nur eine schwach saure, schwach alkalische oder neutrale Lösung vor, erfolgt eine Reduktion des Mangans im Kaliumpermanganat-Ion nur zu Mangan(IV). Es entsteht das in Wasser schwer lösliche Salz Mangandioxid (MnO2), das wegen seiner Farbe auch Braunstein genannt wird:
Reduktion von Kaliumpermanganat unter Anwesenheit einer Säure. 1
Kaliumpermanganat ist ein starkes Oxidationsmittel, d.h. es ist in der Lage andere Stoffe zu oxidieren. Diese Stoffe geben Elektronen an das Permanganat-Ion ab, wodurch es selbst reduziert wird.
Ist die Reaktionslösung hingegen ausreichend sauer, wird das Mangan im Permanganat-Ion zu Mangan(II) reduziert. Als Nebenprodukt entsteht Wasser. Aber Vorsicht: Ein Ansäuern der Analyselösung darf nicht mit Salzsäure erfolgen, da die anwesenden Chlorid-Ionen zu elementarem Chlor oxidiert werden würden. Elementares Chlor ist bei Raumtemperatur ein Gas, welches hochgiftig ist. Das Redoxschema für die Redoxreaktion zwischen Kaliumpermanganat und Salzsäure würde also wie folgt aussehen:
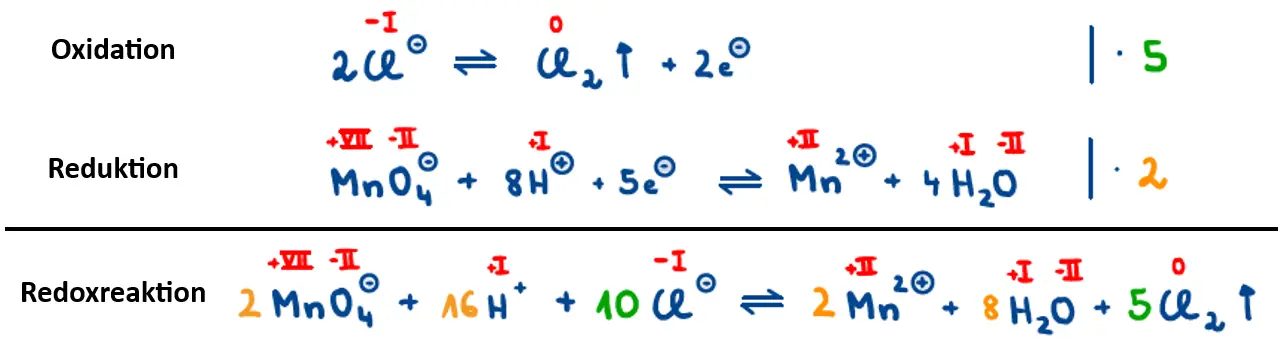
Redoxschema für die Redoxreaktion zwischen Kaliumpermanganat und Salzsäure.1
Bestimmung von Oxidationszahlen
Weiteres
Die Oxidationszahl stellt eine formale Ladung eines Atoms in einem Molekül oder Ion dar. Sie sind gedachte Ladungen, die in der Chemie verwendet werden, um die Verteilung von Elektronen in einer Verbindung zu beschreiben. Sie wird in römischen Ziffern (0, I, II, III, IV, V, VI …) über dem Elementsymbol angegeben, z.B.:
Beispiele für Oxidationszahlen. 1
Bestimmte Elemente haben in Verbindungen in den meisten Fällen eine bestimmte Oxidationszahl!
Halogene
Halogene ziehen aufgrund ihrer vergleichsweise hohen Elektronegativität Bindungselektronen zu sich. Ihre Oxidationszahl ist fast immer -I.
Sauerstoff
Sauerstoff zieht aufgrund seiner vergleichsweise hohen Elektronegativität Bindungselektronen zu sich. Seine Oxidationszahl ist fast immer -II.
Wasserstoff
Wasserstoff hat in Verbindungen fast immer die Oxidationszahl +I.
Metalle
Metalle haben in ionischen Verbindungen immer eine positive Oxidationszahl. Sie entspricht meist der Nummer der Hauptgruppe.
Die Oxidationszahl der Nebengruppenelemente lässt sich meist nur rechnerisch herleiten, indem zunächst die Oxidationszahl der anderen Bindungspartner ermittelt wird. Elementare Stoffe besitzen die Oxidationszahl 0!
Die Summe der Oxidationszahlen innerhalb einer Verbindung muss der Gesamtladung der Verbindung entsprechen.
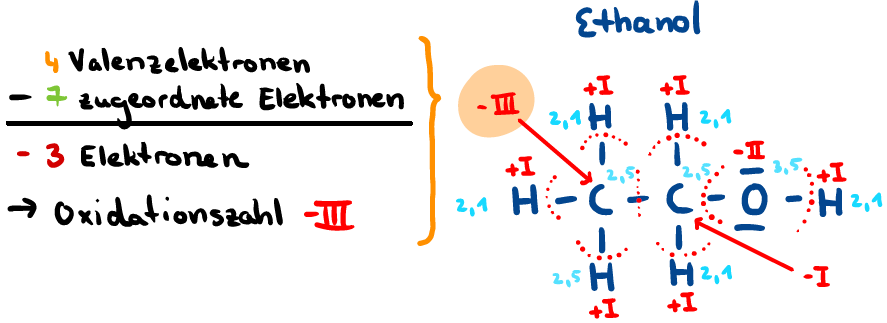
Die Oxidationszahl von Atomen in Molekülen lässt sich anhand der Valenzstrichformel ermitteln. Hierbei werden die Bindungselektronen eines jeden Atoms dem elektronegativeren Bindungspartner zugeordnet. Besitzen beide Bindungspartner die gleiche Elektronegativität, so werden jedem die Hälfte der Bindungselektronen zugeordnet. Zuletzt werden die zugeordneten Elektronen eines jeden Atoms addiert und von der Valenzelektronenzahl (entspricht meist der Hauptgruppe des Elements) des Atoms abgezogen.
Oxidationszahlen am Beispiel von Ethanol. 1
Übungen
- Üben Sie das Aufstellen von Oxidationszahlen mit Hilfe von M3.
- Üben Sie das Prinzip einer Redoxtitration am Beispiel von Oxalsäure mit Hilfe von M4. Nutzen Sie hierfür die Tipps in M5.
Oxidationszahlen üben
Weiteres
- Bestimmen Sie die Oxidationszahlen aller Atome von:
NH4+
K2Cr2O7
S2O32-
Cl2
Ca(OH)2
NaClO3
Au
Cu2+
H2O2
- Ordnen Sie mit Hilfe gestrichelter Linien die Elektronen der bindenden Elektronenpaare den Atomen in den Molekülen zu und geben Sie die Oxidationszahlen wie im obigen Beispiel für Ethanol an:
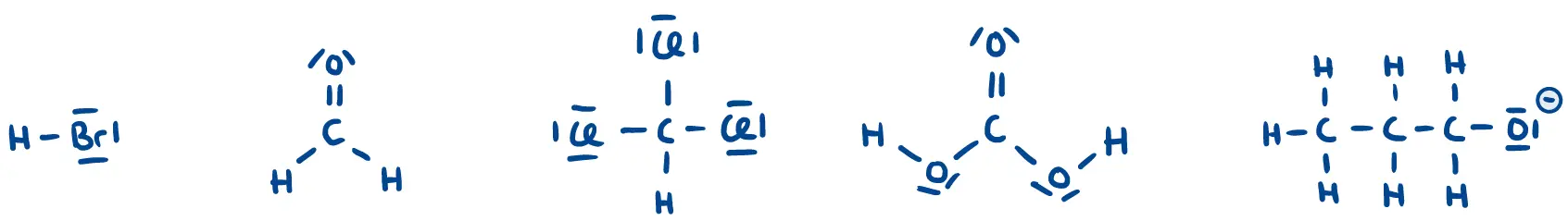
Redoxtitration von Oxalsäure
Weiteres
Bei der Redoxtitration einer Oxalsäure-Lösung mit einem Volumen von 200 mL wurden 25 mL Kaliumpermanganat-Lösung mit einer Konzentration von c(KMnO4) = 0,1 mol/L verbraucht. Bei der Titration entsteht ein Gas, das als Kohlenstoffdioxid identifiziert werden konnte. Am Boden der Analyselösung setzte sich ein brauner Feststoff ab.
Werten Sie den Versuch aus, indem Sie…
- die zugrundeliegende Redoxreaktion inkl. aller Teilgleichungen notieren. Beachten Sie die pH-Abhängigkeit der Wirkung von KMnO4 als Oxidationsmittel.
- das Verhältnis der Stoffmengen von Oxalsäure zu Kaliumpermanganat mit Hilfe der Redoxgleichung ableiten.
- die Stoffmenge und die Konzentration von Oxalsäure in der Analyselösung gemäß ihres Stoffmengenverhältnisses berechnen.
- die berechnete Stoffmenge an Oxalsäure in Gramm umrechnen. M(Oxalsäure)) = 90,04 g/mol)
Tipps zum Aufstellen von Redoxschemata mit Molekülen
Deute immer zuerst die Beobachtung: Im folgenden Beispiel entsteht bei der Verbrennung von Methan Kohlenstoffdioxid und Wasser.
Notiere dann die Teilgleichungen und beginne mit der Oxidation. Skizziere die Moleküle in der Valenzstrichformel (Lewisformel) und bestimme die Oxidationszahlen aller Atome im Molekül.
Weiteres
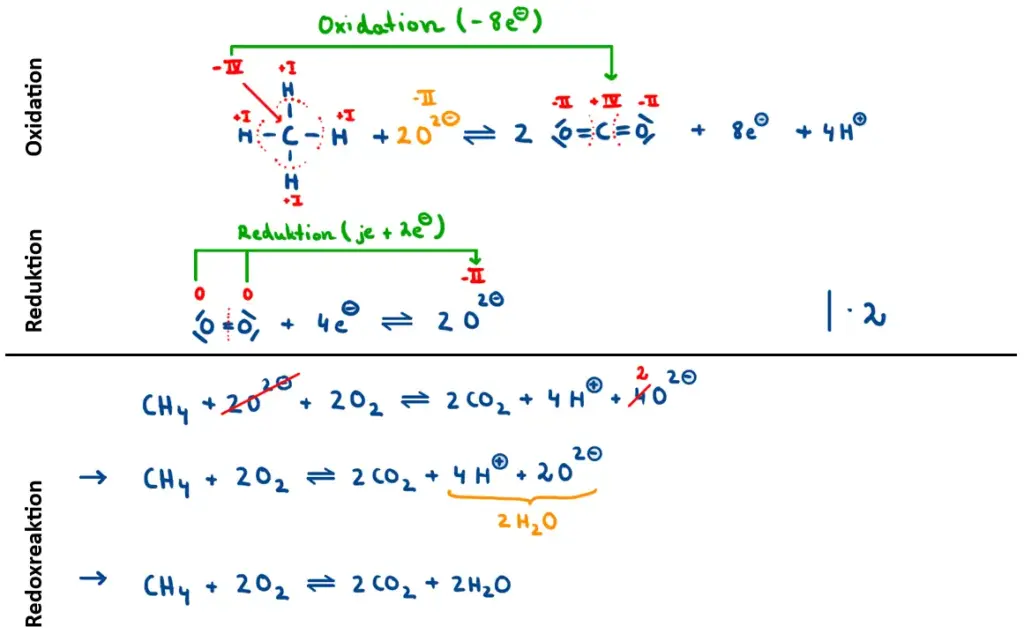
Tipps im Aufstellen von Redoxschemata am Beispiel der Verbrennung von Methan. 1
Aus der finalen Redoxreaktionsgleichung kann man entnehmen, dass 1 Methan-Teilchen mit 2 Sauerstoff-Teilchen reagiert. Hieraus ergibt sich das Stoffmengenverhältnis: