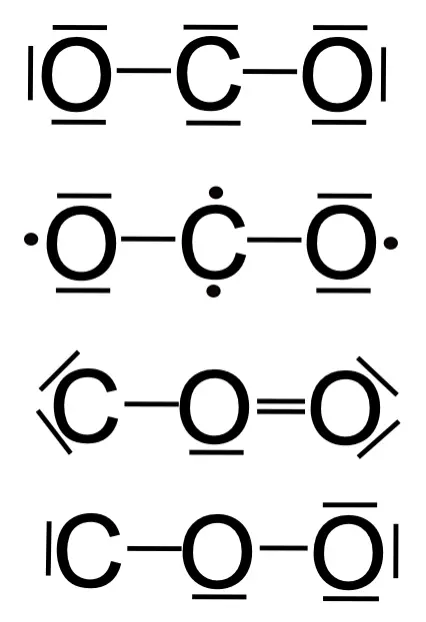Moleküle sind wichtig!
Das Leben beruht auf Molekülverbindungen
Alle Lebewesen bestehen überwiegend aus Molekülen! Moleküle sind Teilchen, die aus mindestens zwei Atomen zusammengesetzt sind. Was hält eigentlich die Atome in solchen Molekülen zusammen?
Z. B. die DNA oder Proteine. Das sind riesige Moleküle. Wir fangen einmal ganz klein an. Keine Sorge – du wirst das direkt verstehen!
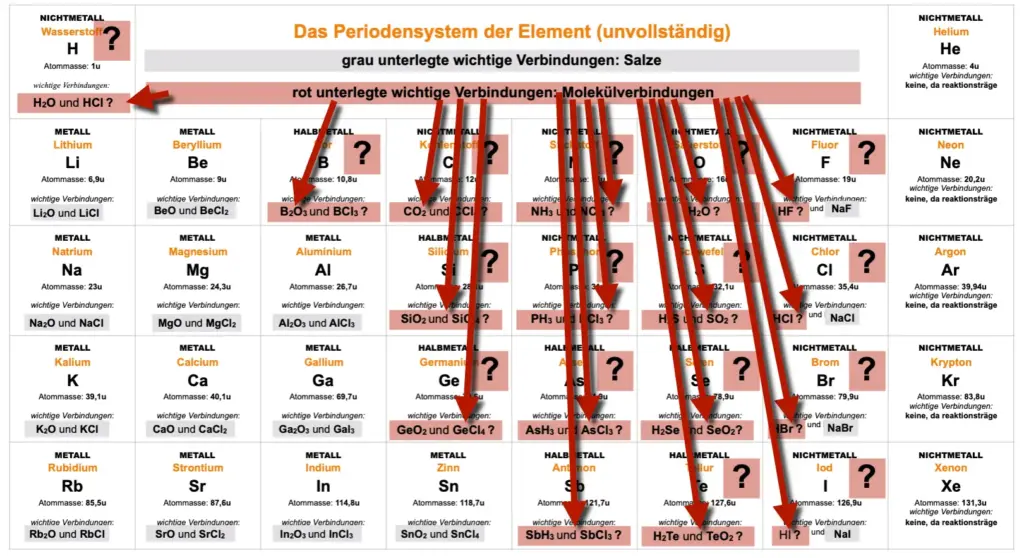
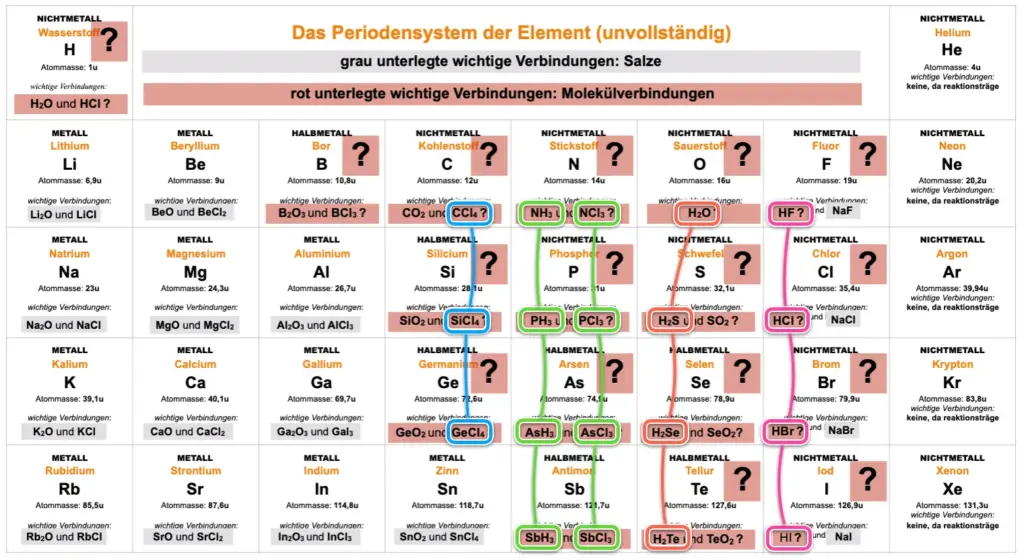
Wirf noch einmal einen Blick in die beiden Darstellungen des PSE3. Metalle bilden z. B. bei der Reaktion mit Sauerstoff oder mit Halogenen Salze, da bei der Reaktion Kationen und Anionen entstehen. Reagiert aber ein Nichtmetall wie Wasserstoff mit Sauerstoff oder Halogenen, entstehen keine Salze, sondern Molekülverbindungen. Was passiert bei der Reaktion auf Atomebene? Wieso bleiben die Atome in den Molekülen zusammen?
Ein erneuter Blick in das PSE
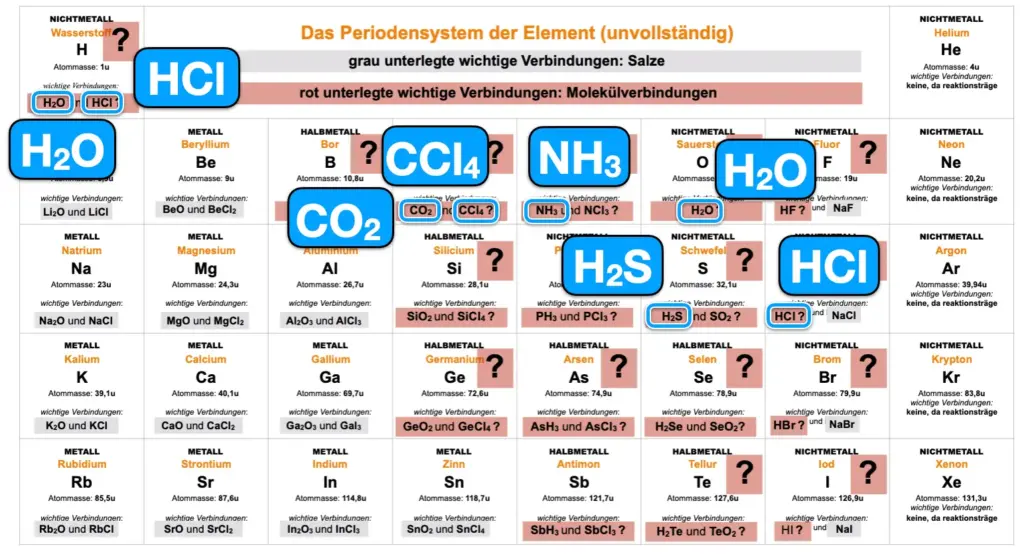
Manche Elemente bilden bei der Reaktion miteinander Salze….andere Molekülverbindungen PSE.1
Aufgaben
Wir arbeiten zuerst gemeinsam mit M2 und M3 ein Beispiel für die Bildung eines Moleküls durch. Du hast drei Aufgaben dabei:
- Vollziehe nach, was bei der Bildung des Wasserstoffmoleküls auf subatomarer Ebene passiert.
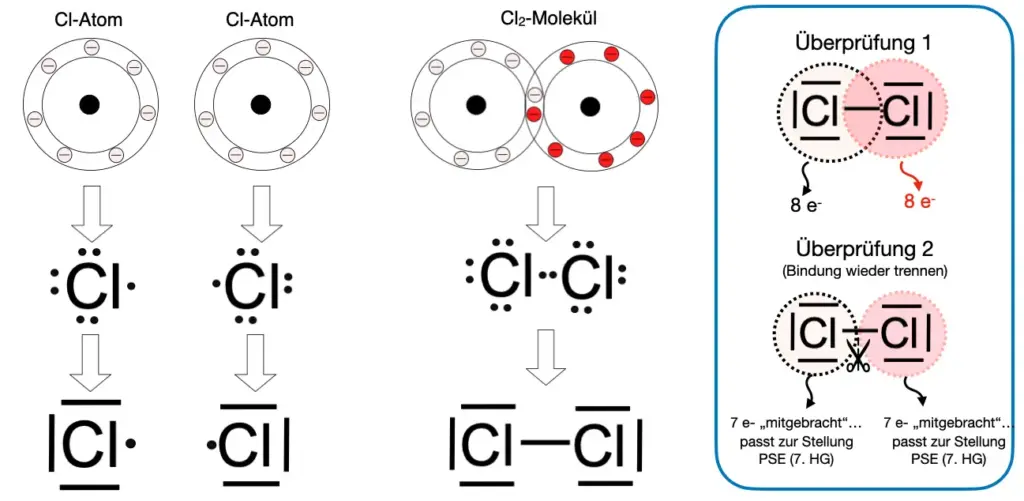
- Zeichne ein Cl2-Molekül und ein O2-Molekül, indem Du in einer vereinfachten Darstellung die Verteilung der Elektronen in den äußeren Schalen darstellst. (Eine Musterdarstellung findest Du in den Hinweisen. s.u.)
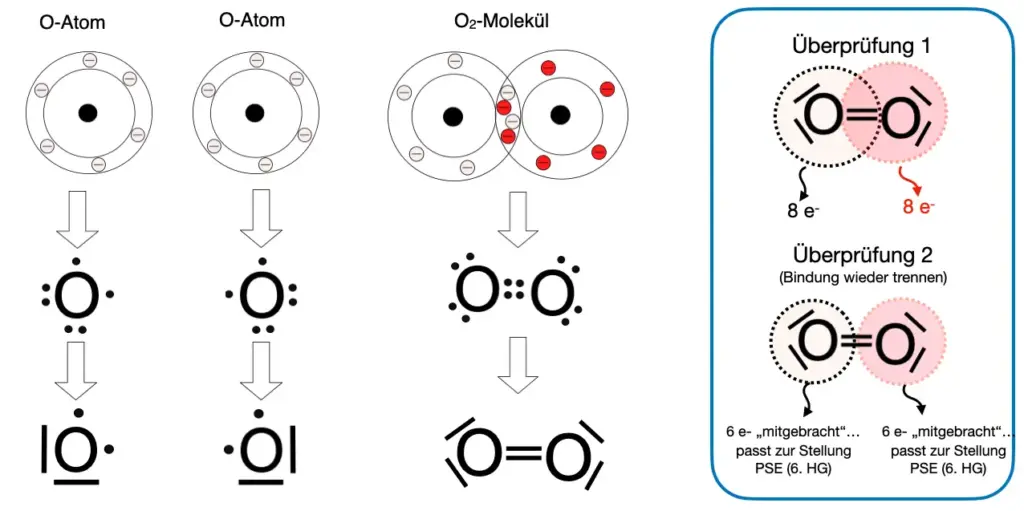
- Zeichne nun die Valenzstrichformeln und erkläre, wie man auch mithilfe der Valenzstrich-Formeln erkennen kann, ob keine Schale „überfüllt“ ist (siehe „Überprüfung 1“ in Abb. 6), ob die Anzahl der laut Formel „mitgebrachten“ Elektronen jedes Atoms zur Position des Elements im Periodensystem passt (siehe „Überprüfung 2“ in Abb. 6).
- Erstelle nun die Lewis-Formel für ein N2-Molekül.
Das einfachste Beispiel: ein Wasserstoff-Molekül
In Molekülen teilen sich Atome Elektronen
Stellen wir uns vor, zwei H-Atome treffen aufeinander. Was wird passieren?
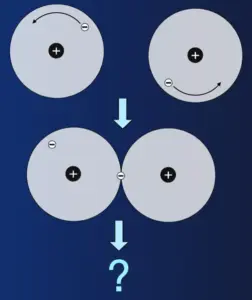
Treffen sich zwei H-Atome…2
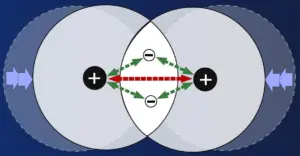
Wenn die Atome sich berühren, gelangen über kurz oder lang die Elektronen während ihrer Bewegungen um den Atomkern in den Bereich, in dem sie auch der Anziehungskraft des benachbartem Atomkerns ausgesetzt sind. In der Abbildung ist das für das Elektron des rechten Atoms dargestellt.
Das kann man aber auch anders betrachten: Das Elektron wird ja nicht nur von den Kernen angezogen – das Elektron übt ja auch eine Anziehungskraft auf die beiden Kerne aus! Es zieht die beiden Atomkerne also näher zusammen, so dass die Schalen der Atome überlappen. Da für das zweite Elektron prinzipiell das gleiche gilt, wird auch dieses sich dann bevorzugt zwischen den beiden Atomkernen aufhalten.
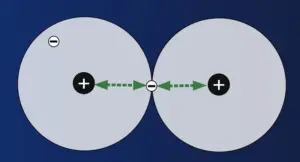
Die Elektronen halten sich bevorzugt im Überlappungsbereich zwischen den beiden Atomkernen auf, dort werden sie von beiden Kernen angezogen.2
Klar…und da die Atomkerne von beiden Elektronen angezogen werden, bleiben sie in dieser Konstellation zusammen, die Atome sind also verbunden. Da es zwei Elektronen im Überlappungsbereich sind, die die Atome zusammenhalten, spricht von einer Elektronenpaarbindung. Ein andere Bezeichnung lautet „kovalente Bindung“, weil zwei Valenzschalen Elektronen gemeinsam „nutzen“.
Werden denn jetzt die Atomkerne nicht immer näher zusammengezogen, so dass die Atome komplett miteinander „verschmelzen“?
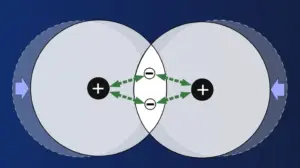
Das kann nicht passieren, da sich die Kerne immer stärker abstoßen, je näher sie sich kommen. Die Abstoßungskräfte zwischen den Kernen wären also stärker als die Anziehungskräfte, die die Elektronen auf sie ausüben.
Bei zu starker Überlappung der Schalen schieben die Abstoßungskräfte zwischen den Kernen diese wieder etwas auseinander.2
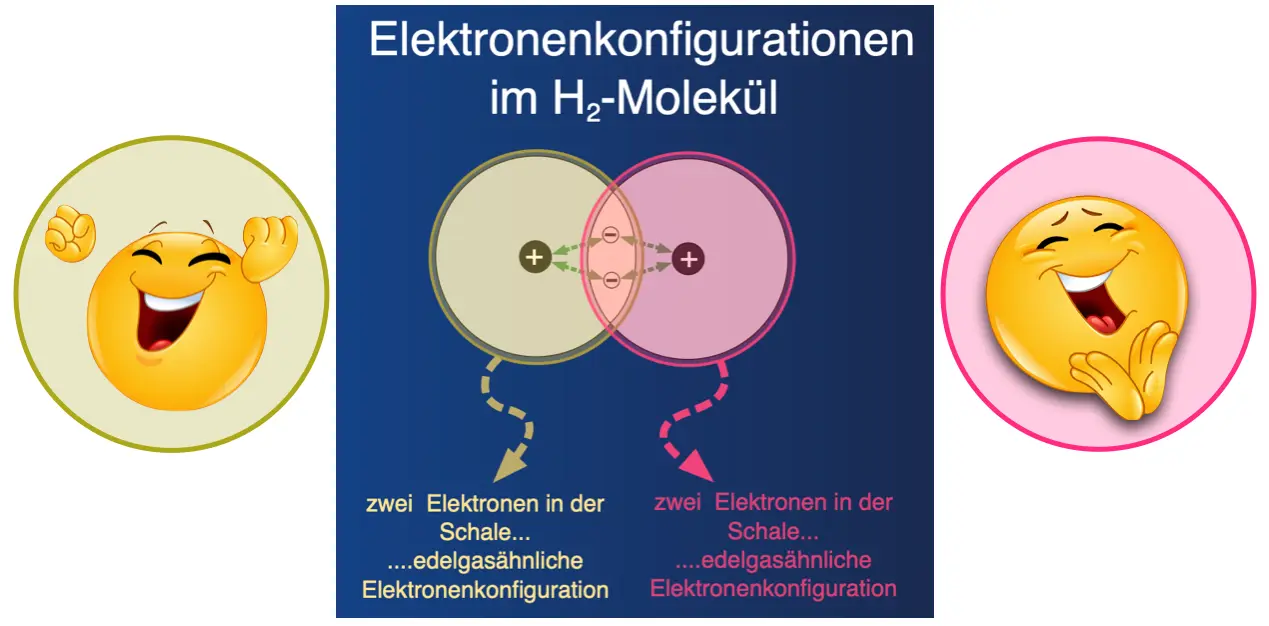
Eine letzter Aspekt: Wenn Atome Ionen bilden, erreichen sie durch das Abgeben bzw. Aufnehmen von Elektronen eine edelgasähnliche Elektronenkonfiguration. Wenn man sich die Schalen der Wasserstoffatome im H2-Molekül ansieht, stellt man fest, dass durch das Knüpfen der Elektronenpaarbindung beide Atome im Molekül eine edelgasähnliche Elektronenkonfiguration erhalten.
Darstellung von Molekülen mit Lewis-Formeln
Weiteres
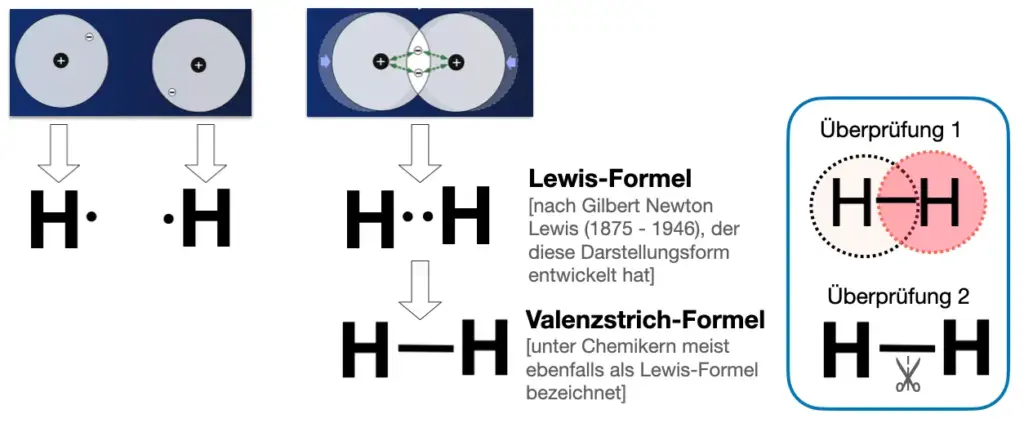
Um ein Wasserstoffatom und ein Wasserstoffmolekül nicht jedesmal mit überlappenden Schalen zeichnen zu müssen (was bei Atomen mit mehr Schalen und mehr Elektronen noch aufwendiger wäre), verwendet man die sogenannten Valenzstrich-Formeln bzw. Lewis-Formeln. (Die Begriffe werden oft synonym verwendet.)
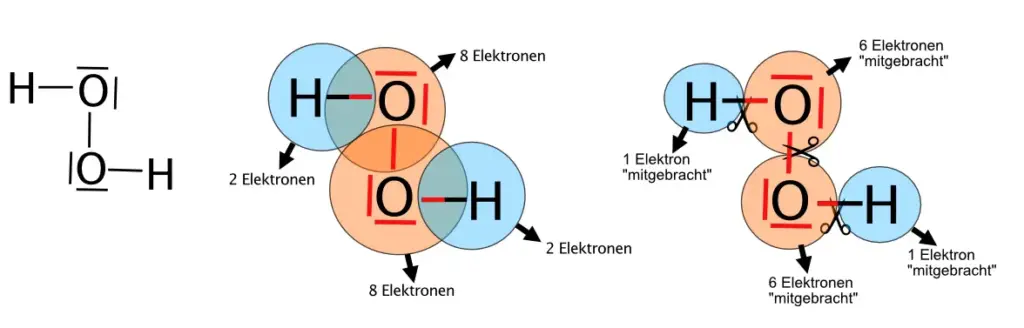
Mit den beiden Überprüfungsschritten kannst Du testen, ob in der gezeichneten Lewis-Formel die äußeren Schalen nicht mehr Elektronen enthalten, als sie aufnehmen können und ob jedes Atom die Anzahl an Elektronen „mitgebracht“ hat, die der Position des Elementes im Periodensystem entspricht.
Lewis-Formeln.2
Molekülbau für Fortgeschrittene: Moleküle aus verschiedenen Atomsorten
Weiteres
Im nächsten Schritt betrachten wir kleine Moleküle, die nicht nur aus Atomen des gleichen Elements bestehen, sondern in denen Atome verschiedener Elemente miteinander verknüpft sind.
Aufgaben für Fortgeschrittene
Im nächsten Schritt sollen Atome unterschiedlicher Elemente verbunden werden. Erstelle die Lewis-Formeln für ein H2O-Molekül, ein HCl-Molekül, ein CO2-Molekül, ein CCl4-Molekül, ein NH3-Molekül und ein H2S-Molekül. (Kontrolliere die Lewis-Formeln mit den zwei Überprüfungsschritten, korrigiere gegebenenfalls die Formeln.)
Lösungen zum Überprüfen
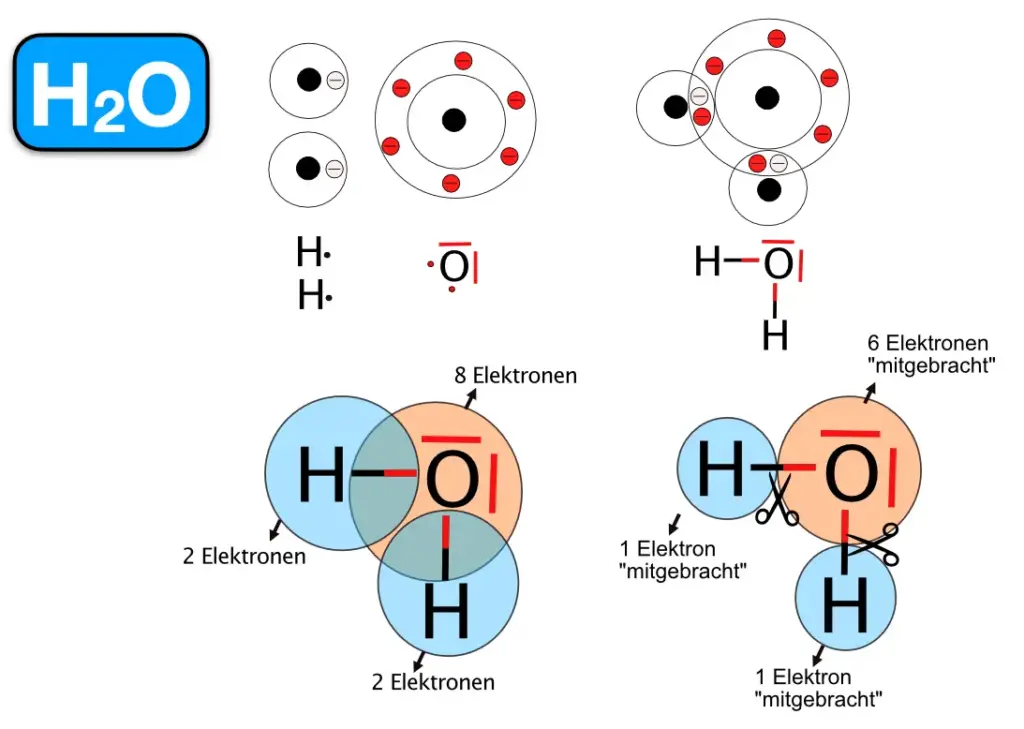
H2O-Molekül 3
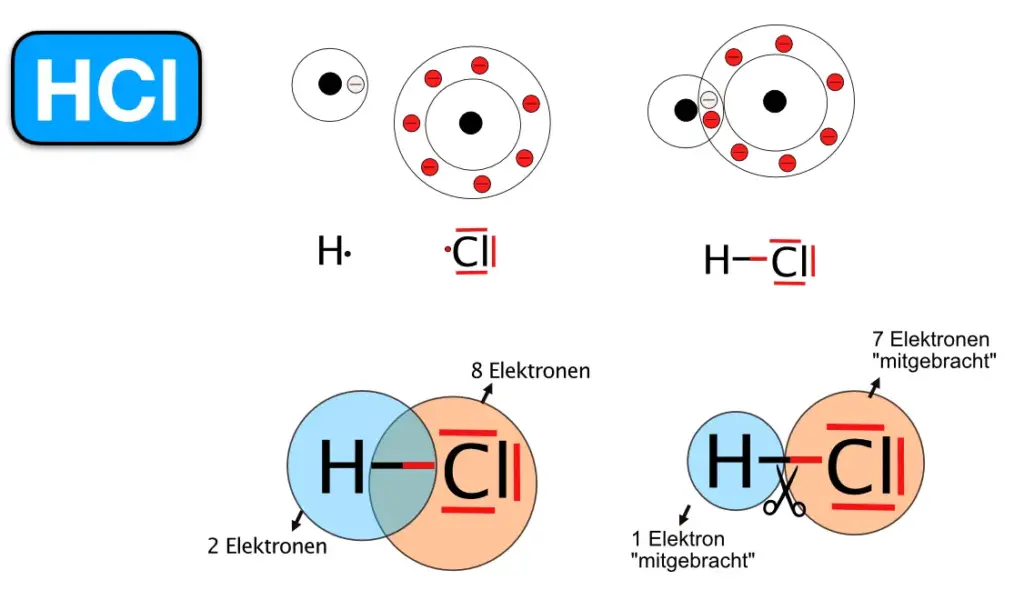
HCl-Molekül; die Moleküle entstehen bei der Reaktion von H2-Gas mit Cl2-Gas. Wenn man HCl-Gas in Wasser löst, entsteht Salzsäure. 2
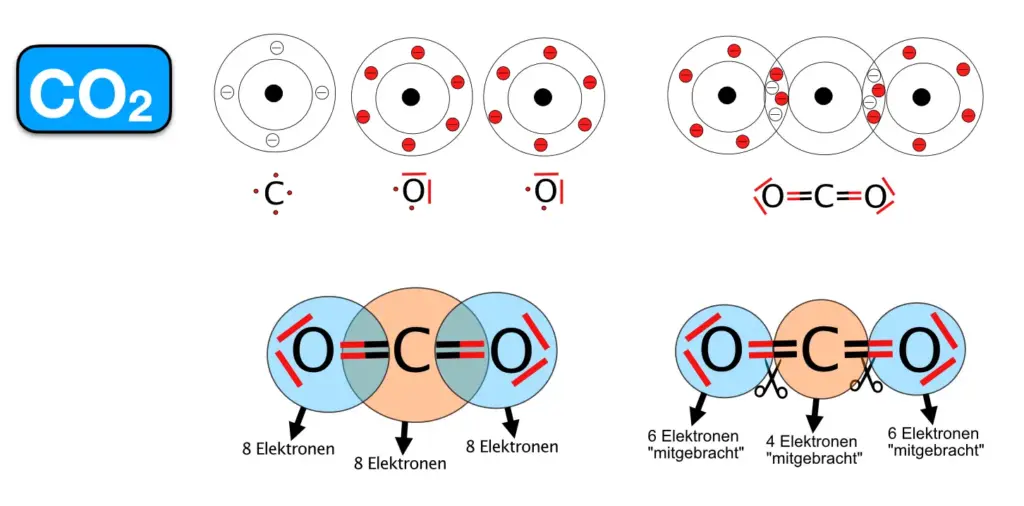
CO2-Molekül 2
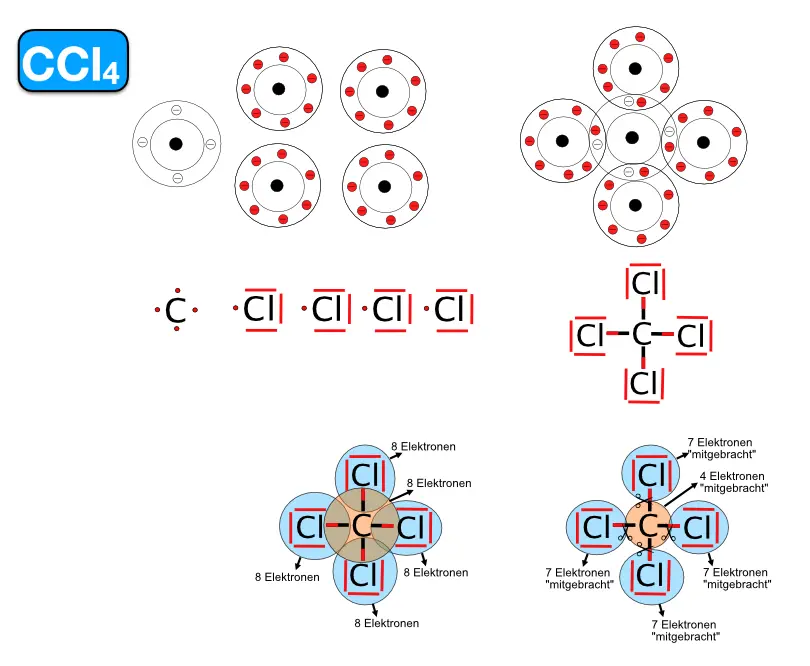
Tetrachlorkohlenstoff2
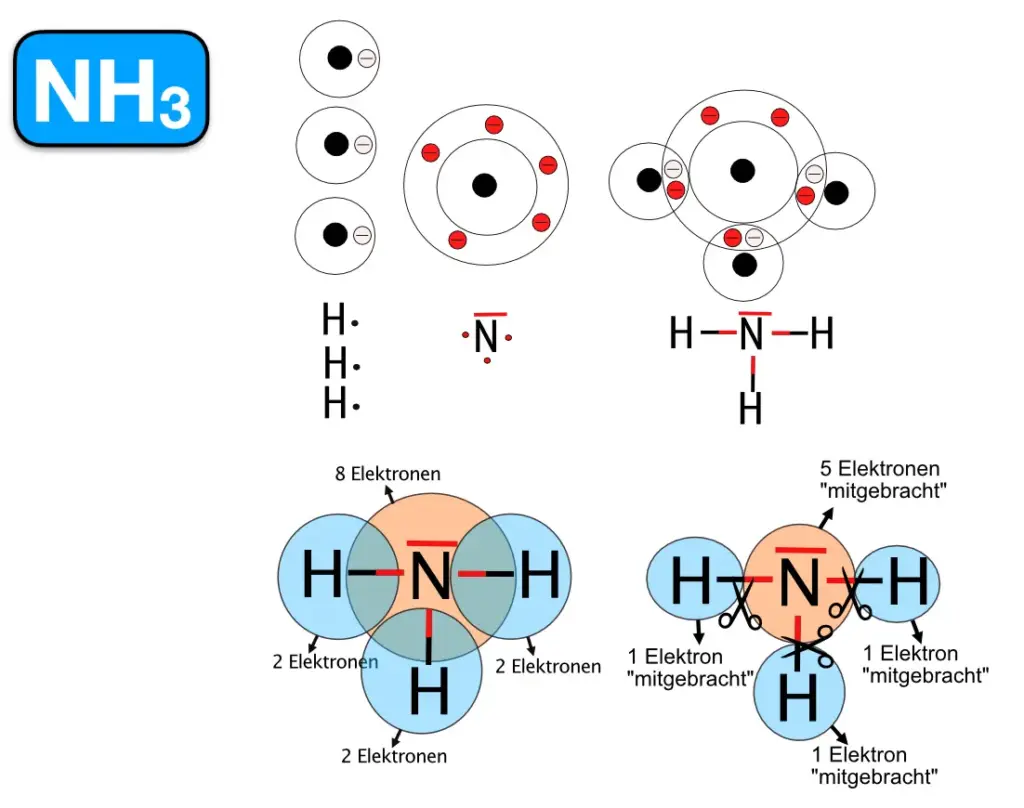
Ammoniak hat einen stechenden Geruch und ist für die Schleimhäute schädlich. Der Geruch ist auch von Salmiakgeist bekannt. 2
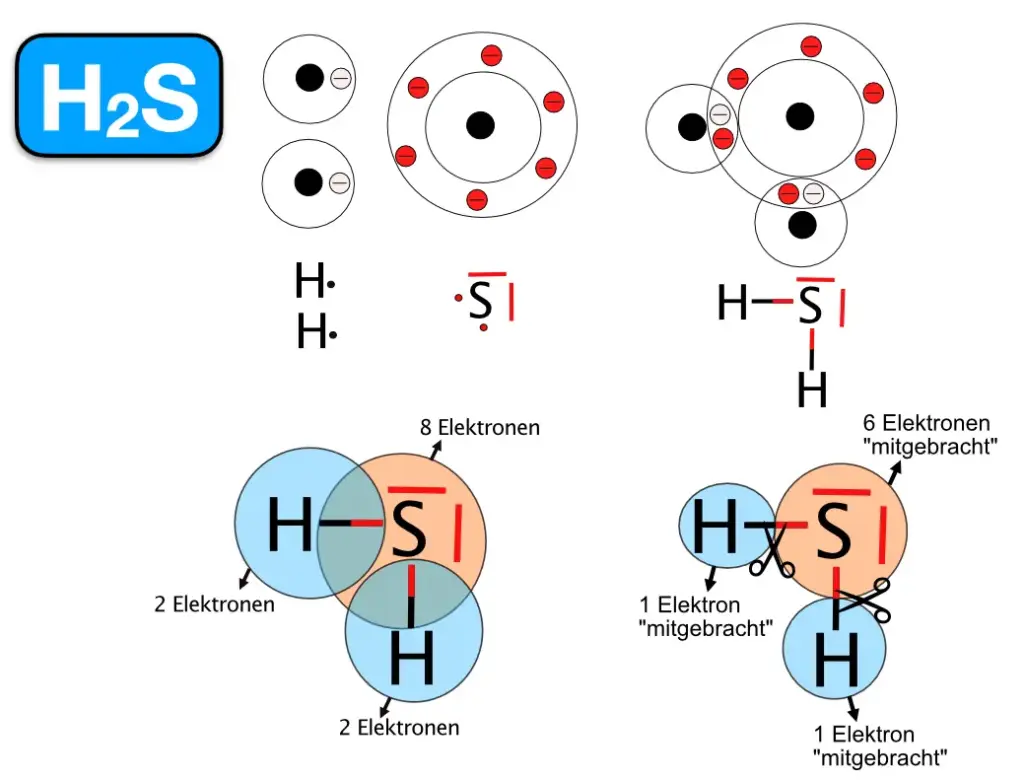
Das Schwefelwasserstoffmolekül ist für den Geruch nach faulen Eiern verantwortlich. H2S ist sehr giftig, unsere Nase aber auch sehr empfindlich für H2S. Schon kleinste, noch ungefährliche Konzentrationen riechen wir. Sehr, sehr kleine Konzentrationen riechen übrigens nach frisch gekochten Eiern. Erst etwas größere Konzentrationen riechen nach faulen Eiern. 2
Ein erneuter Blick ins Periodensystem
Weiteres
Elemente der gleichen Hauptgruppe bilden Verbindungen mit analogem Atomzahlenverhältnis. Dies ist für einige Beispiele in der Darstellung des PSE verdeutlicht. „Kennt man die Lewisformel von H2O, kenn man auch die von H2Se.“ Erkläre diese Aussage.
Eine Beschriftung.4
Mal was Kniffligeres...Aufgabenstellung
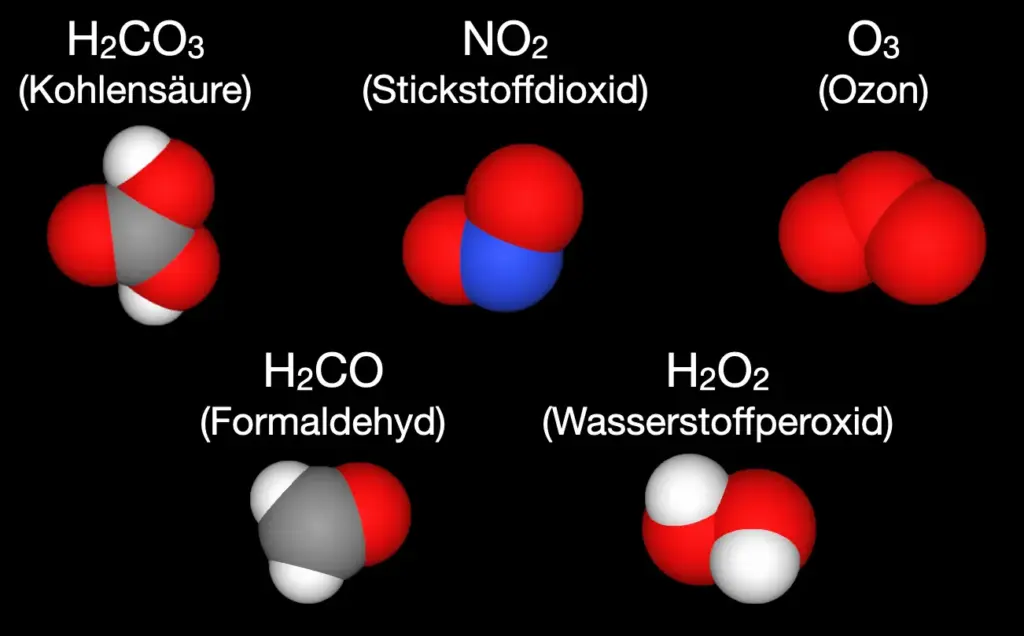
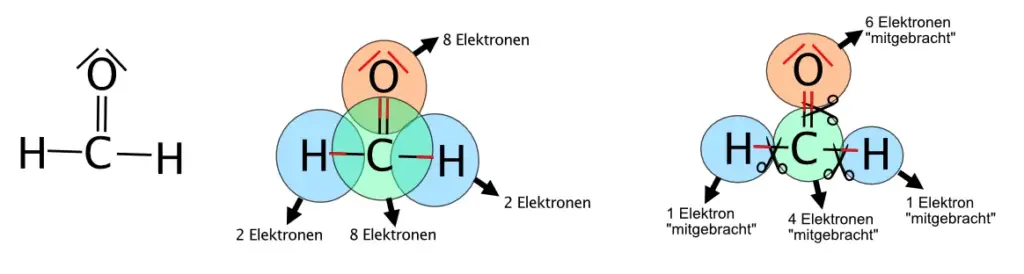
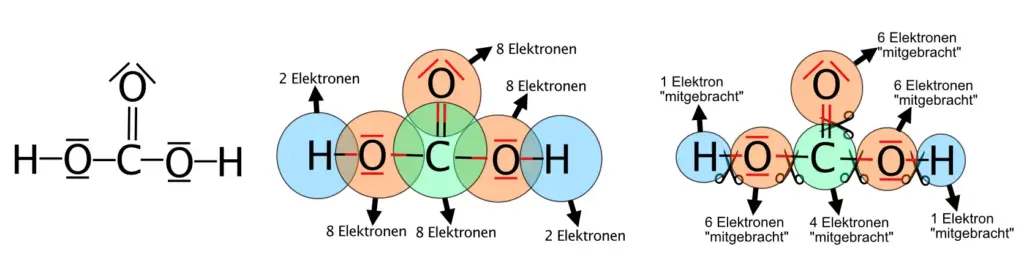
- Zeichne mit Hilfe der Molekülmodelle in Abb. 9 die Lewisformeln für H2O2, H2CO und H2CO3.
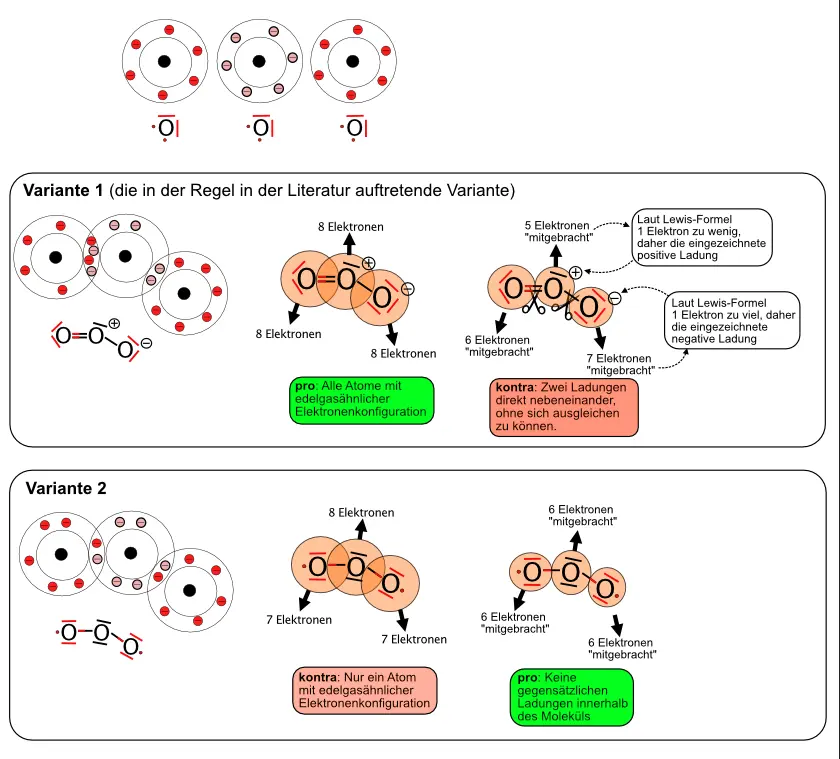
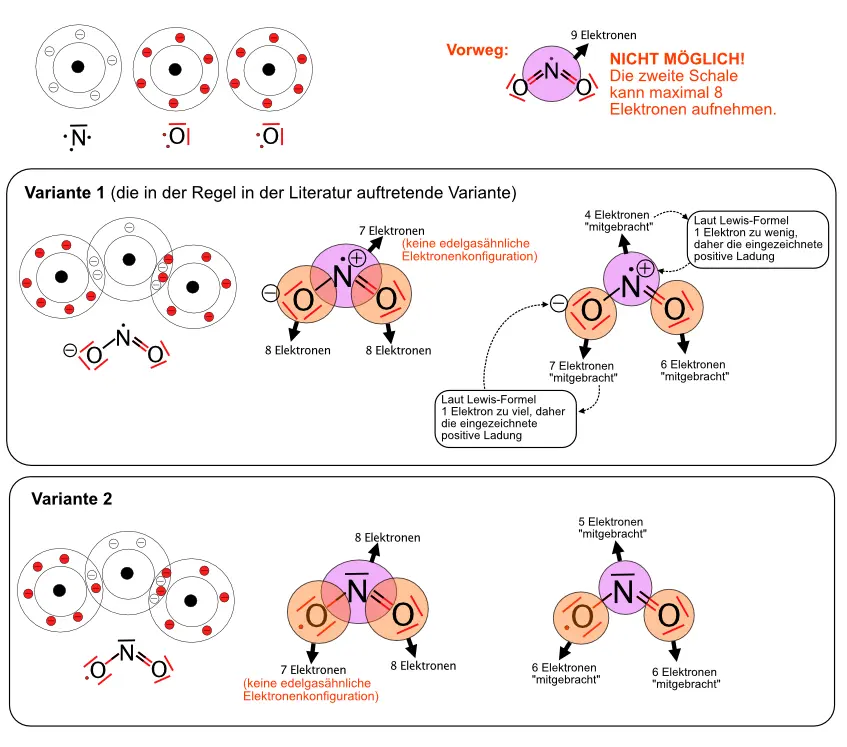
- In Abb. 9 sind noch zwei Molekülmodelle zu sehen, für die sich keine „perfekte“ Lewis-Formel finden lässt: O3 und NO2. Die Moleküle sind sehr reaktiv. Versuche, möglichst stimmige Lewis-Formeln zu entwickeln.
- In Abb. 10 sind vier falsche Lewis-Formeln für das CO2-Molekül dargestellt. Erkläre, was genau an den Lewis-Formeln falsch ist.
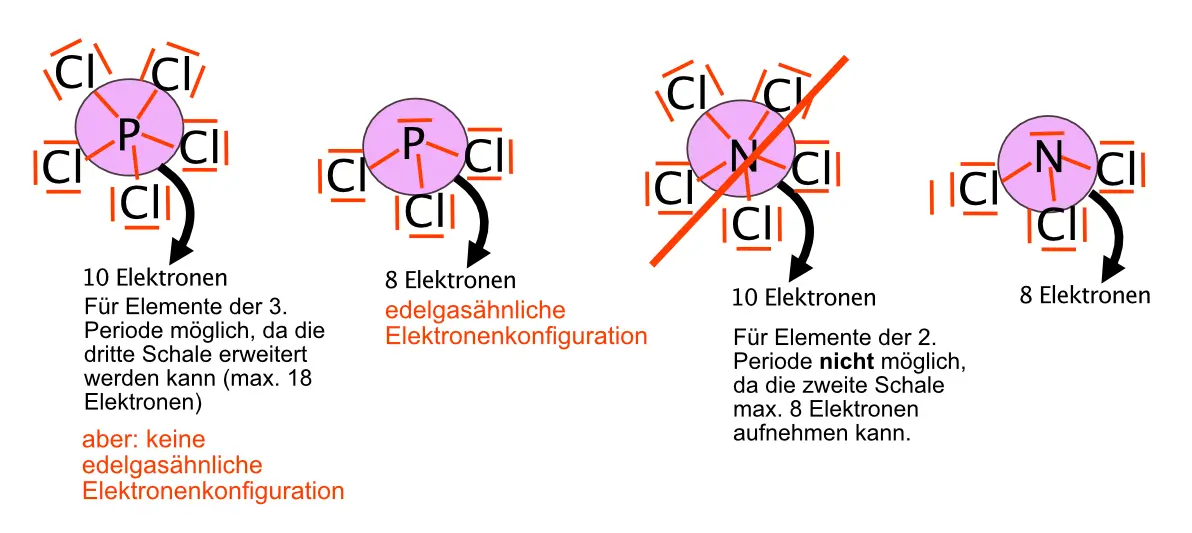
- Aus Phosphor und Chlor lassen sich PCl3 und PCl5 herstellen. Eine Verbindung mit der Verhältnisformel NCl5 existiert dagegen nicht, NCl3 lässt sich herstellen. Erkläre mit Hilfe der Lewis-Formeln.
- Zu PCl5 findet man in Chemiebüchern die Information: „Schon bei Normaltemperatur dissoziiert das Pentachlorid zum Phosphortrichlorid unter Abgabe von Chlor. Generell dient Phosphorpentachlorid daher als Chlorierungsmittel.“ Erkläre diese Eigenschaften von PCl5.
Musterlösungen zum Vergleichen
Kommt in einem Molekül die recht leicht zu spaltende O-O-Einfachbindung vor, wird das im Namen des jeweiligen Stoffes deutlich: Solche Stoffe werden Peroxide genannt. Sie sind alle recht reaktiv.
H2O2-Molekül.6
H2CO-Molekül. Formaldehyd ist für Menschen als krebserregend eingestuft.6
H2CO3-Molekül. Kohlensäure-Moleküle entstehen, wenn CO2 in Wasser geleitet wird (z. B. im Sodastreamer).6
O3-Moleküle sind sehr reaktiv. Die gebräuchliche Lewisformel ist die als Variante 1 dargestellte.6
Das NO2-Molekül ist sehr reaktiv. Es gehört zu den Stickoxiden, die gesundheitsschädlich sind und u.a. im Automotor entstehen und durch den Abgaskatalysator in möglichst großem Umfang beseitigt werden sollen.6
Moleküle zerbrechen und bilden sich neu
Weiteres
Elektronenpaarbindungen können prinzipiell auch wieder brechen. Es bedarf dazu aber Energie. Auf diese Weise können die von uns betrachteten Moleküle, die nur aus einer Atomsorte bestehen, „zerbrechen“ und es können auch Moleküle mit Atomen mehrerer Elemente bilden. Für das Leben, wie wir es kennen, unerlässlich!
Das Aufbrechen und Neubilden von Molekülen passiert permanent. In Pflanzen entstehen z. B. aus Kohlenstoffdioxid und Wasser und Energie aus der Sonne Glucose und Sauerstoff. Im Körper wiederum entstehen wieder Kohlenstoffdioxid und Wasser und wir nutzen die freigesetzte Energie.
Weiteres
Hier mal ein simples Beispiel: die sogenannte Knallgasprobe. Wasserstoff und Sauerstoff reagieren miteinander. Die Moleküle der Elemente zerbrechen dabei und es bilden sich neue Moleküle mit stabileren Elektronenpaaren: Wassermoleküle.
Knallgasprobe7