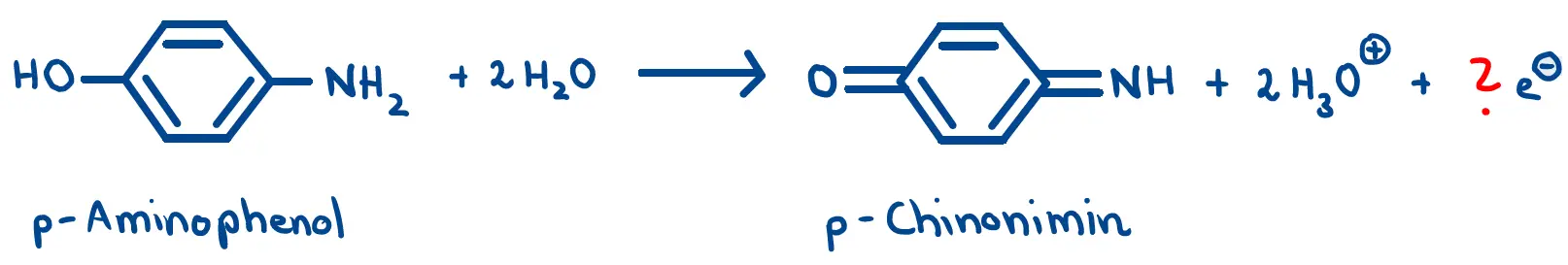Hintergrund
Weiteres
Medikamente enthalten Wirkstoffe, die den arzneilich wirksamen Bestandteil darstellen. Eine Tablette Paracetamol enthält beispielsweise neben diversen Hilfsstoffen den gleichnamigen Wirkstoff Paracetamol (auch Acetaminophen oder N-(4-Hydroxyphenyl)acetamid genannt), das bekannterweise schmerzstillend und fiebersenkend wirkt, indem es das Enzym im Körper hemmt, welches für die Produktion von Prostaglandinen zuständig ist. Diese Gewebshormone spielen bei Entzündungsprozessen, Fieber und der Schmerzvermittlung eine Rolle.
Um sicher zu sein, welche Menge eines Wirkstoffes in einer Dosis enthalten ist, ob dieser über eine ausreichende Reinheit verfügt, oder im Produktionsprozess keine Fehler unterlaufen sind, gibt es analytische Verfahren, die sich neben der Identität auch mit dem Gehalt und der Reinheit eines Arzneimittels beschäftigen. Im Falle von Paracetamol wird im Europäischen Arzneibuch eine valide Methode beschrieben, die Cerimetrie.
Die Cerimetrie stellt eine Redoxtitration dar, in der Cer(IV)-Ionen als Oxidationsmittel zum Einsatz kommen. Das Elementsymbol des Seltenerdenmetalls Cer ist Ce:
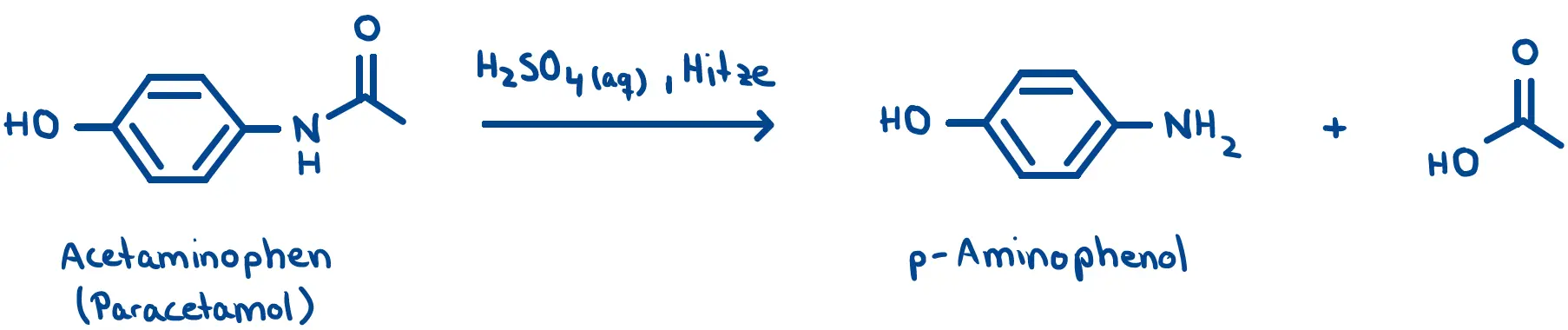
Der Gehalt des Wirkstoffes in einer Paracetamol-Tablette kann nicht direkt bestimmt werden, wohl aber das Spaltprodukt p-Aminophenol. Hierzu wird eine zermahlene Tablette in verdünnter Schwefelsäure erhitzt. Als Nebenprodukt entsteht Essigsäure:
Reaktion von Acetaminophen zu p-Aminophenol.1
Das p-Aminophenol lässt sich durch Cer(IV)-Ionen oxidieren zu p-Chinonimin:
Reaktion p-Aminophenol zu p-Chinonimin.1
Das Ende der Redoxtitration wird im Falle von Paracetamol durch die Zugabe geringer Mengen Ferroin, einem Redoxindikator, ermittelt. Während der Titration wird er selbst durch die Cer(IV)-Ionen oxidiert und ändert so seine Farbe von Rot nach Blau. Da er nur in geringen Mengen zugeführt wird, kann sein Einfluss auf die benötigte Menge an Maßlösung (hier Ammoniumcer(IV)sulfat) vernachlässigt werden.
Weiteres
Illustration Paracetamol Tabletten.2
Wusstest Du, dass Paracetamol seit 1977 auf der Liste der unentbehrlichen Arzneimitteln der WHO steht?
Aufgaben
- Werten Sie den Versuch in M2 aus, indem Sie …
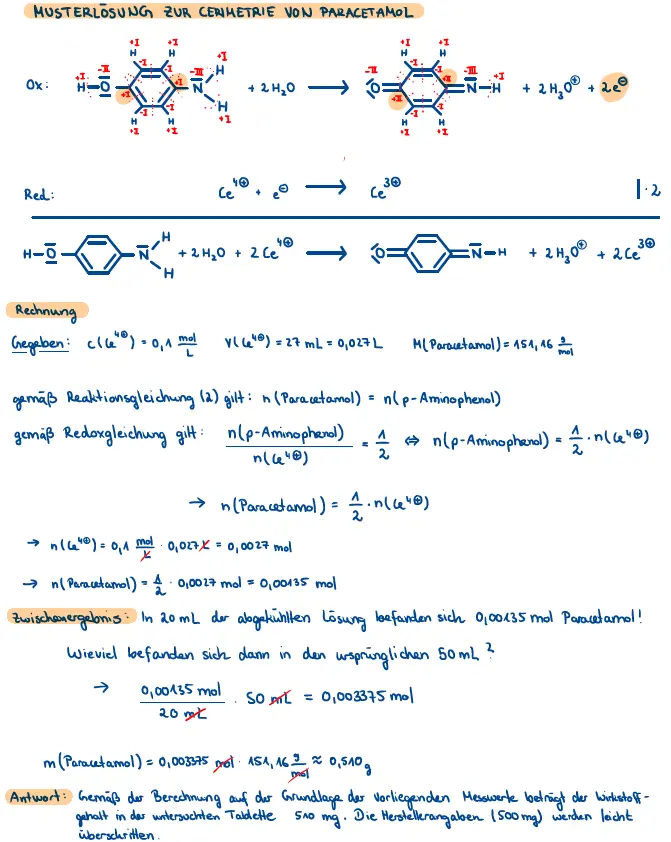
- das zugrundeliegende Redoxschema zur Redoxreaktion inkl. aller Teilgleichungen notieren. Nutzen Sie hierzu auch die Anregungen.
- die Masse an Wirkstoff in mg in einer Tablette Paracetamol aus den Messergebnissen berechnen und ihr Ergebnis mit den Herstellerangaben vergleichen (vgl. Abb. 1).
Anregungen & Lösungen
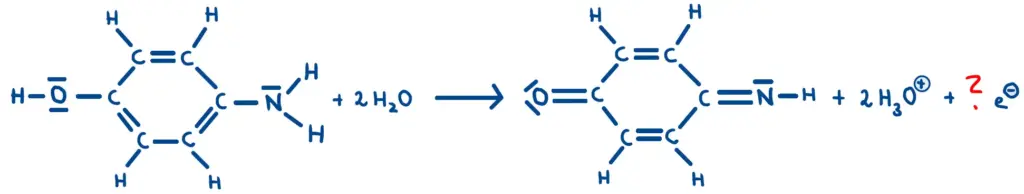
Für ihr Redoxschema benötigen Sie die Reaktionsgleichung 1 und die Reaktionsgleichung in Abb. 2. In dieser fehlt eine Angabe zur Anzahl der gebildeten Elektronen. Diese müssen Sie unter Verwendung von Oxidationszahlen selbst ermitteln. Dies gelingt Ihnen am einfachsten, wenn Sie die relevanten Moleküle, die in einer Mischung aus Skelett- und Halbstrukturformel dargestellt sind, zunächst in eine Valenzstrichformel mit allen Bindungen und freien Elektronenpaaren skizzieren. Die Reaktionsgleichung in Abb. 2 sieht dann wie folgt aus:
Durchführung & Messergebnisse
Weiteres
- Eine Tablette Paracetamol wurde in einem Mörser zerrieben und das Pulver in 50 mL konzentrierte Schwefelsäure (H2SO4) unter Erwärmen aufgelöst, bis die Lösung leicht siedet.
- 20 mL der abgekühlten Lösung wurden mit dest. Wasser auf 100 mL Gesamtvolumen aufgefüllt.
- Die Lösung wurde mit 2 mL konzentrierte Schwefelsäure angesäuert und mit einigen Tropfen Ferroin versetzt.
- Die Titration erfolgte mit 0,1 molarer Ammoniumcer(IV)sulfat-Lösung bis zu einem Farbumschlag nach Blau.
- Hierbei wurden 27 mL Ammoniumcer(IV)sulfat-Lösung verbraucht.
Weitere Angaben
- Ammoniumcer(IV)sulfat: (NH4)4Ce(SO4)4
- Ein gelöstes Teilchen liefert ein Cer(IV)-Ion
- M(Paracetamol) = 151,16 g/mol