Material
Weiteres
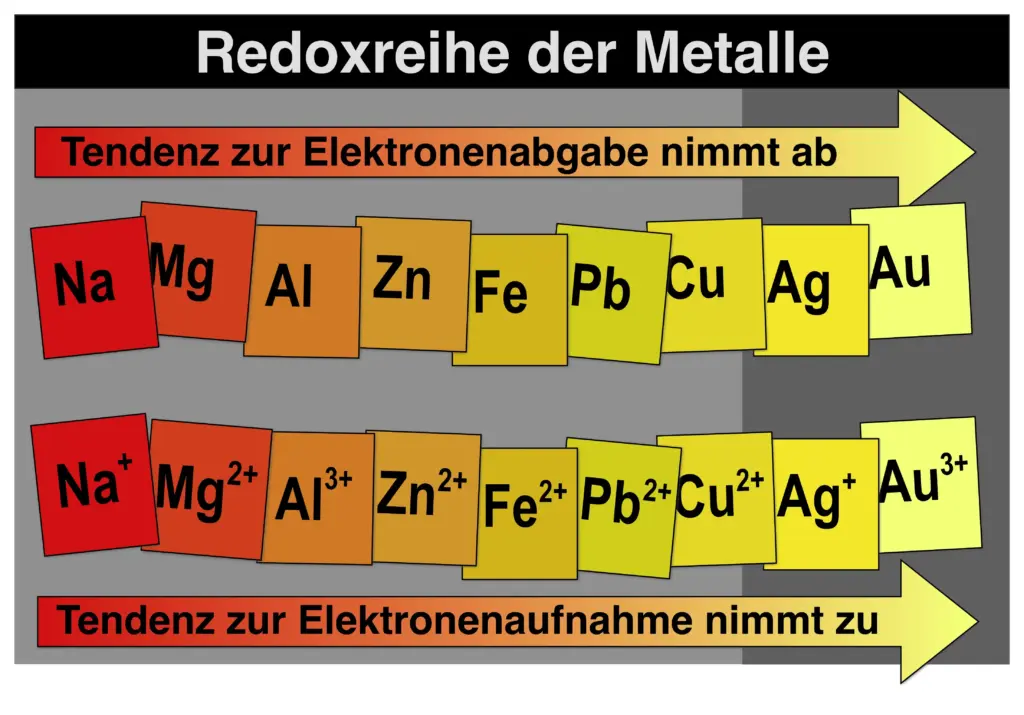
Erinnerst du dich an die Redoxreihe der Metalle? Was wird damit dargestellt bzw. welche Informationen lassen sich dieser entnehmen?
Die Redoxreihe der Metalle.1
Weiteres
Im Röderstollen – heute UN Weltkulturerbe – in der Nähe von Goslar wurden vor über 200 Jahren Kupfersalze unter Tage abgebaut, aus denen man dann reines Kupfer herstellte.
Im Laufe der Zeit hat man das eine oder andere im Stollen liegen gelassen, z.B. eine Eisenleiter, die dort aber nicht einfach nur verrostet ist…

Röderstollen. Heute UN Weltkulturerbe.2
Farbe von Kupfer & Kupferverbindungen
Kupfercarbonat, Kupferchlorid, Kupfersulfat und Kupfer.3
Aufgaben
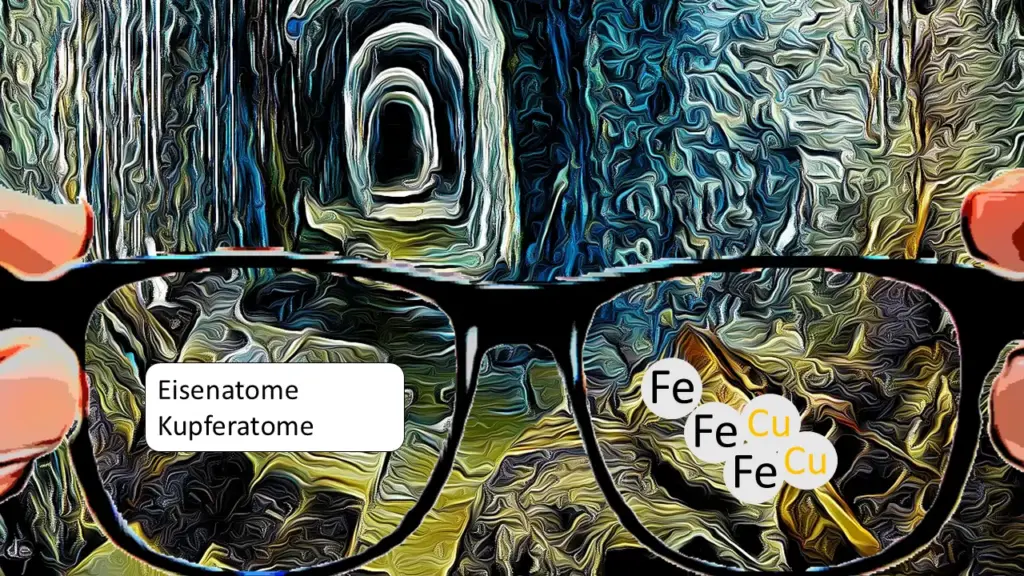
- Beschreiben Sie, was auf dem Foto in Abb. 2 zu sehen ist. Stellen Sie mit Hilfe von Galerie 1 Vermutungen auf, welche Stoffe in Abb. 2 abgebildet sind.
- Benennen Sie explizit das Besondere an der Leiter in der Aufnahme in Abb. 2. Erklären Sie basierend auf ihrem Vorwissen aus der Sekundarstufe 1, wie diese Besonderheit wahrscheinlich zustande kam. Nutzen Sie die Anregungen auf Teilchenebene in M2.
- Planen Sie einen einfachen Versuch, der ihre Vermutung bezüglich der Abläufe in der Kupfermine stützen oder widerlegen kann. Benennen Sie auch benötigte Chemikalien.
- Führen Sie den Versuch nach einer grundlegenden Besprechung durch, protokollieren Sie ihre Beobachtungen, machen Sie ein Foto und werten Sie den Versuch aus.
Auswertungshilfe zu Aufgabe 4
- Du kannst dir hier eine Animation zu den Abläufen auf Teilchenebene anschauen.
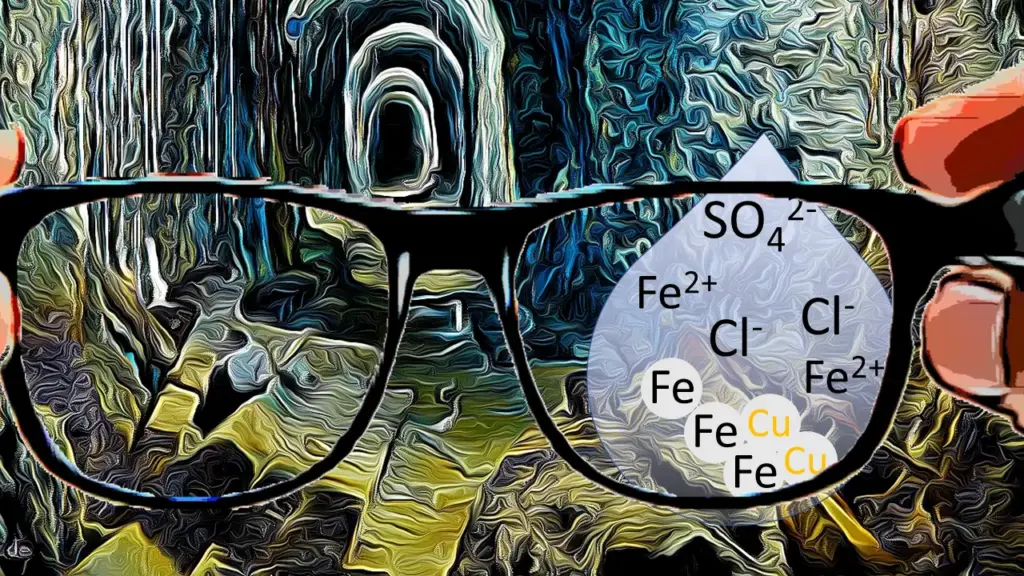
Ein Wechsel auf Teilchenebene
Was ist hier passiert? Betrachte einmal die folgende Präsentation.
Weiteres
Die Kupfermine auf Teilchenebene. 4
Kupfersulfat auf Eisen
Materialien
- Pipetten
- Schleifschwämme / Schmirgelpapier
Chemikalien
-
Eisen
- Blech oder Pulver
- Kupfersulfat-Lösung 0,1 mol/L
-
Rotes Blutlaugensalz
- Kaliumhexacyanoferrat(III)
Durchführung
- Das Eisenblech abschmirgeln und dadurch Rostflecken entfernen.
- Kupfersulfat-Lösung auf das Eisenblech tröpfeln.
- Nach einer Weile eine winzige Menge rotes Blutlaugensalz auf einen Tropfen Kupfersulfat-Lösung auf dem Eisenblech geben.
Aufbau.4
Entsorgen und Aufräumen
-
Reste mit einer Pipette aufnehmen und im Sammelbehälter für Schwermetallsalze geben.
-
Alle verunreinigten Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
Was wäre wenn?
Stell dir vor, man hätte neben der Eisen-Leiter ein Blech aus Zink oder einen Ring aus Silber in der Kupfermine liegen gelassen.
Ich glaube, das wäre dasselbe passiert wie mit der Eisen-Leiter!
Weiteres


Zinkgießkanne | Silbermünzen und -ring im Kupferbergwerk5
Weitergedacht
- Stellen Sie eine begründete Vermutung auf, was mit dem Zink-Blech oder dem Silber-Ring im Laufe der Zeit passiert wäre.
- Benennen Sie die Chemikalien, mit deren Hilfe Sie ihre Vermutung aus A1 stützen oder widerlegen können.
- Führen Sie den erweiterten Versuch 2 durch und werten Sie diesen aus!
Überprüfung diverser Redoxreaktionen
Materialien
- Pipetten
- Schleifschwämme / Schmirgelpapier
- Papiertuch
Chemikalien
- Eisen-Blech
- Zink-Blech
- Silber-Blech
- Kupfer-Blech
-
Magnesium-Blech
- oder Band
- Kupfersulfat-Lösung 0,1 mol/L
- Zinksulfat-Lösung 0,1 mol/L
-
Eisen(II)sulfat-Lösung 0,1 mol/L
- Frisch ansetzen!
-
Magnesiumsulfat-Lösung 0,1 mol/L
- Frisch ansetzen!
- Silbernitrat-Lösung 0,1 mol/L
Durchführung
- Alle Bleche abschmirgeln und so von Verunreinigungen befreien.
- Bleche auf einem Papiertuch legen und darauf einen Tropfen der verschiedenen Metallsalz-Lösungen tropfen.
- Die Beobachtungen tabellarisch festhalten (siehe unten).
Aufbau.4
Beobachtung
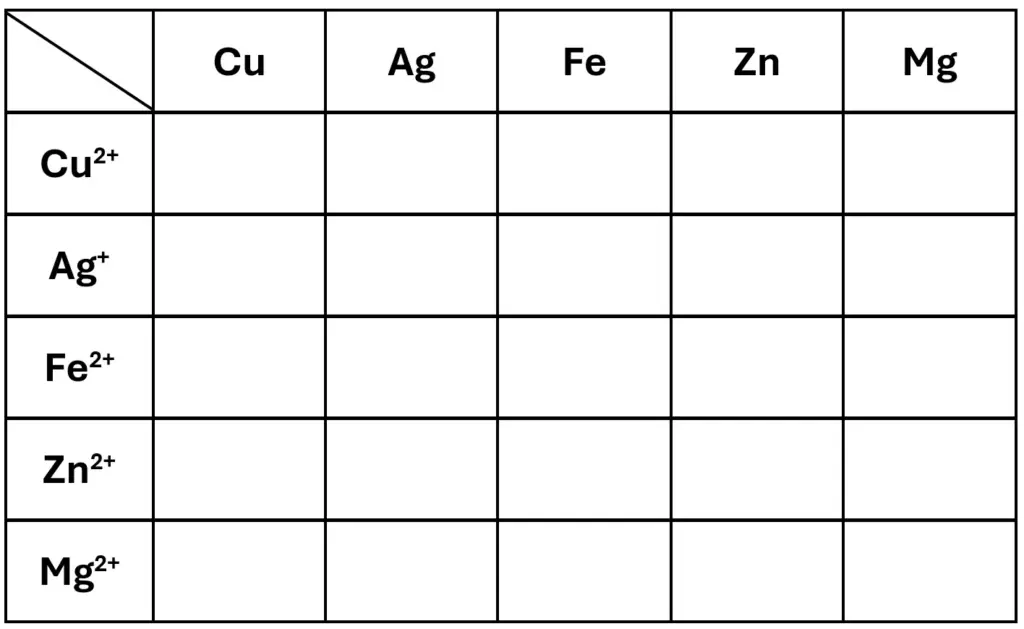

Oben Rechts: Zink, recht daneben: Eisen. Unten links: Kupfer, rechts daneben Silber.4
Entsorgen und Aufräumen
-
Reste der Metallsalzlösungen mit einer Pipette aufnehmen und im Sammelbehälter für Schwermetallsalze geben.
-
Alle verunreinigten Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.