Grundlegendes
Weiteres
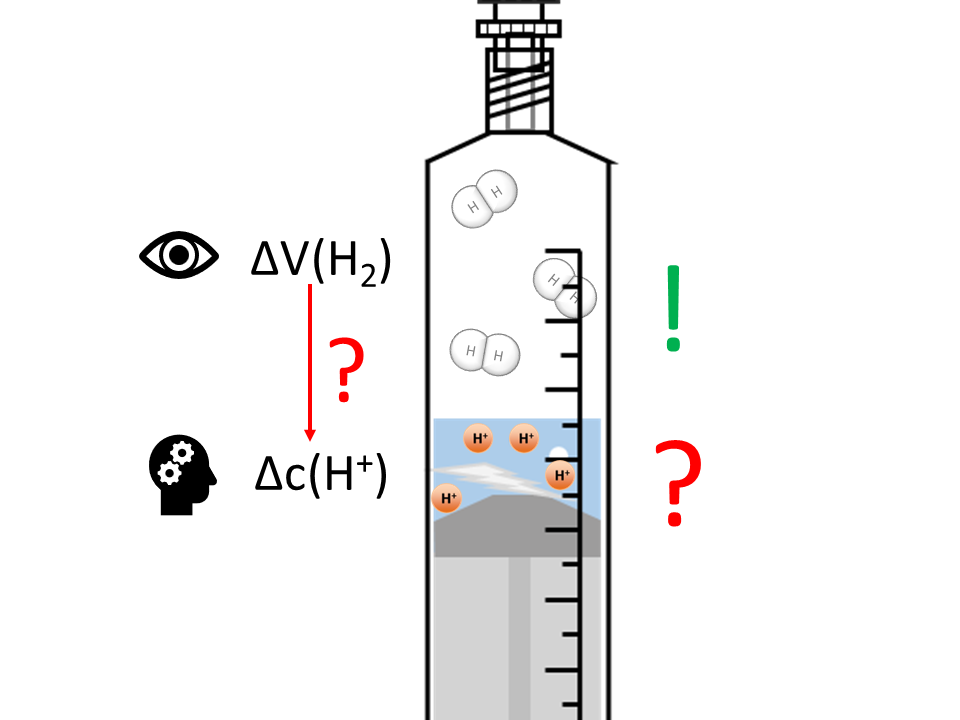
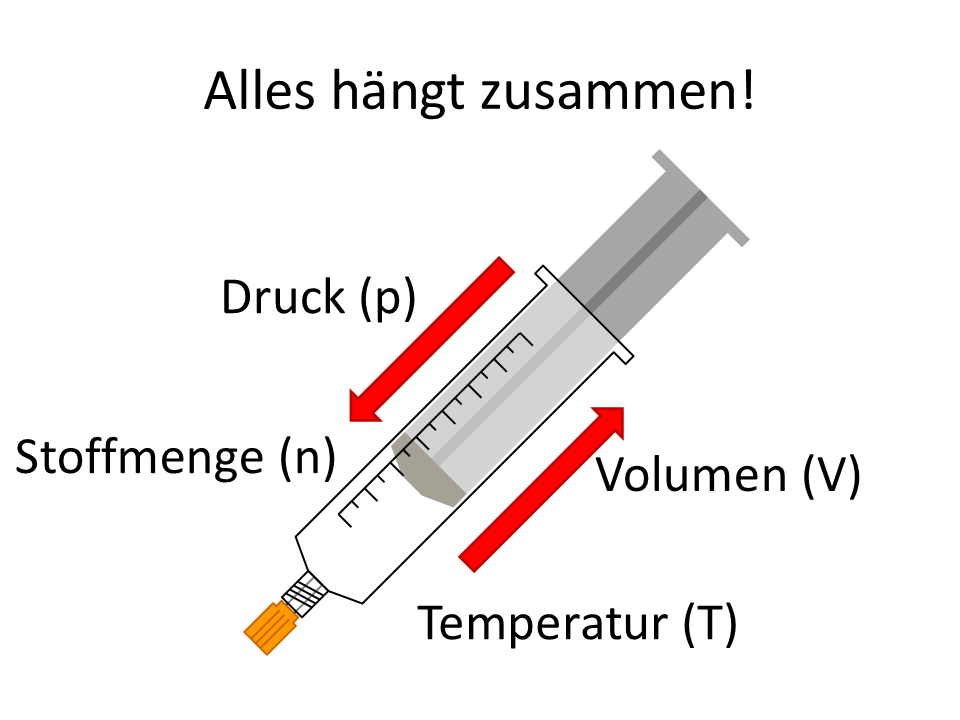
Oft interessieren uns in der Chemie auch die Reaktionsgeschwindigkeiten der Stoffe, deren Konzentrationsänderung wir nicht direkt beobachten können.
Beispielweise könnten wir die Volumenzunahme an Wasserstoff beobachten, uns aber für die Konzentrationsänderung der Wasserstoff-Ionen / Protonen (H+)1 interessieren:
Hier wird zunächst einmal erklärt, wie man z.B. aus dem Volumen des entstandenen Wasserstoffs die Konzentration der verbliebenen Protonen in der Lösung berechnet und dann in M2 wie man daraus die Konzentrationsänderungen der Magnesium-Ionen ermittelt.
Volumen -> Konzentration
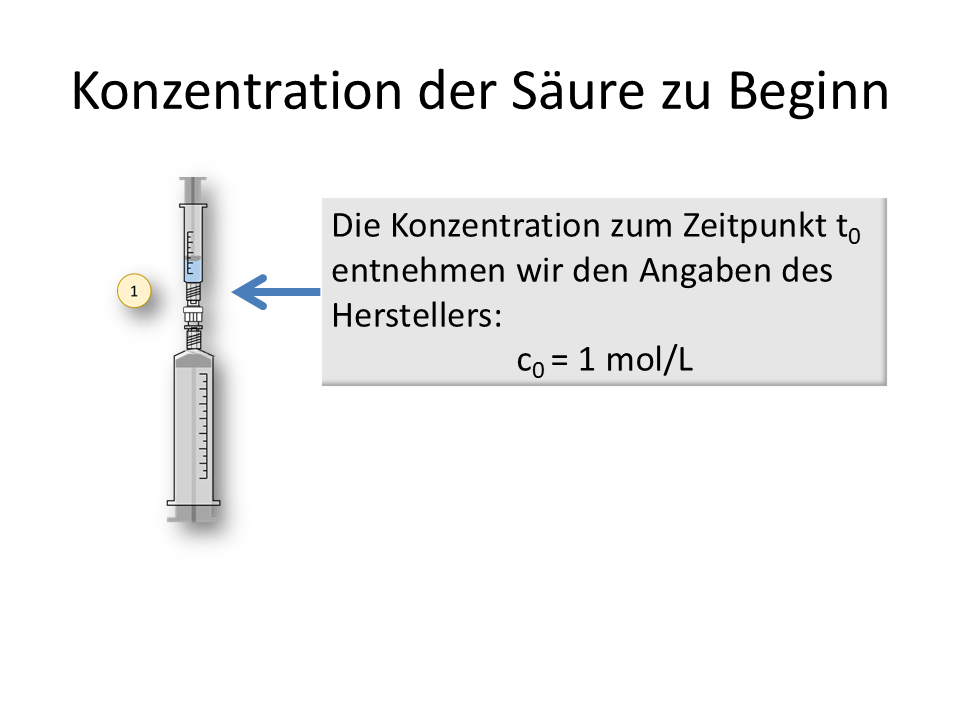
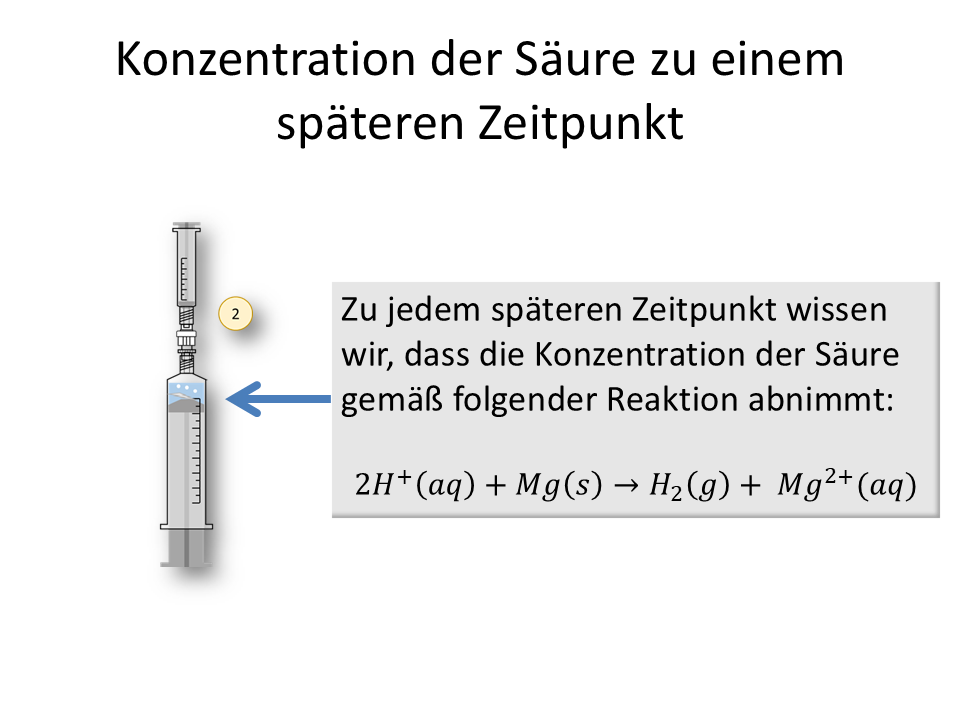
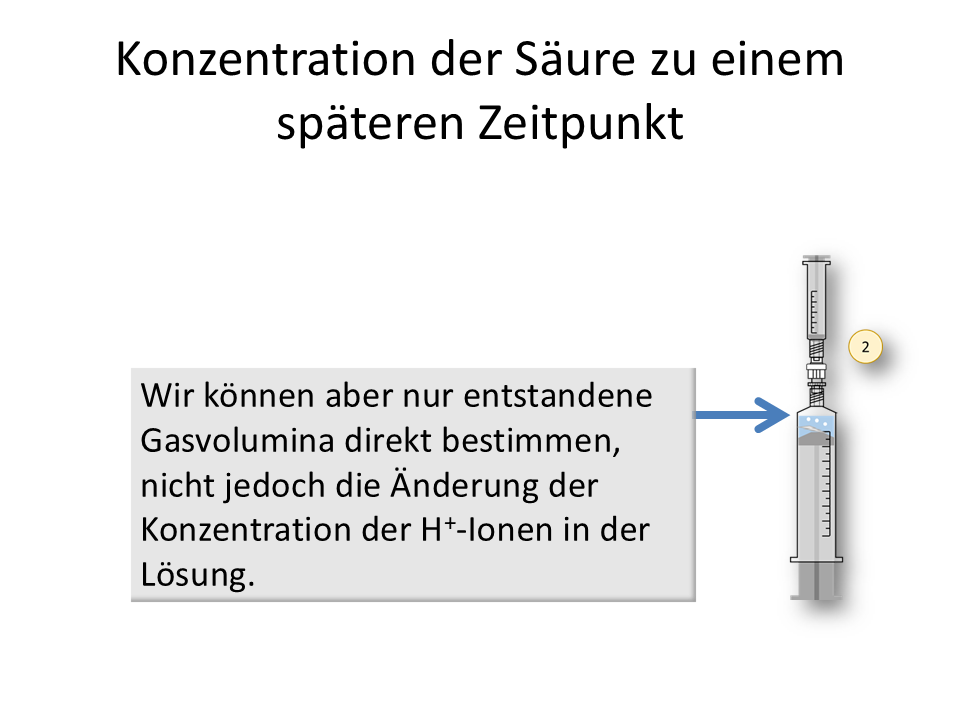
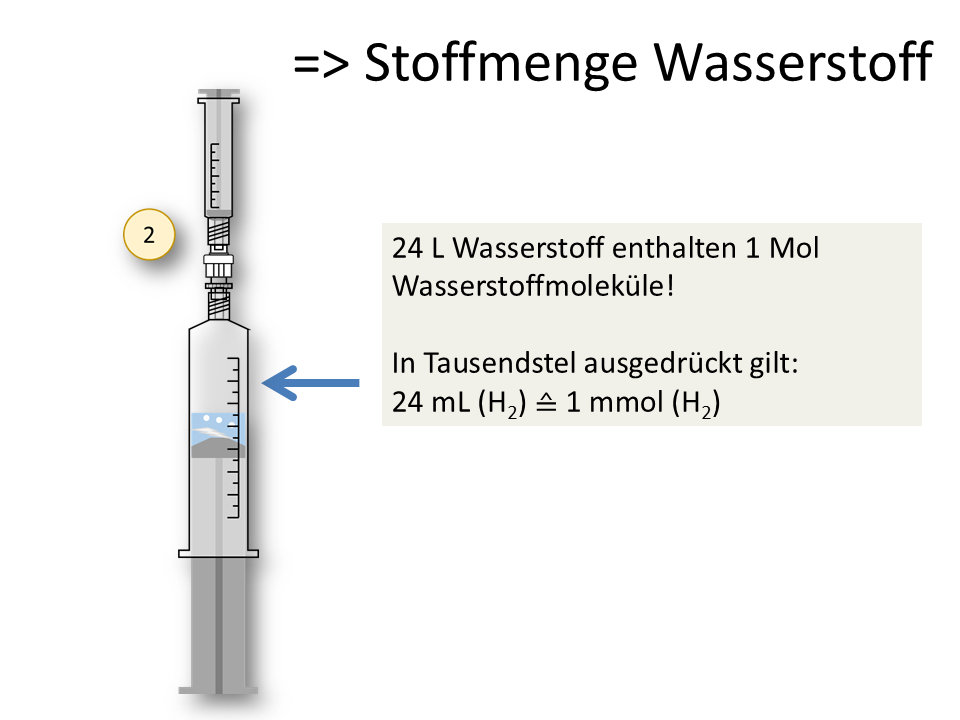
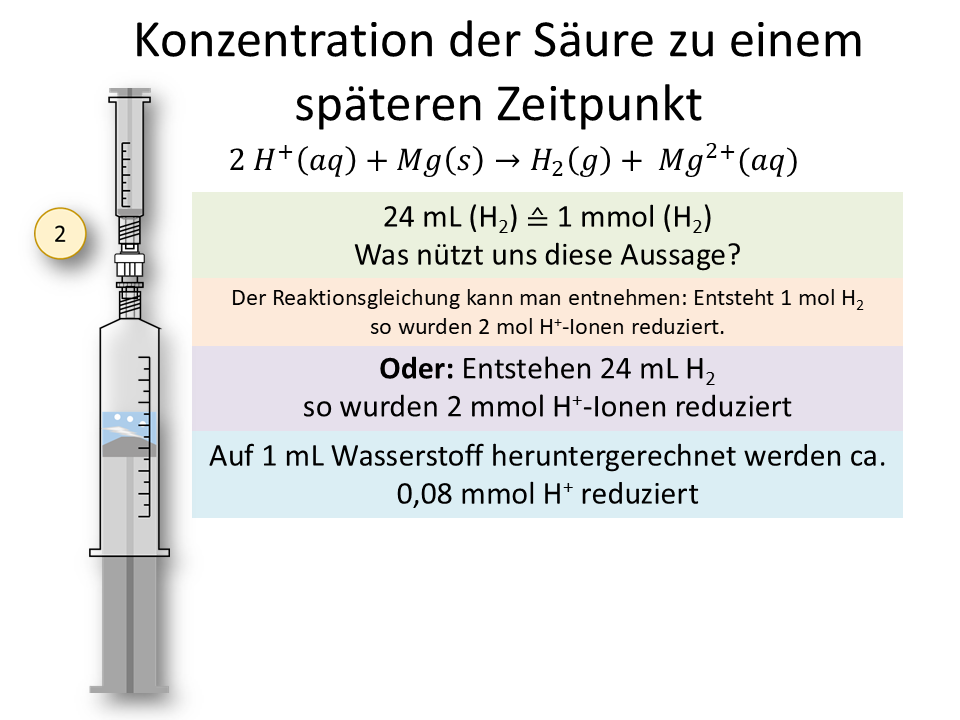
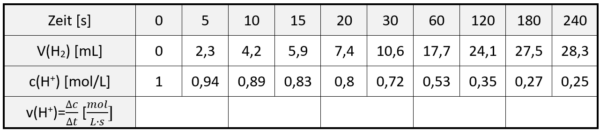
Wie man aus dem entstehende Volumen an Wasserstoffgas die verbliebene Konzentration der H+-Ionen in der Lösung berechnet, wollen wir hier einmal nachvollziehen.
Wie kommt man vom Volumen zur Konzentration?2
Weiteres
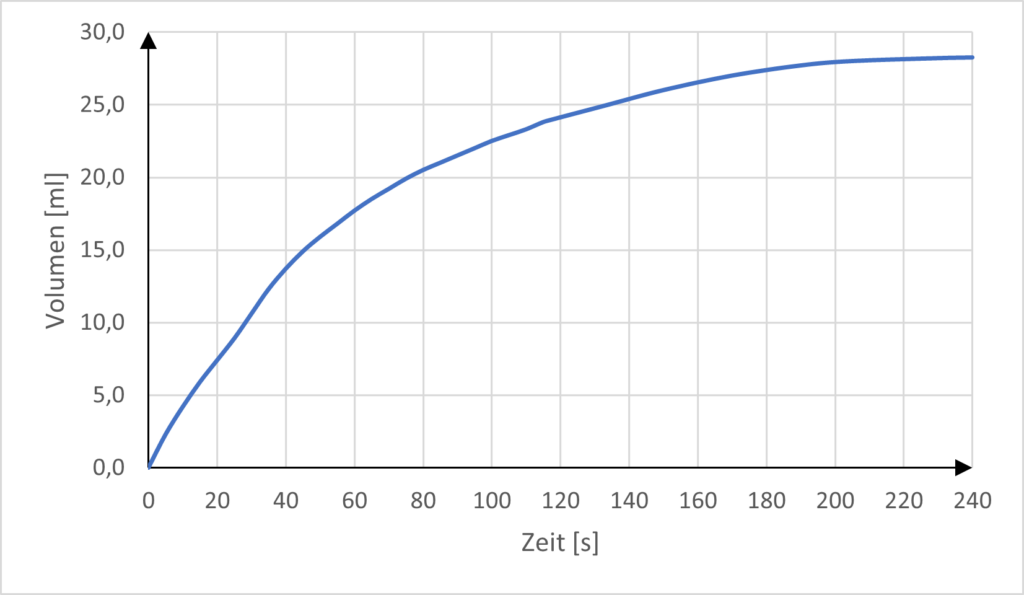
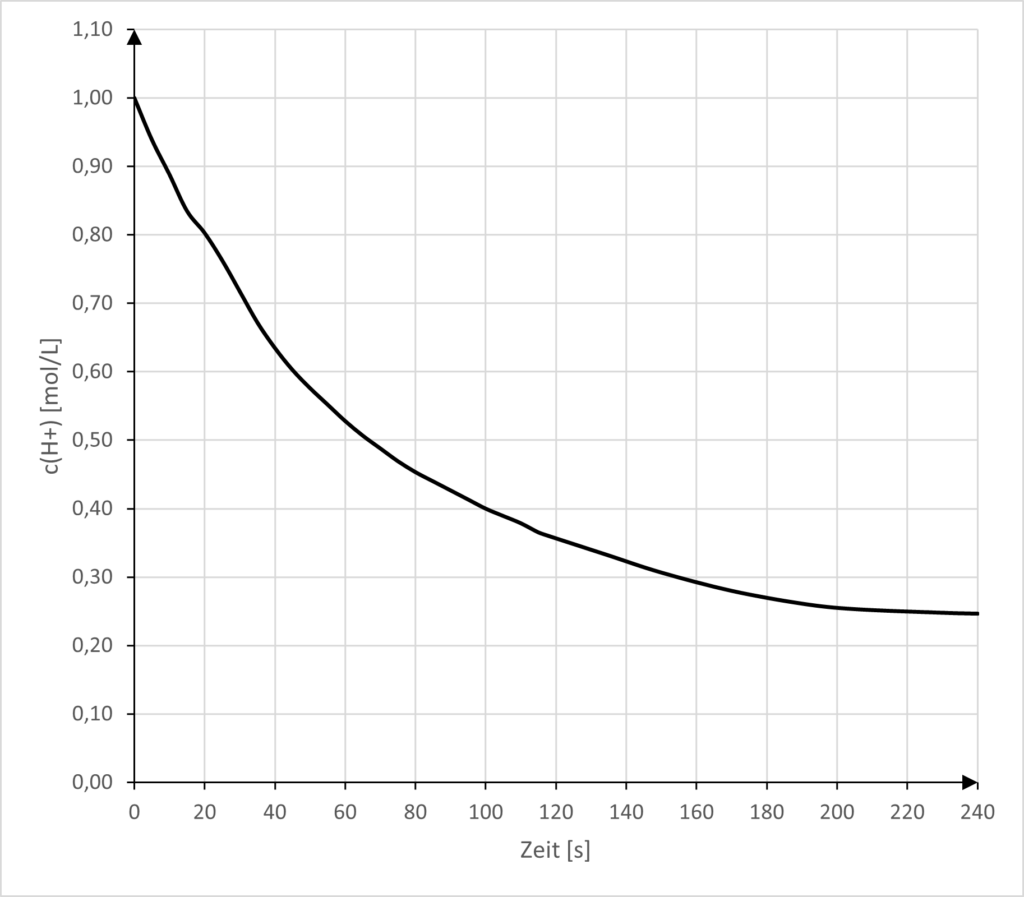
Darstellungen von Messwerten.3
Aufgaben
- Klären Sie anhand von Galerie 1, wie man prinzipiell aus dem gemessenen Volumen an Wasserstoff auf die verbliebene Konzentration an Wasserstoff-Ionen in der Lösung schließen kann.
- Wählen Sie aus Galerie 2 die Darstellung(en) aus, aus der/denen man die Reaktionsgeschwindigkeit des Verbrauchs an H+-Ionen ermitteln kann. Ermitteln Sie zeichnerisch oder mit Hilfe der Wertetabelle …
- … die Anfangsgeschwindigkeit für den Verbrauch der H+-Ionen.
- … die Reaktionsgeschwindigkeit des Verbrauchs an H+-Ionen zu zwei weiteren verschiedenen Zeitpunkten oder Zeiträumen.
- Erklären Sie die Aussage: Die Geschwindigkeit ist eigentlich negativ.
Die Konzentration der Magnesium-Ionen zu diversen Zeitpunkten ableiten
Bestandsaufnahme
Kennt man die verbrauchte Stoffmenge an Protonen, kann man mit Hilfe der Reaktionsgleichung daraus leicht die entstehende Stoffmenge und Konzentration der Magnesium-Ionen ableiten.
Weiteres
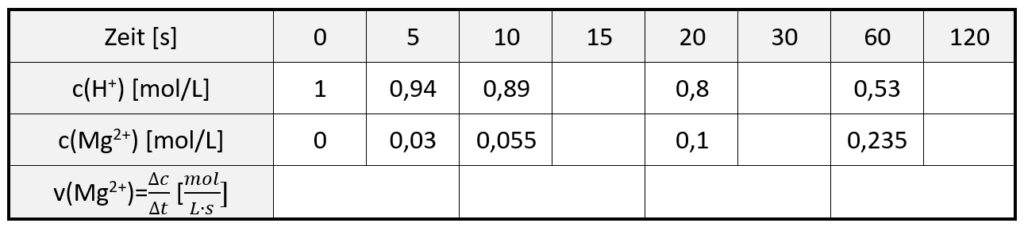
Wertetabelle zur Bildung von Magnesium-Ionen.2
Lösungsansatz
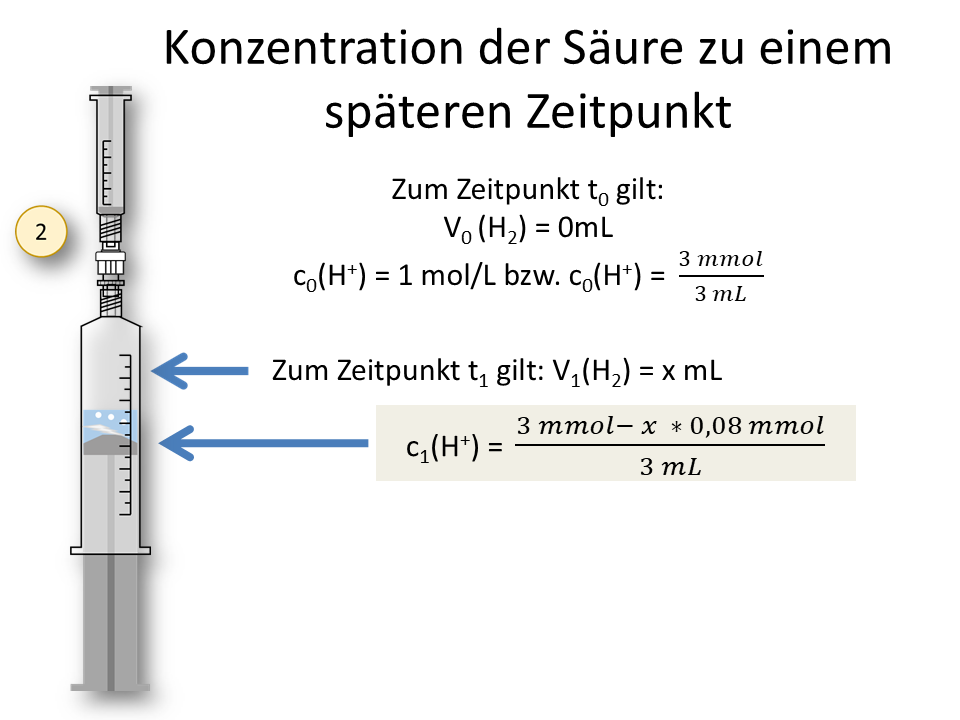
Es gilt aus bekannten Größen die Konzentration der Magnesium-Ionen zu bestimmen. Zu Beginn ist die Konzentration von Magnesium-Ionen: c(Mg2+) = 0 mol/L. Am einfachsten kann man die Konzentration mit Hilfe der Reaktionsgleichung aus der Konzentration der H+-Ionen berechnen: Bei der Reduktion von 2 mol H+-Ionen entstehen zeitgleich immer 1 mol Mg2+-Ionen. Daraus lässt sich ein Verhältnis aufstellen:
Die Konzentration der Protonen, die bis zum Zeitpunkt t zu Wasserstoffgas reduziert wurde, lässt sich leicht herleiten: Von der Anfangskonzentration c0 muss die Konzentration der Protonen abgezogen werden, die zum Zeitpunkt t noch vorliegt:
Aufgaben
- Vollziehen Sie nach, wie man aus den Messwerten und der Reaktionsgleichung in M2 auf die nicht gemessene Konzentration der Magnesium-Ionen schließen kann.
- Ergänzen Sie in der Wertetabelle die fehlenden Werte der Geschwindigkeit bei der Bildung von Magnesium-Ionen (Mg2+) in mindestens zwei verschiedenen Zeitintervallen.
Übung
Weiteres
Die Geschwindigkeit der Reaktion von Salzsäure mit Methanol wurde gemessen:
Weiteres
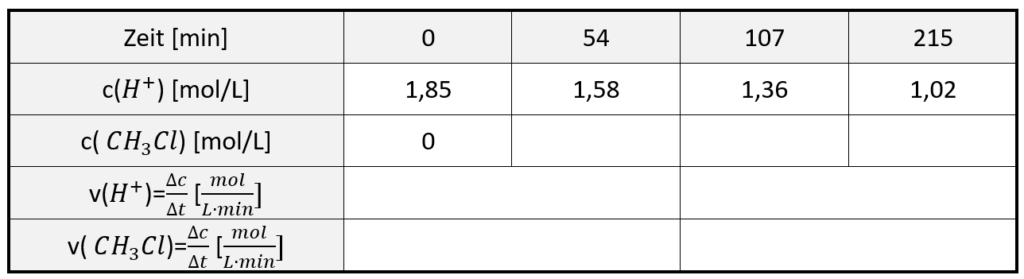
Wertetabelle zur Reaktion.2
Aufgaben
- Berechnen Sie aus den Angaben in M3 die Geschwindigkeiten des Verbrauchs an H+-Ionen und der Bildung von Chlormethan (CH3Cl ) in den beiden angegebenen Zeitintervallen.