Versuchsbeobachtungen und selbsterhitzende Lebensmittel und Kühlkissen
Weiteres
Sammlung von Hotpots (selbsterhitzender Kaffee und Instant-Ramen) und Kältekissen.1
Weiteres
Messdaten zum Experiment Temperaturänderungen beim Lösen von Salzen.2
Aufgaben
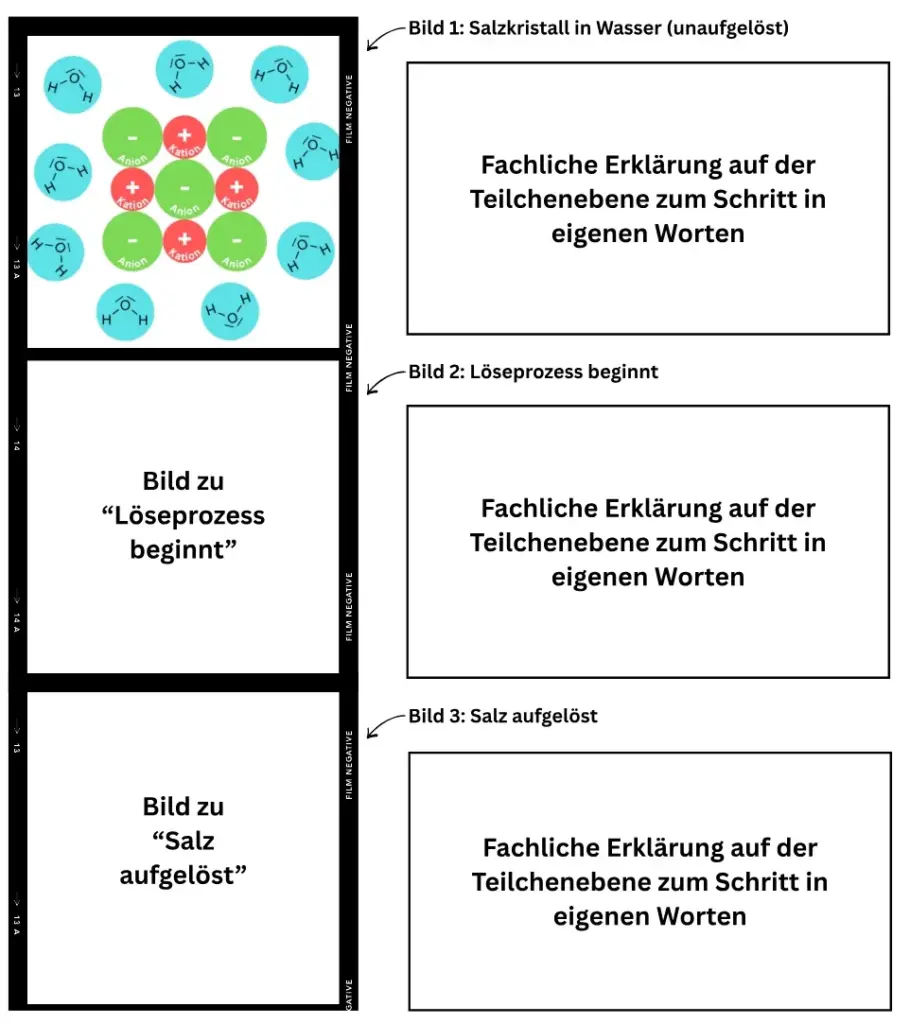
- Stelle den allgemeinen Lösevorgang eines Salzes (Kationen/Anionen) auf der Teilchenebene in Form einer Filmleiste dar.
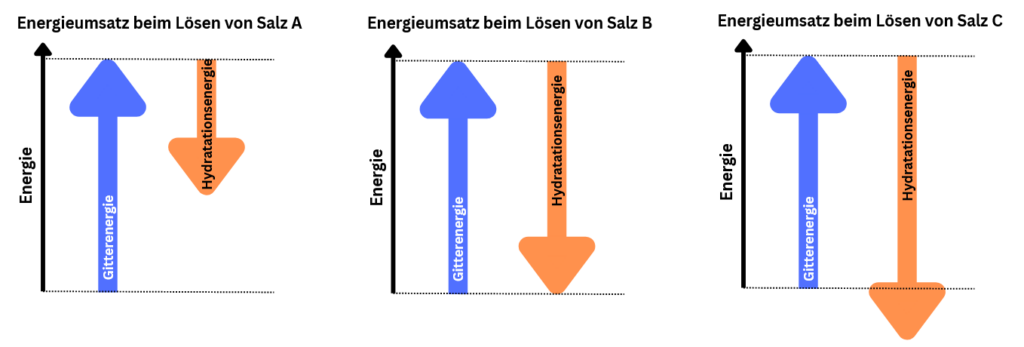
- Mache dich mit den neuen Begriffen „Gitterenergie“ und Hydratationsenergie“ und den verschiedenen Energiediagrammen in M3 vertraut.
- Ergänze basierend darauf dein zweites Bild („Lösevorgang beginnt“) auf dem Whiteboard und in der Filmleiste. Stelle dort geeignet dar,
- wobei Energie aufgenommen wird und
- wobei Energie abgegeben wird.
- Ordne dem Lösevorgang im Hotpot eines der drei Energiediagramme (A–C) von M3 zu.
- Bereite dich darauf vor dein Ergebnis zu präsentieren und zu erläutern, warum sich der Löseprozess im Hotpot zu einer Erwärmung führt.
Hilfekarten
Verwende diese Begriffe, um zu erklären, wie es beim Lösen von Salzen warm werden kann:
- Anion,
- Kation,
- Ionengitter,
- Dipol,
- Ionen-Dipol-Wechselwirkung,
- Hydrathülle,
- Gitterenergie (neuer Begriff),
- Hydratationsenergie (neuer Begriff).
Der Prozess des Lösevorgangs müsste dir bereits bekannt sein.
Wenn du dir dennoch unsicher bist, schaue nochmal in deine Unterlagen aus der Stunde Das Salz in der Suppe – Was passiert beim Lösen eines Kochsalzkristalls auf Teilchenebene?
Die Richtungen und die Länge beider Pfeile haben eine Bedeutung.
Welcher Pfeil zeigt nach oben?
→ Die Länge und Richtung dieses Pfeils steht für die Größe der Gitterenergie (Energieaufnahme).
Welcher Pfeil zeigt nach unten?
→ Die Länge und Richtung dieses Pfeils steht für die Größe der Hydratationsenergie (Energieabgabe).
Sprinter-Aufgabe
- Ordne dem Löseprozess in einem Kältekissen eines der drei Energiediagramme (A–C) aus M3 zu.
Begründe deine Entscheidung fachlich unter Verwendung der Begriffe Gitterenergie, Hydratationsenergie und Energieaufnahme/-abgabe. - Erkläre, wie die Beschriftung einer Filmleiste zur Beschreibung der Löseprozesse in einem Kältekissen lauten müsste.
Erstellung einer Filmleiste zum Lösevorgang
Vorlage für die allgemeine Darstellung des Löseprozesses
Vorlage für die Darstellung des Löseprozesses eines Salzes als Filmleiste.2
Vorgehensweise
- Modelliere den Ausgangzustand mit den Modellen der Anionen (-), Kationen (+) und Wasser-Moleküle (H2O) auf dem Whiteboard.
- Ergänze in deiner Darstellung die Teilladungen der Wassermoleküle. Fotografiere dein Ergebnis.
- Modelliere auf dieselbe Art und Weise die beiden weiteren Bilder. Fotografiere auch diese beiden Bilder.
- Erstelle mit deinen Fotos den linken Teil einer Filmleiste.
- Ergänze deine Fotos jeweils durch einen erklärenden Text, indem du die notwendigen Fachbegriffe verwendest. Halte dich kurz.
Energetische Betrachtung beim Lösen eines Salzes
Hydratationsenergie
Befinden sich Ionen in Wasser, werden sie von Wassermolekülen umgeben. Dabei entsteht um jedes Ion eine Hydrathülle. Zwischen Ion und Wassermolekülen bilden sich neue Anziehungskräfte (Ionen-Dipol-Wechselwirkungen). Bei diesem Vorgang wird Energie an die Umgebung abgegeben – diese nennt man Hydratationsenergie.
Dargestellt durch den orangenen Pfeil!
Gitterenergie
In einem festen Salz sind die Ionen durch elektrostatische Anziehungskräfte in einem regelmäßigen Gitter angeordnet. Diese Kräfte halten das Ionengitter zusammen. Wird das Gitter aufgetrennt, müssen diese Anziehungskräfte überwunden werden. Die dafür erforderliche Energie nennt man Gitterenergie.
Dargestellt durch den blauen Pfeil!
Diagramme zum Energieumsatz beim Lösen von Salzen
Energiediagramme zur Beschreibung des Lösevorgangs von verschiedenen Salzen.2