Aufgaben
- Beschreiben Sie das in M1 dargestellte Diagramm.
- Erklären Sie mit Hilfe von M1 und M2, wie sich zunehmende Emissionen von Kohlenstoffdioxid auf die Reaktion 1 – 4 auswirken.
- Erläutern Sie die in M3 dargestellten Folgen für Korallen und andere kalkskelettbildende Meeresbewohner.
- Entnehmen Sie M4 die Definition des so genannten pH-Wertes. Erläutern Sie basierend darauf die Korrelation zwischen den rot, grün und blau dargestellten Messwerten.
- Die so genannte Versauerung der Meere wird auch als böser Zwilling der Klimaerwärmung bezeichnet. Stellen Sie den Zusammenhang dieser Aussage dar.
Je mehr Kohlenstoffdioxid in der Atmosphäre, desto ...
Weiteres
Die Weltmeere sind der größte Kohlendioxidspeicher unseres Planeten. Durch die zunehmenden menschlichen Emissionen von Kohlenstoffdioxid nehmen die Meere immer mehr davon auf.
Die Konzentration von Kohlenstoffdioxid im Meer und der pH-Wert der Meere werden u.a. in der 1988 ins Leben gerufenen Station ALOHA der Universität Hawaii gemessen. Die Messwerte für den Anteil von Kohlenstoffdioxid in der Atmosphäre stammen von der nahe gelegenen Station Mauna Loa. Abb. 1 zeigt das Ergebnis der Messungen.
- Rote Kurve: Anteil von Kohlenstoffdioxid in der Atmosphäre (linke y-Achse)
- Grüne Kurve: Konzentration Kohlenstoffdioxid im Meer (linke y-Achse)
- Blaue Kurve: pH-Wert des Meeres (rechte y-Achse)
Weiteres
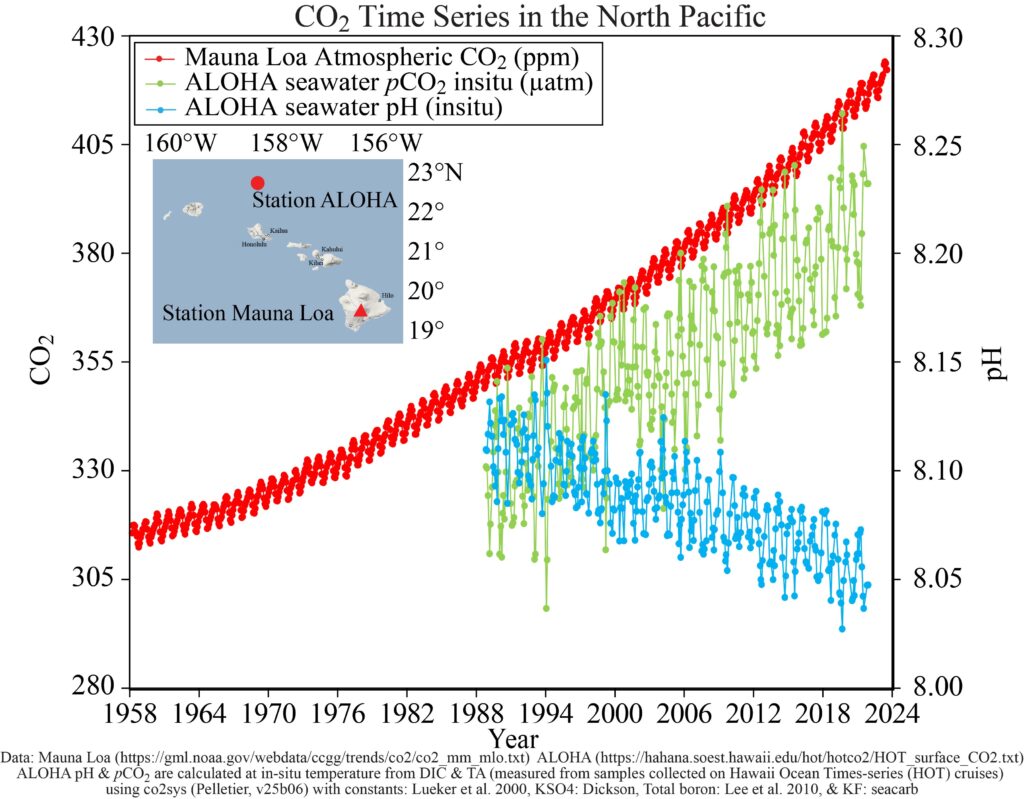
Messungen im Nordpazifik1
Kohlenstoffdioxid-Aufnahme in den Meeren
Kohlenstoffdioxid wird in Wasser nicht einfach gelöst, sondern es finden mehrere chemische Reaktionen statt.
Folgen
kalkbildende Meeresbewohner leiden
Die bekanntesten Korallen sind Steinkorallen, die den Hauptanteil an der Entstehung der Korallenriffe haben, die artenreichsten marinen Lebensräume auf der Erde. Sie bilden ein Kalkskelett, das zu 99,7 % aus Calciumcarbonat (CaCO3) besteht. Hierfür nehmen die Korallen zu jeweils einem Calcium-Ion (Ca2+) zwei Hydrogencarbonat-Ionen auf und bilden daraus Calciumcarbonat.
Der zunehmende Eintrag von Kohlenstoffdioxid aus der Erdatmosphäre in die Meere hat jedoch zur Folge, dass die Steinkorallen schwieriger Kalkstrukturen aufbauen können. Auch andere kalkbildende Meeresbewohner wie Muscheln oder Flügelschnecken sind von dieser Problematik betroffen.
Studien zeigen außerdem, dass bei einer anhaltenden „Versauerung“ die Löslichkeit von Calciumcarbonat in Wasser ansteigt und so auch bereits gebildete Kalkskelette wieder aufgelöst würden.
Weiteres
Daneben kommt es zur sogenannten Korallenbleiche, wenn das Wasser zu warm wird.

Steinkorallen im Great Barrier Reef.2
Der pH-Wert
Der Begriff des pH-Werts geht auf Søren Sørensen zurück. Schon zu Beginn des 20. Jahrhunderts wusste man, dass die Konzentration an H3O+ ein wertvolles Maß für die Azidität einer wässrigen Lösung ist.
Ein Maß für die Azidität wässriger Lösungen
Die Oxonium-Ionen-Konzentration ist oft sehr klein: In neutralem Wasser bspw. beträgt sie nur 0,0000001 mol/L. Man kann solche Zahlen als 10x schreiben, in diesem Fall 10-7 mol/L.
In Magensäure ist die Konzentration der Oxonium-Ionen in etwa 0,01 mol/L = 10-2 mol/L. Das ist das 10000-fache von der in Wasser.
Søren Sørensen schlug vor, mit dem pH-Wert nur die Zahl über der 10 zu betrachten. Mathematisch gesagt nimmt er den dekadischen Logarithmus und erhält den Exponenten. Weil die Zahlen in aller Regel negativ sind (im Beispiel oben -7 und -2) kehrte er mit dem pH-Wert dann noch das Vorzeichen um, um nicht ständig ein Minus mitzuschleppen: 7 und 2.
In seiner Skala ist pH 7 neutral, je weiter unter 7, desto saurer, je weiterüber 7 desto basischer.


