Was ist eigentlich eine Säure? Man kennt die Begriffe Säure und sauer, vielleicht auch Base, Lauge und alkalisch. Meistens verbindet man damit bestimmte Eigenschaften, die diese Stoffe haben: Zum Beispiel schmecken Säuren sauer und reagieren mit unedlen Metallen. Basen können Fette lösen.
Auf der Stoffebene kann man sagen: Säuren sind Stoffe, die in Wasser saure Lösungen bilden und Basen sind Stoffe, die in Wasser alkalische Lösungen bilden.
Aufgaben
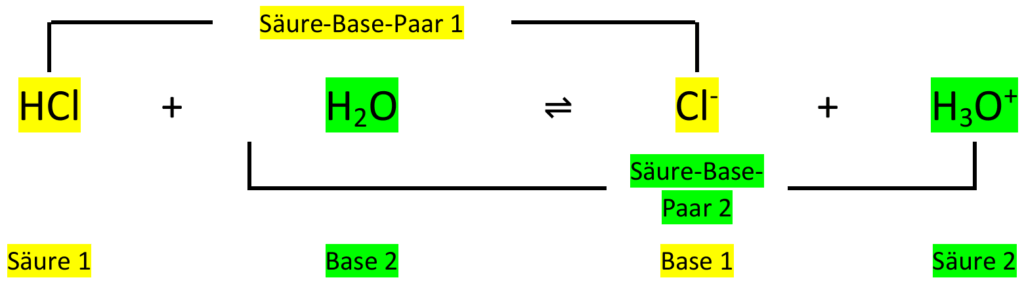
- Machen Sie sich mit den historischen Begriffsbedeutungen in M1 vertraut. Zeichnen Sie die Strukturformeln in das Beispiel der Reaktion von Chlorwasserstoff mit Wasser ein und kennzeichnen Sie die Protonenübertragung. Zeigen Sie an diesem Beispiel, was man unter Protonendonator und Protonenakzeptor im Sinne Brönsteds versteht.
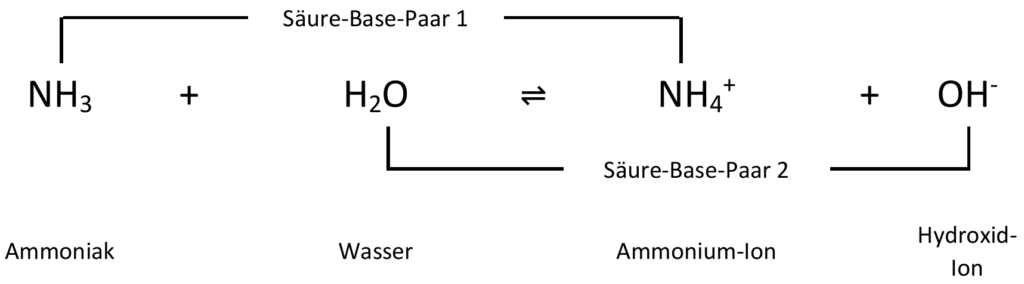
- Zeichnen Sie die Strukturformeln in das Beispiel der Reaktion von Ammoniak mit Wasser in M2 ein, kennzeichnen Sie die Protonenübertragung und ordnen Sie die Begriffe Säure und Base zu.
- Vergleichen Sie das Reaktionsverhalten des Wassermoleküls in den beiden Beispielen.
- Übertragen Sie das Konzept und die entsprechenden Fachbegriffe auf die Reaktionen 3 und 4 aus dem Material „Versauerung der Meere“. Stellen eine begründete Vermutung auf, warum die Kohlensäure ein Beispiel für eine so genannte mehrprotonige Säure darstellt. Recherchieren Sie den Begriff Ampholyt und wenden Sie diesen hier an.
Ein Blick in die historische Begriffsbedeutung
Weiteres
Es gab in der Geschichte der Chemie die Bestrebung, die Eigenschaften der Stoffklasse der Säuren zunehmend auf der Teilchenebene zu erklären. Das noch heute verwendete Konzept ist das des dänischen Chemikers Brønsted.
Robert Boyle (1627 - 1691)
Säuren Schmecken sauer, färben Lackmus rot. Basen färben roten Lackmus blau, heben die Wirkung von Säuren auf. Lackmus ist ein Säure-Base-Indikator. Seine Farbe lässt Rückschlüsse auf das Vorhandensein einer Säure oder Base zu.1
Antoine Lauren Lavoisier (1743 - 1794)
Säuren enthalten Sauerstoff. Der wissenschaftliche Name für Sauerstoff Oxygenium bedeutet Säurebildner.2
Hymphry Davy (1778 - 1829)
Nein, Säuren enthalten Wasserstoff!3
Justus von Liebig (1803 - 1873)
Der Wasserstoffgehalt ist eine notwendige, aber nicht hinreichende Bedingung für eine Säure; der Wasserstoff muss durch Metalle ersetzbar sein.4
Svante Arrhenius (1859 - 1927)
Säuren sind Stoffe, deren wässrige Lösung Wasserstoff-Ionen enthalten. Basen sind Stoffe, deren wässrige Lösungen Hydroxid-Ionen enthalten.5
Johannes Brønsted (1879 - 1947)
Säuren sind Protonendonatoren (von donare (lat.) = geben/schenken), Basen sind Protonenakzeptoren (von accipere (lat.) = annehmen).
Bei einer Säure/Base-Reaktion findet ein Protonenübergang (= Protolyse) von einem Säure-Teilchen auf ein Base-Teilchen statt. Betrachtet man verschiedene Säure-Base-Reaktionen, so erkennt man Teilchenpaare, bei denen die beiden Teilchen sich jeweils um ein Proton unterscheiden, wie z.B. HCl und Cl–, H3O+ und H2O.
Ein solches Paar von Teilchen nennt man korrespondierendes Säure-Base-Paar. An jeder Säure-Base-Reaktion sind stets zwei korrespondierende Säure-Base-Paare beteiligt.6
Anwendung des Säure-Base-Konzepts nach Brønsted
Weiteres
Protolysegleichgewichtsreaktion von Chlorwasserstoff:
Protolysegleichgewichtsreaktion von Ammoniak:
Weitergedacht
-
Begründen Sie mit Hilfe von M3, warum Natriumhydroxid im Sinne des Brønsted-Konzepts nicht als Base gilt, sondern als ein Stoff, der aus einer Base aufgebaut ist, bezeichnet werden kann.
-
Erklären Sie mit Hilfe von M4, warum alle sauren Lösungen im Sinne Brønsteds sauer schmecken.
Entstehung alkalischer Lösungen
Weiteres
Im Vergleich zur Bildung von sauren Lösungen können alkalische Lösungen auf verschiedene Art hergestellt werden. Neben der Säure-Base-Reaktion zwischen einer Brønsted-Base und Wasser können Hydroxid-Ionen auch durch die Reaktion von bestimmten Metallen und Metalloxiden mit Wasser entstehen, zum Beispiel:
Alkalische Lösungen entstehen zudem durch das Lösen von Metallhydroxiden in Wasser. Metallhydroxide sind Salze, die aus Metall-Kationen und Hydroxid-Ionen aufgebaut sind. Das bekannteste Beispiel ist Natriumhydroxid (NaOH), das in Wasser gelöst die sogenannte Natronlauge (Bezeichnung für die alkalische Lösung) bildet:
Forscher klären "Sauergeschmack" auf
Weiteres
Was passiert in den Geschmacksknospen der Zunge, wenn sie durch einen Schluck Zitronensaft stimuliert werden?
Wissenschaftler haben in einigen Geschmackszellen einen besonderen Ionenkanal gefunden, der auf saure Reize reagiert. Ionenkanäle sind Poren in der Zellmembran, die im geöffneten Zustand elektrisch geladene Teilchen – Ionen – von einer Seite der Membran auf die andere fließen lassen. […]. Reizt man die Geschmackszellen mit vielen Protonen, konnten die Wissenschaftler in den Geschmackszellen nun einen erhöhten Ionenstrom messen. Der Ionenkanal besitzt folglich Bindungsstellen für Protonen und dient deshalb als Rezeptor.
Damit hat das Forscherteam den „Sauer-Geschmack“ aufgeklärt und entdeckt, dass die Ionenkanäle protonengesteuert arbeiten.7

Ein junges Mädchen beißt in eine Zitronenscheibe.8
