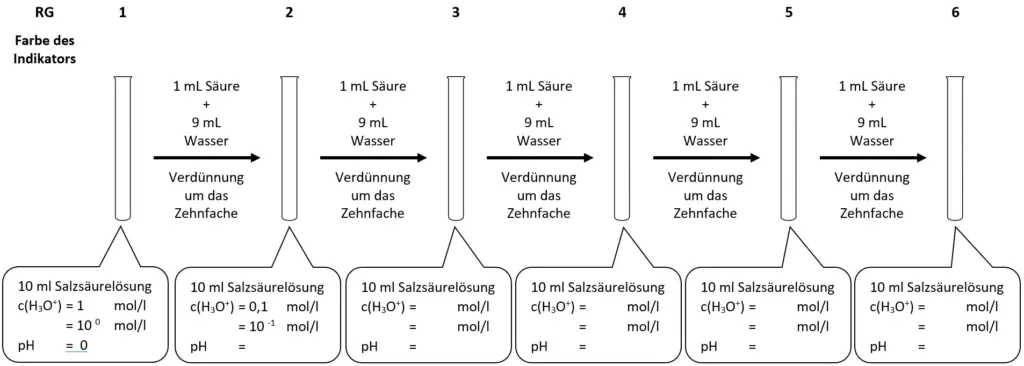
Wie muss eine 10 mL Salzsäurelösung mit pH = 3 verdünnt werden, um eine Salzsäurelösung mit dem pH = 6 herzustellen?
Aufgaben
- Führen Sie den Versuch V1 durch und dokumentieren Sie ihre Beobachtungen mit Hilfe der Vorlage. Ermitteln Sie aus dem pH-Wert die Konzentration der Oxonium-Ionen in der natürlichen und in der Exponentenschreibweise und ergänzen Sie so die Lücken in den Sprechblasen ihrer Auswertungsvorlage.
- Die Buchstaben p und H von pH wurden von den lateinischen Begriffen potentia hydrogenii abgeleitet. Was könnte damit gemeint sein?
- Arbeiten Sie den Zusammenhang zwischen dem pH-Wert, der Verdünnung und der Oxonium-Ionen-Konzentration heraus. Welche Regelmäßigkeiten können Sie feststellen?
- Leiten Sie mithilfe ihrer Erkenntnisse eine Definition für den pH-Wert ab (in Worten oder ggf. als mathematischen Ausdruck).
V1
Verdünnungsreihe von Salzsäure
Materialien
- Schutzbrille
- 6 Reagenzgläser
- Reagenzglasständer
- 1 mL Spritze
- 10 mL Spritze
- Becherglas
Chemikalien
- Salzsäure (1 mol / L)
- Universalindikator
- pH-Indikatorpapier
-
dest. Wasser
- im Becherglas als Vorrat für die Verdünnungsreihe
Hinweis
Bei diesem Versuch kommt es auf Genauigkeit an! Messen Sie die angegebenen Volumina so genau wie möglich ab. Ansonsten könnte ihr Ergebnis nicht zufriedenstellend sein.
Durchführung
- Befüllen Sie das erste Reagenzglas mit 10 mL einmolarer Salzsäure.
- Überführen Sie genau 1 mL Salzsäure aus dem ersten Reagenzglas in das zweite Reagenzglas. Fügen Sie zum zweiten Reagenzglas 9 mL dest. Wasser hinzu und schütteln/schwenken Sie vorsichtig gut durch.
- Verfahren Sie mit den restlichen Reagenzgläsern nach dem gleichen Schema.
- Versetzen Sie alle Reagenzgläser mit 5 Tropfen Indikatorlösung und lesen Sie mit Hilfe einer pH-Farbskala den pH-Wert der Lösung ab. Überprüfen Sie ggf. den pH-Wert der Lösungen zusätzlich mit einem pH-Indikatorpapier.
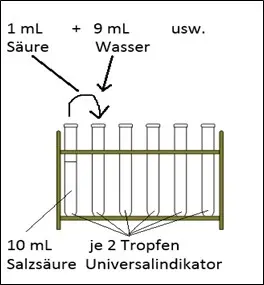
Versuchsskizze.
Entsorgung
- Alle Lösungen über den Abguss entsorgen.
- Glasgefäße spülen und wieder an ihren Ursprungsort zurückstellen.