Wässrige Lösungen von Salzen leiten den elektrischen Strom. Die elektrische Leitfähigkeit einer Salzsäure-Lösung ist um ein Vielfaches größer. Reinstes Wasser weist jedoch auch eine elektrische Leitfähigkeit auf!
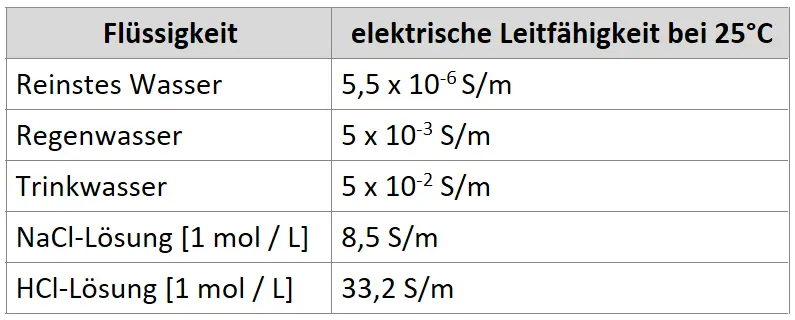
Die elektrische Leitfähigkeit verschiedener Lösungen im Vergleich. Die Leitfähigkeit wird hier in Siemens pro Meter angegeben.
Aufgaben
- Erklären Sie mit Hilfe von M1 die unterschiedlich große elektrische Leitfähigkeit verschiedener Lösungen in Tabelle 1. Stellen Sie hierbei heraus, welchen Rückschluss man aus der Leitfähigkeit von reinstem Wasser ziehen kann.
- Formulieren Sie mit Hilfe von M1 und M2 in eigenen Worten einen Zusammenhang zwischen der Autoprotolyse des Wassers, dem Ionenprodukt des Wassers und dem pH-Wert von Wasser. Stellen Sie dabei alltagssprachlich heraus, worüber der pH-Wert und der pOH-Wert nach ihrem Verständnis eine konkrete Aussage macht.
Wissenswertes zur elektrischen Leitfähigkeit wässriger Lösungen
Ladungstransporte
Wässrige Lösungen von Salzen können elektrischen Strom leiten. Taucht man zwei Elektroden in eine solche Lösung und legt eine Spannung an, so fließt Strom. Ursache ist die Beweglichkeit der Ionen: Kationen wandern im elektrischen Feld zur Kathode (Minuspol) und können dort Elektronen aufnehmen, während Anionen zur Anode (Pluspol) wandern und dort Elektronen abgeben.
Die elektrische Leitfähigkeit hängt sowohl von der Konzentration als auch von der Art der gelösten Ionen ab. Besonders hoch ist sie in Lösungen, die Oxonium-Ionen (H3O+) oder Hydroxid-Ionen (OH–) enthalten. Der Grund: Protonen im Oxonium-Ion wechseln extrem schnell von einem Wassermolekül zum nächsten (Lebensdauer ca. 10-13 s). Dieser schnelle Staffellauf der Protonen sorgt für eine außergewöhnlich gute Leitfähigkeit. Der zugrunde liegende Transportmechanismus wird Grotthuß-Mechanismus genannt – nach Theodor Grotthuß (1785–1822).
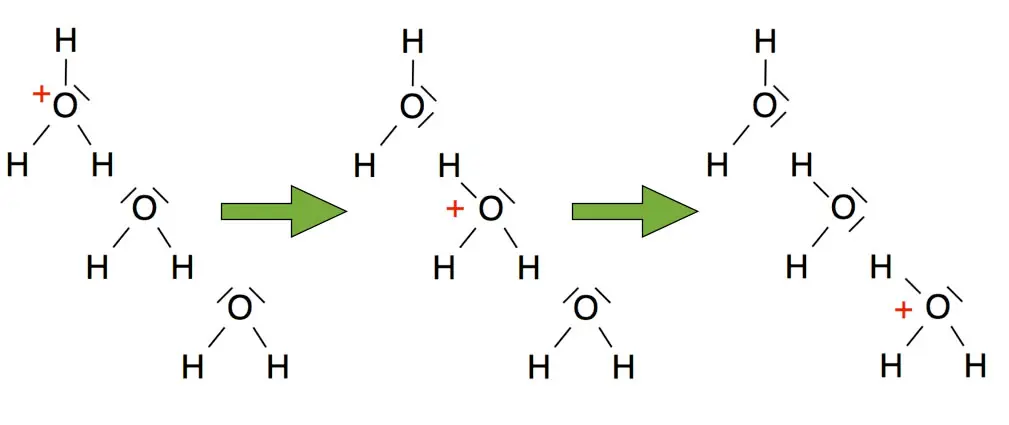
Vereinfachte und schemenhafte Darstellung des Grotthuß-Mechanismus.
Die Autoprotolyse des Wassers
Wasser kann nicht nur Lösungsmittel sein, sondern auch selbst als Säure und Base reagieren: Ein Wassermolekül überträgt dabei ein Proton auf ein anderes. Dieser Vorgang heißt Autoprotolyse des Wassers.
Dadurch entstehen in reinem Wasser stets geringe Mengen an Oxonium-Ionen (H3O+) und Hydroxid-Ionen (OH–). Ihre Konzentration ist sehr klein, lässt sich aber nachweisen und wird in der folgenden Darstellung anschaulich verdeutlicht.
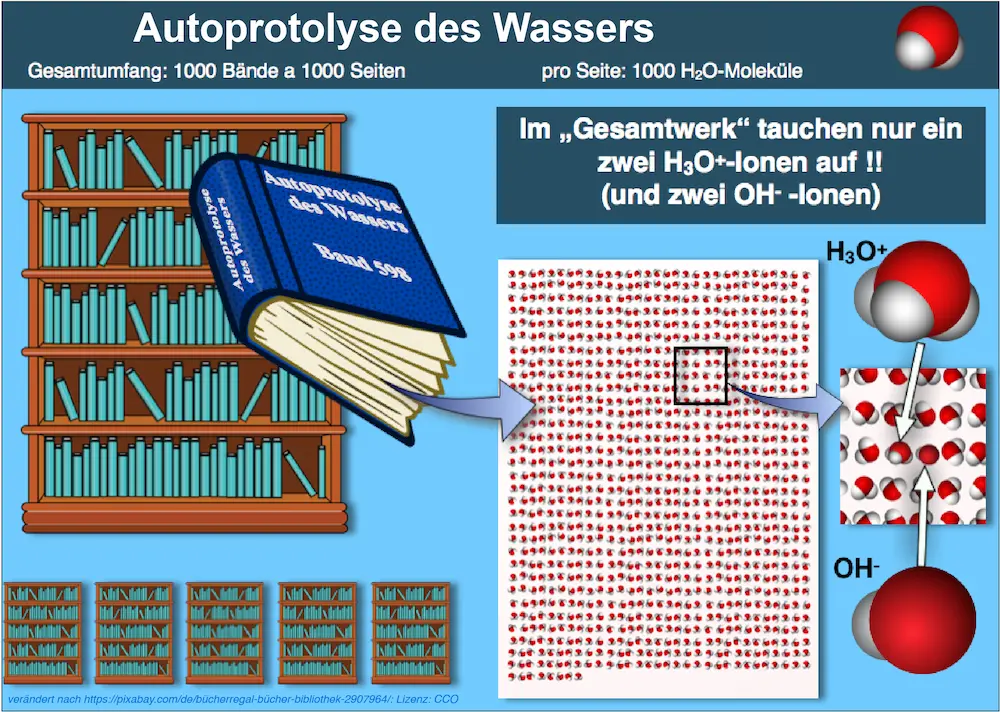
Eine vereinfachte Darstellung der Autoprotolyse des Wassers.1
The Simple Club: Die Autoprotolyse des Wassers.
Die Autoprotolyse im Detail
Autoprotolyse des Wassers
Wässrige Lösungen von Salzen leiten den elektrischen Strom. Daraus folgt, dass sie Ionen enthalten. Messungen zeigen jedoch: Auch reinstes Wasser besitzt eine – wenn auch sehr geringe – elektrische Leitfähigkeit. Die darin vorhandenen Ionen sind Oxonium-Ionen (H3O+) und Hydroxid-Ionen (OH–). Sie entstehen durch die Autoprotolyse des Wassers:
Dabei wirkt ein Wassermolekül als Säure (Protonendonator), das andere als Base (Protonenakzeptor). Wasser ist somit amphoter. Das Gleichgewicht liegt allerdings stark auf der linken Seite, d.h. die Rückreaktion überwiegt deutlich.
Aus Leitfähigkeitsmessungen wurde die Gleichgewichtskonstante Kc bei 25 °C bestimmt:
Die Konzentration des Wassers beträgt bei 25 °C etwa c(H2O) = 55,4 mol/L. Da sich diese Konzentration durch die Autoprotolyse praktisch nicht verändert, kann sie in die Konstante einbezogen werden. Es entsteht die temperaturabhängige Konstante KW:
Man nennt KW auch das Ionenprodukt des Wassers.
Der pH-Wert
Um die sehr kleinen Konzentrationen der Oxonium-Ionen anschaulicher anzugeben, wurde der pH-Wert eingeführt:
Beispiel: Wird eine Salzsäure mit pH = 2 zehnfach verdünnt, so steigt der pH-Wert auf 3. Eine erneute zehnfache Verdünnung führt zu pH = 4. Jede pH-Stufe entspricht also einer zehnfachen Änderung der Oxonium-Ionen-Konzentration. Damit gilt: Je größer der pH-Wert, desto geringer die Konzentration an Oxonium-Ionen.
Weiteres
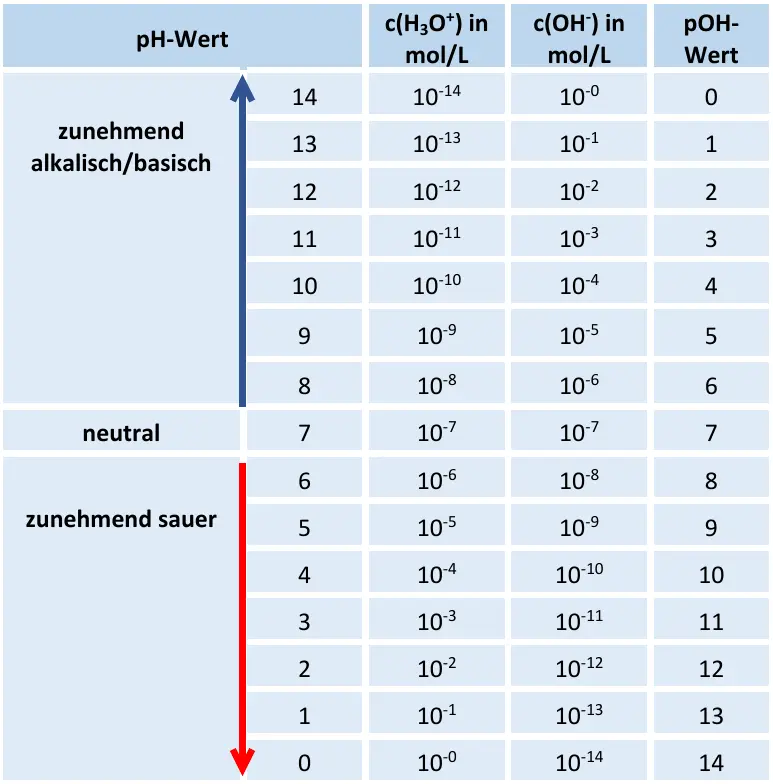
pH- und pOH-Wertetabelle. 2
Zusammenhang mit Hydroxid-Ionen
In alkalischen Lösungen dominieren Hydroxid-Ionen. Über das Ionenprodukt des Wassers sind beide Ionensorten miteinander verknüpft:
Eine saure Lösung mit pH = 3 (also c(H3O+) = 10-3 mol/L) enthält gleichzeitig eine Hydroxid-Ionen-Konzentration von c(OH–) = 10-11 mol/L. Umgekehrt besitzt eine alkalische Lösung mit pH = 11 nur c(H3O+) = 10-11 mol/L, dafür aber c(OH–) = 10-3 mol/L.
Analog zum pH-Wert definiert man den pOH-Wert:
Setzt man beide Definitionen in das Ionenprodukt ein, ergibt sich die wichtige Beziehung:
Damit lässt sich aus dem pH-Wert stets der pOH-Wert berechnen – und umgekehrt.
Aufgaben zum pH-Wert
- Berechnen Sie die Konzentration der Oxonium- und Hydroxid-Ionen aus den nachfolgenden pH-Werten wässriger Lösungen. Geben Sie an, ob die Lösungen sauer, neutral oder alkalisch/basisch sind.
- 1
- 4
- 8
- 12
- 13.5
- Berechnen Sie den pH-Wert der folgenden wässrigen Lösungen mit angegebener Oxonium-Ionen-Konzentration. Geben Sie an, ob die Lösungen sauer, neutral oder alkalisch/basisch sind.
- 10-4 mol/L
- 5 ‧ 10-7 mol/L
- 10-8 mol/L
- 3 ‧ 10-10 mol/L
- 0,4 mol/L
- 1,6 mol/L
- Berechnen Sie den pH-Wert der folgenden wässrigen Lösungen mit angegebener Hydroxid-Ionen-Konzentration. Geben Sie an, ob die Lösungen sauer, neutral oder alkalisch/basisch sind.
- 0,1 mol/L
- 10-4 mol/L
- 10-7 mol/L
- 4 ‧ 10-7 mol/L
- 10-11 mol/L


