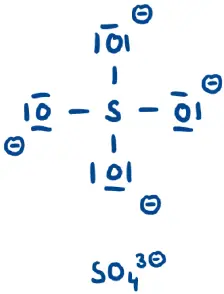Viele chemische Verbindungen tragen im Alltag Namen, die kaum einen Hinweis auf ihre chemische Formel geben. Ein bekanntes Beispiel ist Kalk – damit ist das Salz Calciumcarbonat (CaCO3) gemeint.
Diese Namensgebung hat historische Gründe: Der Begriff Kalk war lange vor der genauen Kenntnis der chemischen Zusammensetzung gebräuchlich.
Aufgaben
- Ergänzen Sie die fehlenden Angaben in der Tabelle 1 in M1 (grüne Kästchen) und recherchieren Sie ggf. fehlende Informationen.
- Skizzieren Sie die Strukturformeln des dritten und vierten Mitglieds der homologen Reihe der Alkansäuren. Notieren Sie jeweils eine Protolysegleichgewichtsreaktion mit Wasser und benennen Sie die Produkte mit Hilfe von M2.
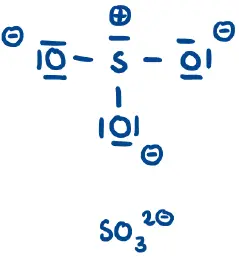
- Geben Sie die Oxidationszahlen der Atome in Abb. 2 und Abb. 3 an. Bereiten Sie sich darauf vor, die verschiedenen Endungen zu erläutern.
Bezeichnung gängiger Säuren und ihrer Salze
Weiteres
Die Problematik der Namensgebung zeigt sich besonders deutlich bei Säuren und ihren Salzen. Deren Bezeichnungen können in doppelter Hinsicht verwirrend sein: Einerseits spiegeln die geläufigen Namen der Salze nicht immer ihre chemische Zusammensetzung wider, anderseits weisen sie nicht zwingend auf die jeweilige Säure hin, von der sie abgeleitet sind. So ist Calciumcarbonat ein Salz der Kohlensäure (H2CO3).
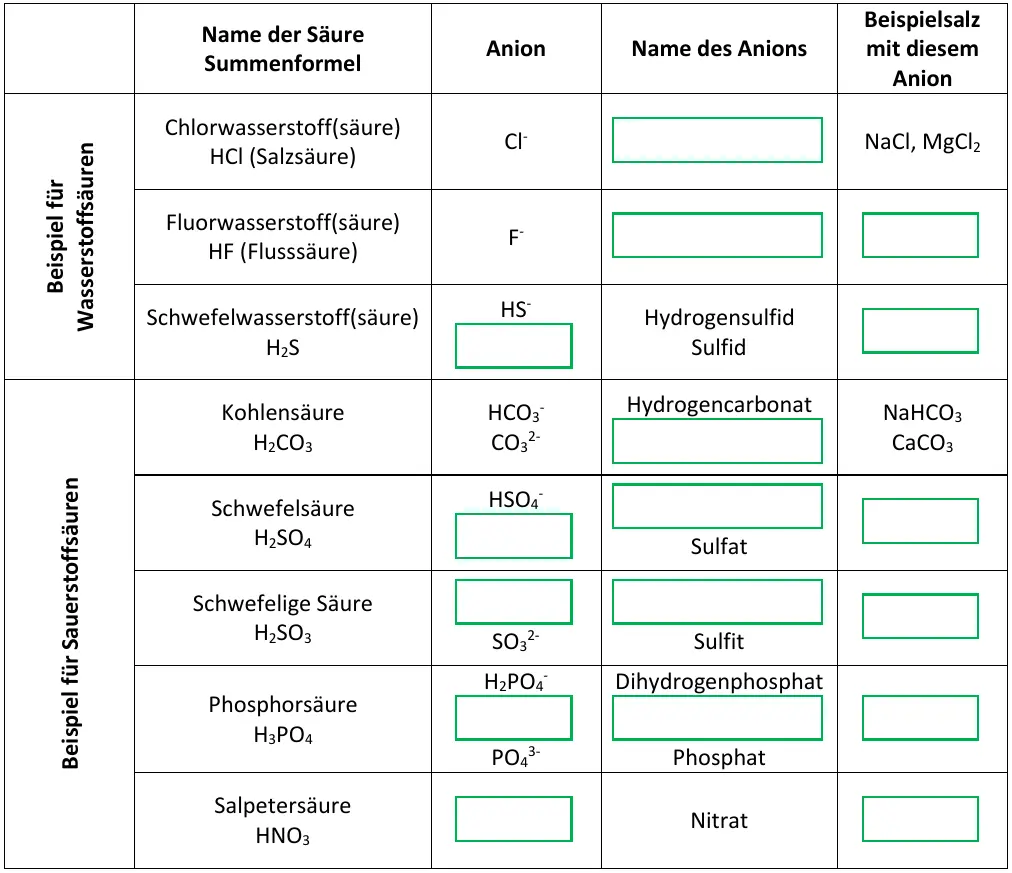
Übersicht verschiedener Säuren. Die grünen Lücken sind auszufüllen.1
Namensgebungen
Homologe Reihe der Alkansäuren
Neben den anorganischen Sauerstoffsäuren und Wasserstoffsäuren gibt es auch noch organische Sauerstoffsäuren. Diese leiten sich von den entsprechenden Alkanen ab und werden Alkansäuren genannt. Wie aus der EF bekannt bilden Alkansäuren eine homologe Reihe: Methansäure, Ethansäure, Propansäure u.s.w.
Strukturmerkmal dieser Säuren ist die funktionelle Gruppe aller Carbonsäuren: Die Carboxylgruppe (auch Carboxygruppe oder Carbonsäuregruppe genannt). Sie wird in Halbstrukturformeln gerne mit COOH abgekürzt:
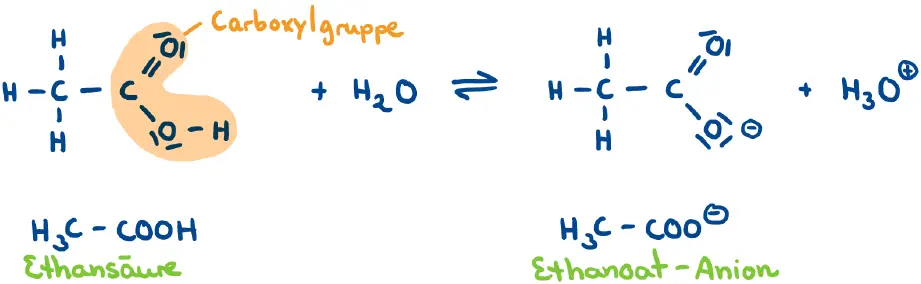
Protolyse von Ethansäure (Essigsäure).2
Die Bezeichnung der Anionen der organischen Sauerstoffsäuren endet auf oat. Auch hier gibt es teilweise andere Namen aufgrund fehlender Kenntnisse über die chemische Zusammensetzung der Säuren. Zum Beispiel wird das Anion der Ethansäure auch Acetat genannt, oder das Anion der Zitronensäure Citrat.
Chemische Zusammensetzung und ihre Endung
Die Endungen der Namen der Anionen liefern uns wichtige Informationen:
Die Namen von Nichtmetall-Anionen enden in der Regel mit dieser Endung. Zum Beispiel Fluorid (F–), Phosphid (P3-) u.s.w.
Die Namen von Nichtmetall-Anionen, die Sauerstoff enthalten, können auf -at enden, wenn am zentralen Atom der Verbindung die maximale Anzahl an Sauerstoff-Atomen gebunden ist. Dann besitzt das zentrale Atom in der Regel die höchstmögliche Oxidationszahl.
Die Namen von Nichtmetall-Anionen, die Sauerstoff enthalten, können auch auf -it enden, jedoch besitzt das zentrale Atom der Verbindung weniger als die maximal mögliche Anzahl an gebundenen Sauerstoff.