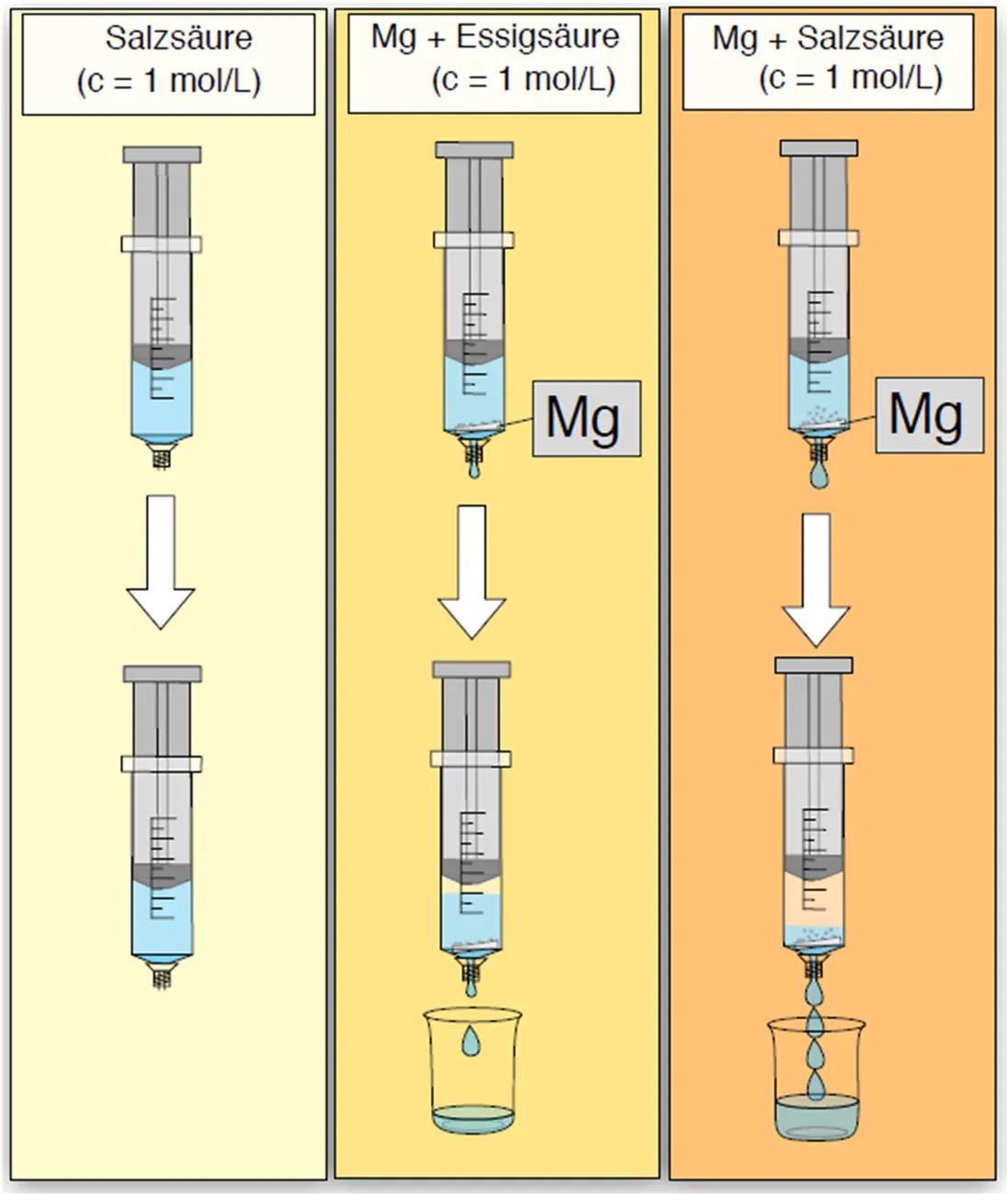
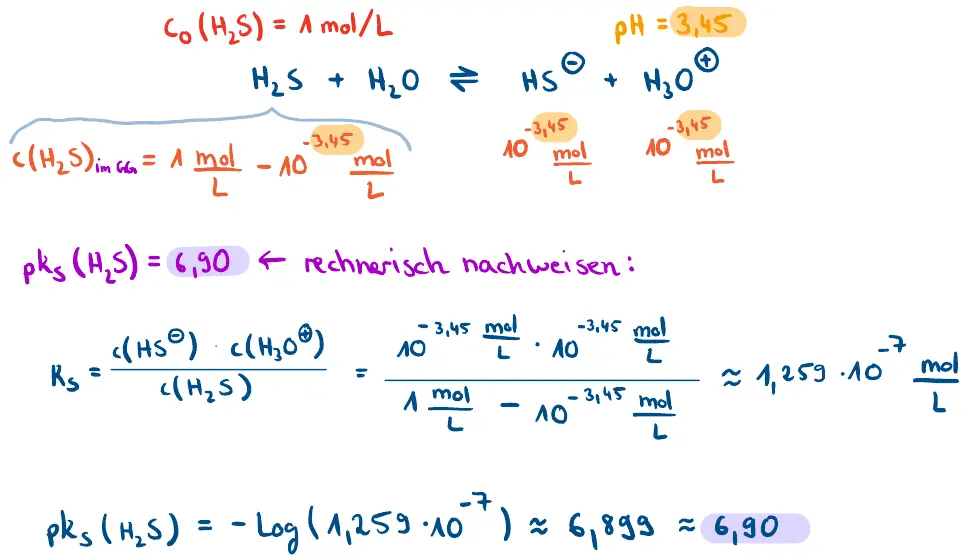Betrachten Sie einmal den folgenden Versuch und notieren Sie, welche Beobachtungen hier verwunderlich erscheinen und warum!
Aufgaben
- Erklären Sie ihre Beobachtungen, indem Sie eine Reaktionsgleichung für die Reaktion zwischen Magnesium und den jeweiligen Säuren notieren und Material M1 heranziehen.
- Erklären Sie mit Hilfe von M2, was man unter der Säure- und Basenkonstante versteht. Formulieren Sie einen Je…desto-Satz für den pKS und pKB-Wert eines Stoffes.
- Benennen Sie Auffälligkeit zwischen dem pKS– und pKB-Wert korrespondierender Säure-Base-Paare in Abbildung 3. Erläutern Sie diese mit Hilfe von M3.
Reaktion von Säuren mit Magnesium
Materialien
- Schutzbrille
- 3 Spritzen 50 mL
- 3 Bechergläser
- 3 Stativstangen
- 3 Stativ-Fundamente
- 3 Stativmuffen
- 3 Stativklemmen
Chemikalien
- Salzsäure (1 mol/L)
- Essigsäure (1 mol/L)
-
2 x 3 cm Magnesiumband
- Lässt sich mit einer Schere und einem Lineal zuschneiden
Durchführung
- Zwei gleichgroße Stücke Magnesiumband (ca. 3 cm) etwas zusammenknüllen und in jeweils eine 50 mL Spritze geben. Stempel so weit es geht hineindrücken.
- Eine leere 50 mL Spritze für einen Kontrollansatz bereithalten.
- Stative aufbauen, sodass die Spritzen mit der Öffnung nach unten über je einem Becherglas locker hängen.
- Unter den hängenden Spritzen Lösungen vorlegen: Unter der ersten (leeren) Spritze 1 molare Salzsäure, unter der zweiten Spritze 1 molare Essigsäure, unter der dritten Spritze 1 molare Salzsäure.
- Nacheinander die Spritzen zügig vollständig mit der darunter stehenden Lösung aufziehen und zurück ins Stativ hängen.
Beobachtung
Das folgende Video zeigt den Versuch:
Säurestärke demonstrieren in Spritzen.
Aufräumen
- Spritzen durch Aufziehen mit Leitungswasser spülen und trocknen. Bechergläser spülen und trocknen.
- Überschüssiges Magnesiumband durch Reaktion mit Salzsäure auflösen.
- Überschüssige Lösungen stark verdünnen und über den Abguss entsorgen.
- Alle Materialien an ihren Ursprungsort zurückstellen.
Genauer hingeschaut
Weiteres
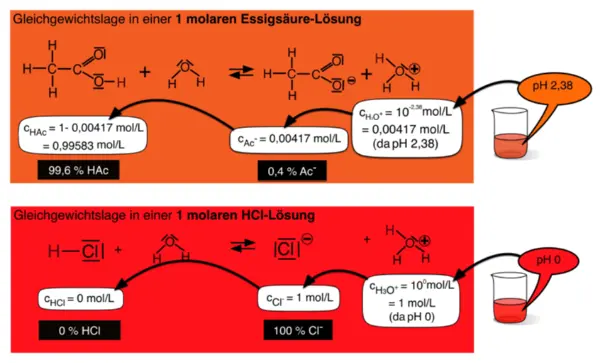
Betrachten wir einmal die Protolysegleichgewichtsreaktionen von Salz- und Essigsäure mit Wasser!
Schematische Darstellung der Gleichgewichtslage einer 1 molaren Salz- und Essigsäure-Lösung.1
Aus der Kenntnis der Oxoniumionen-Konzentrationen im chemischen Gleichgewicht können alle anderen Konzentrationen ermittelt werden. So lässt sich die Gleichgewichtskonstante KS (= Säurekonstante) mit Hilfe des Massenwirkungsgesetzes aufstellen, zum Beispiel für die Protolyse der Essigsäure:
Für die Protolyse der Salzsäure gilt demnach:
Für die Salzsäure ergibt sich das Problem, dass bei den gegebenen Werten beim Einsetzen in das Massenwirkungsgesetz durch Null dividiert werden würde. Dies wäre mathematisch nicht zulässig. In Wahrheit liegen bei höheren Konzentrationen auch Salzsäure-Moleküle vor. Im Nenner steht also bei ganz exakter Messung doch keine Null! Die Oxoniumionen-Konzentration in einer 1 molaren Salzsäure ist statt 1 mol/L nur 0,999999 mol/L. Bedenken wir also, dass die pH-Werte der beiden Lösungen in der Abb. 2 (pH 0 und pH 2,38) nicht ganz exakt aber fast korrekt sind.
Für die Gleichgewichtskonstante KS für die Protolyse der Salzsäure gilt also:
Basenkonstante und Fazit
Weiteres
Für die Protolysereaktion einer Base erhält man in der gleichen Art und Weise die Basenkonstante KB:
Anstelle des KS– oder KB-Werts wird häufig der pKS– bzw. pKB-Wert angegeben, der wiederum dem negativen dekadischen Logarithmus des jeweiligen KS– bzw. KB-Werts entspricht. pKS– und pKB-Werte ermöglichen die Einteilung von Säuren und Basen nach ihrer Stärke.
Weiteres
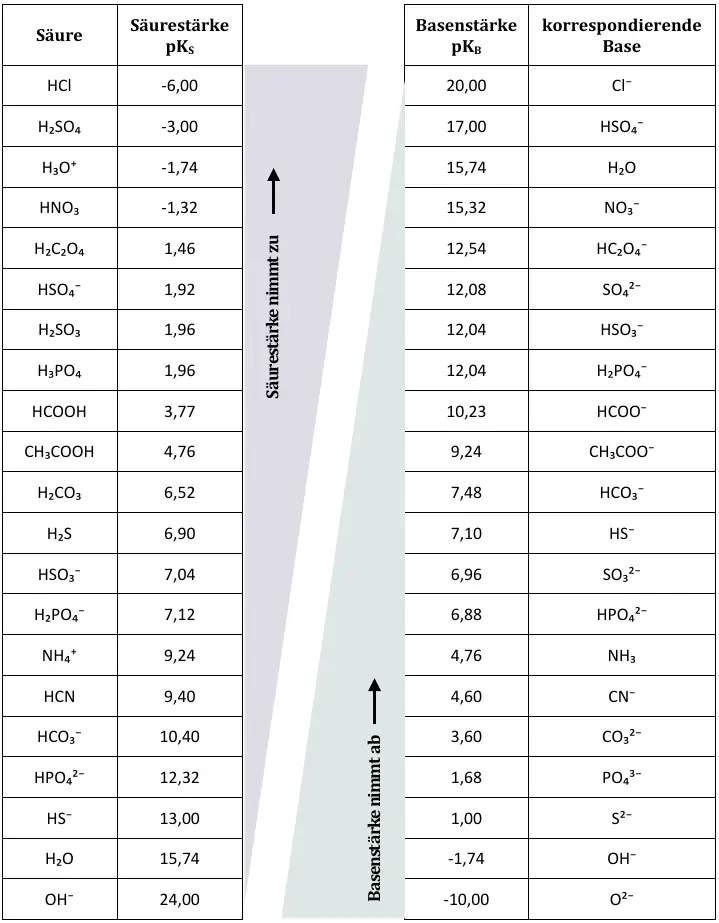
pKS– und pKB-Werte bekannter Säuren und ihrer korrespondierenden Basen.2
Gleichgewichtskonstanten korrespondierender Säure-Base-Paare
Weiteres
Die Reaktion einer Säure (hier mit HA abgekürzt) und ihrer korrespondierenden Base A– mit Wasser können als Gleichgewichtsreaktion betrachtet werden:
Der KS-Wert einer Säure HA und der KB-Wert ihrer korrespondierenden Base A– hängen voneinander ab. Dieser Zusammenhang zeigt sich, wenn man die Gleichgewichtskonstanten durch Multiplikation zusammenfasst:
Durch Kürzen ergibt sich daraus das uns bereits bekannte Ionenprodukt des Wassers KW:
Weiteres
Bei 25 °C gilt somit:
Wird der negative dekadische Logarithmus angewandt, erhält man:
Folglich kann man bei korrespondierenden Säure-Base Paaren bei bekanntem pKS-Wert den pKB-Wert der korrespondierenden Base berechnen, und umgekehrt. Aus der Gleichung lässt sich ebenfalls ableiten:
Je stärker eine Säure, desto schwächer ist ihre korrespondierende Base. Je stärker die Base, desto schwächer ist ihre korrespondierende Säure.
Säuren und Basen kann man nach ihren jeweiligen pKS– und pKB-Werten einteilen:

Einteilung von Säuren und Basen nach ihrem pKS– bzw. pKB-Wert.
Übung
- Gegeben sei eine Schwefelwasserstoff-Lösung mit der Konzentration c0(H2S) = 1 mol/L und einem pH-Wert von 3,45. Zeigen Sie rechnerisch, dass der pKS-Wert von Schwefelwasserstoff 6,90 beträgt.
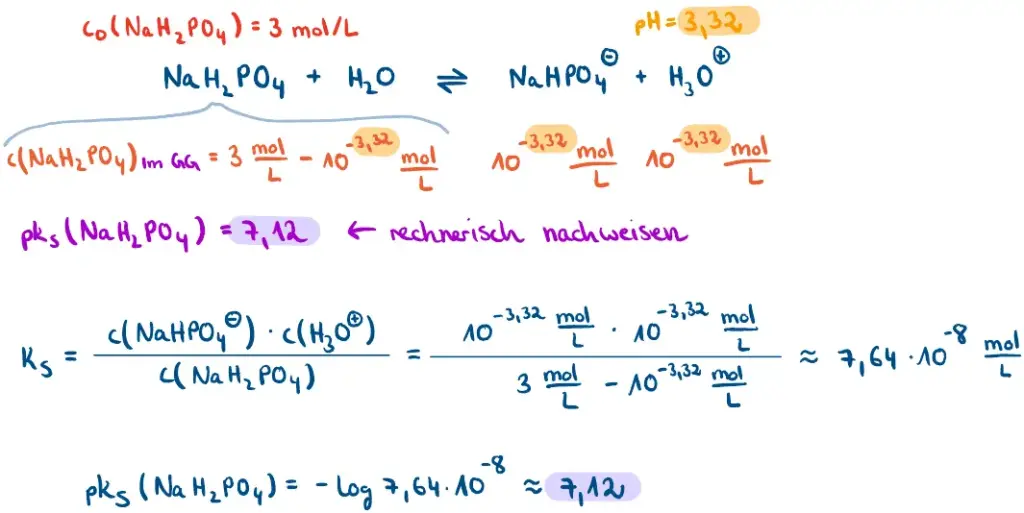
- Gegeben sei eine Natriumdihydrogenphosphat-Lösung mit der Konzentration c0(NaH2PO4) = 3 mol/L und einem pH-Wert von 3,32. Zeigen Sie rechnerisch, dass der pKS-Wert von Natriumdihydrogenphosphat 7,12 beträgt.
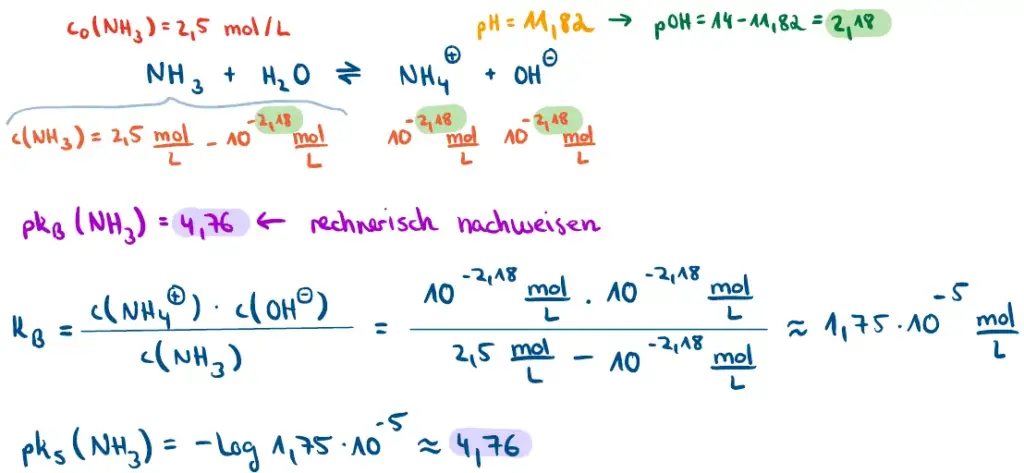
- Gegeben Sei eine Ammoniak-Lösung mit der Konzentration c0(NH3) = 2,5 mol/L und einem pH-Wert von 11,82. Zeigen Sie rechnerisch, dass der pKB-Wert von Ammoniak 4,76 beträgt.
- Gegeben sei eine unbekannte Säure mit der Konzentration c0(HA) = 4 mol/L und einem pH-Wert von 4,40. Berechnen Sie den pKS-Wert und geben Sie an, um welche Säure es sich handelt.
Lösungen