Gibt man etwas Zitronensaft auf Fischfilet, wird der Fischgeruch stark gemildert.
Gibt man dagegen Sodalösung auf Fischfilet, wird er deutlich intensiver. Eine Sodalösung ist eine wässrige Lösung von Natriumcarbonat (Na2CO3), die alkalisch wirkt.
Interessant! Um das erklären zu können, werfen wir einen Blick auf den Verursacher von Fischgeruch: Stickstoffhaltige Stoffwechselprodukte!
Aufgaben
- Erklären Sie unter Zuhilfenahme von M1 die unterschiedliche Basizität von Ammoniak und Harnstoff mit den Unterschieden im Molekülbau.
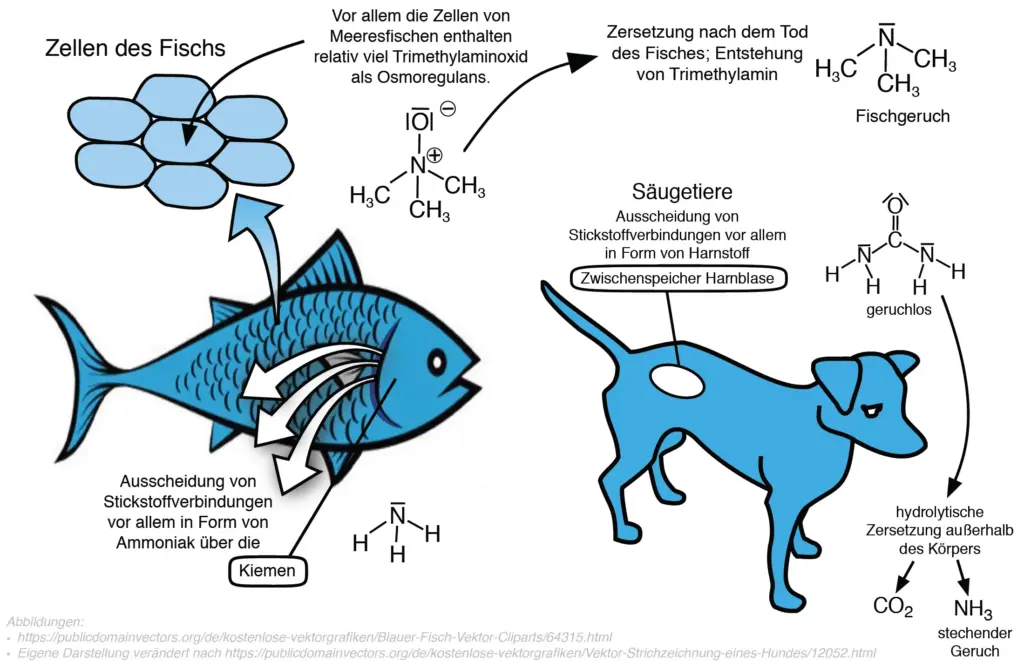
- Erklären Sie unter Zuhilfenahme von M1 den unangenehmen Geruch der Ausscheidungsprodukte von Fischen und Säugetieren.
- Erklären Sie das in der Eingangskonversation beschriebene Phänomen.
- Berechnen Sie mit Hilfe des angegebenen pH-Wertes der 0,1 molaren Trimethylamin-Lösung den pKB-Wert von Trimethylamin.
Stickstoffhaltige Stoffwechselprodukte
Weiteres
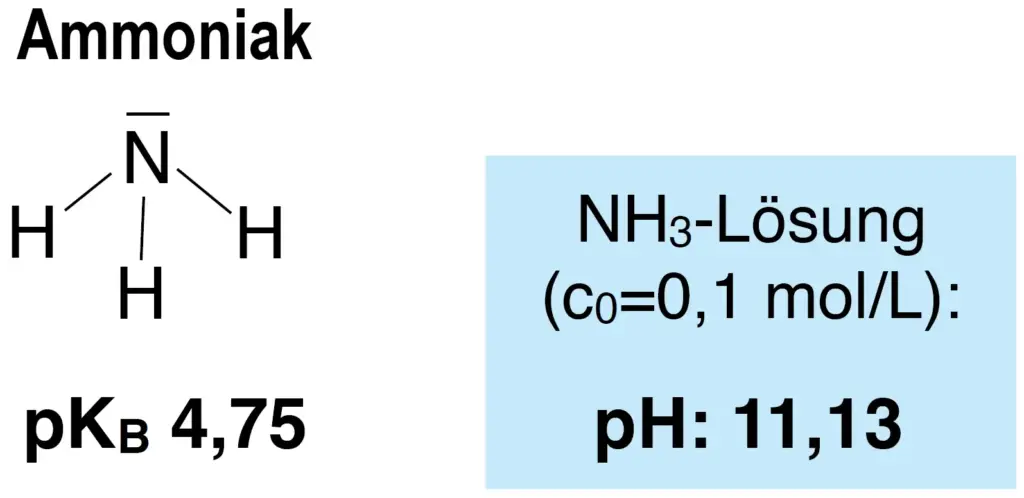
Ammoniak ist das vorwiegende Stickstoff-Ausscheidungsprodukt von Fischen. Fische geben Ammoniak ständig über die Haut oder die Kiemen in das Umgebungswasser ab. Konzentriertere Ammoniak-Lösungen sind ätzend und für ihren intensiv stechenden Salmiak-Geruch bekannt. In der Umgebung der Fische wird der Ammoniak aber sofort verdünnt und ist dann unproblematisch. In reiner Form ist Ammoniak ein Gas, das extrem gut wasserlöslich ist.
Weiteres
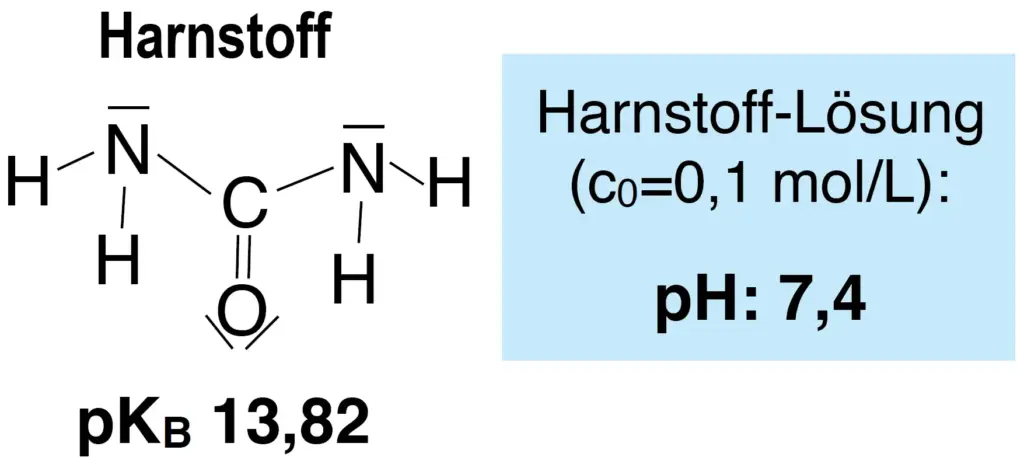
Harnstoff ist in reiner Form ein Feststoff und das vorwiegende Stickstoff-Ausscheidungsprodukt im Urin von landlebenden Säugetieren. Die Zwischenlagerung der Stickstoff-Abfallstoffe in der Harnblase ist nur mit Stoffen möglich, die für den Körper auch in höheren Konzentrationen keine ätzenden Lösungen erzeugen. Dies ist bei Harnstoff gegeben. Der stechende Geruch entsteht erst außerhalb des Körpers, wenn Harnstoff von Mikroorganismen in Ammoniak und CO2 zerlegt wird.
Weiteres
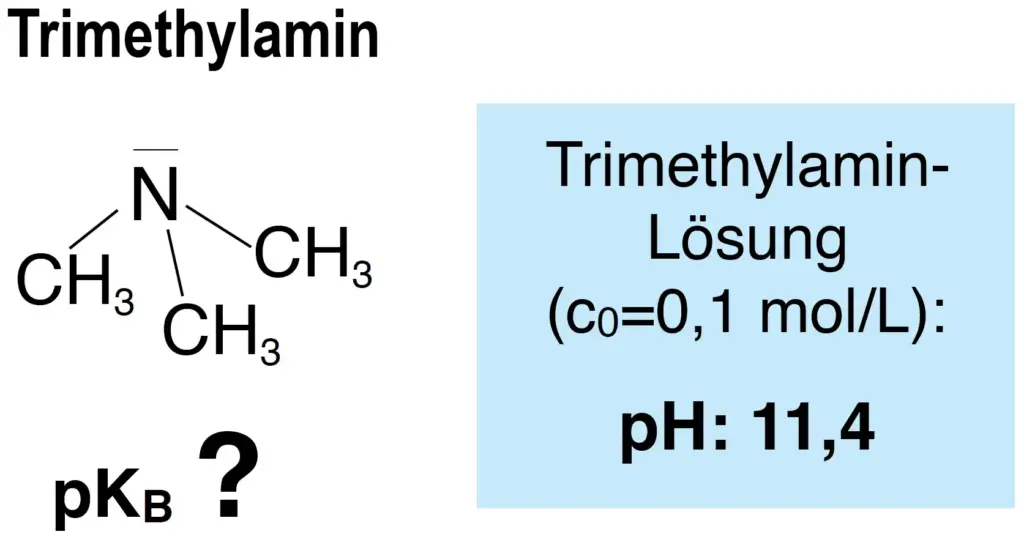
Trimethylamin ist ein Gas, das für den unangenehm stechenden Fischgeruch toter Fische verantwortlich ist. Vor allem das Gewebe von Meeresfischen enthält in größeren Mengen das geruchslose Trimethylaminoxid. Dieses wird bei Zersetzungsprozessen nach dem Tod des Fisches zum unangenehm riechenden Trimethylamin umgesetzt. Verglichen mit Ammoniak-Gas wirkt Trimethylamin-Gas noch aggressiver auf die Schleimhäute.
Weiteres
Stickstoffhaltige Stoffwechselprodukte – Was stinkt denn hier so? 1
Weitergedacht
- Beschreiben Sie den Kurvenverlauf in M2.
- Zeigen Sie rechnerisch mit Hilfe des Massenwirkungsgesetzes, dass bei einem Anteil von 50 % Ammoniak zu 50 % Ammonium pH = pKS bzw. pOH = pKB gilt.
- Zeigen Sie rechnerisch, dass bei einem pH-Wert von 10 85 % Ammoniak und 15 % Ammonium vorliegen.
- Skizzieren Sie einen Kurvenverlauf für Trimethylamin in das Diagramm, den Sie begründen. Falls Ihnen die Berechnung des pKB-Wertes in Aufgabe 4 nicht gelungen ist, erläutern Sie, was sich prinzipiell am Kurvenverlauf im Vergleich zu Ammoniak ändern müsste.
Lösungen
Der pKS-Wert von Ammonium beträgt 9,24. Daraus lässt sich der KS-Wert berechnen. Zudem lässt sich über den angegebenenen pH-Wert von 10 die Oxoniumionen-Konzentration berechnen. Beides lässt sich in die Formel aus Aufgabe 6 einsetzen:
Bei einem pH-Wert von 10 liegt gemäß Formel 3 der Anteil an Ammoniak zu Ammonium bei 5,623 zu 1. Dies lässt sich auch prozentual angeben:
Das Ammoniak/Ammonium-Gleichgewicht
Weiteres
Ammoniak (NH3) hat bei 25 °C einen pKB-Wert von 4,75. Die Lage des Ammoniak/Ammonium-Gleichgewichts bei 25 °C bei verschiedenen pH-Werten zeigt das Diagramm in Abb. 2.
Weiteres
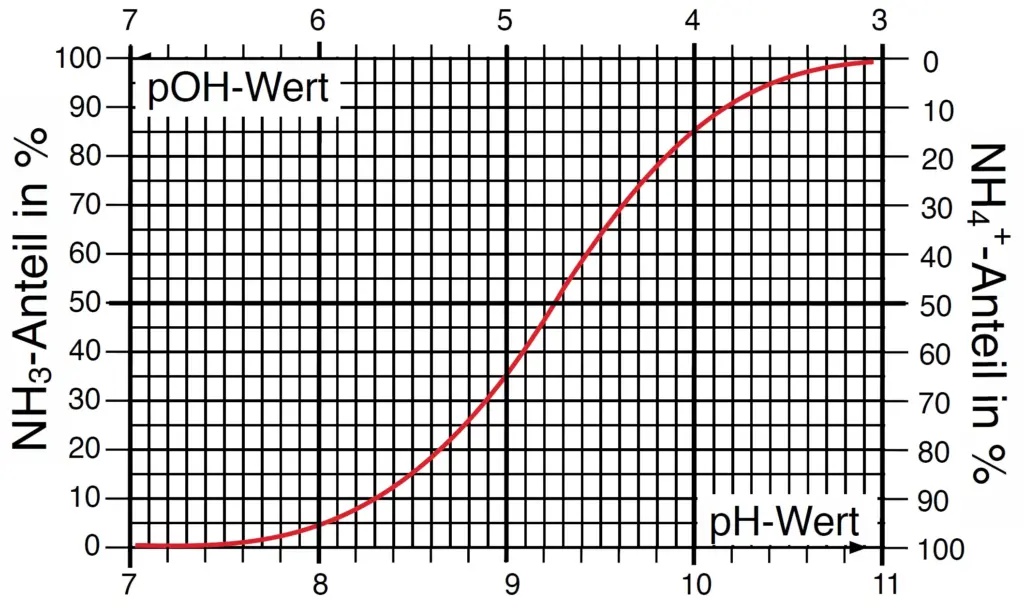
Das NH3/NH4+-Gleichgewicht bei unterschiedlichen pH-Werten.1

