Einstieg
Jean-Pierre, schauen Sie sich das an! Diese kristallklare Langeweile unseres Pools ist passe! Wir verkaufen ab morgen keine Pool-Drinks mehr, sondern Heilbehandlungen. Wir schaffen uns ein eigenes Totes Meer.
Chef, ich habe 18 Tonnen feinstes Speisesalz auf der Kippe. Mein Laster ächzt mehr als ihre Hotelgäste beim Check-out. Aber mal ehrlich: Sind Sie sich sicher, dass das alles da rein passt?
Schütten Sie einfach alles rein! Ich will, dass das Wasser maximal gesättigt ist und unsere Hotelgäste im Wasser liegend Zeitung lesen können, ohne unterzugehen!
Na gut, Sie zahlen, ich kippe! Aber wenn der erste Gast auf dem Salzberg da drin Bergsteigen geht, sagen Sie nicht, ich hätte Sie nicht gewarnt. Achtung, es staubt!
Weiteres
Wie viel Natriumchlorid lösen sich in Wasser?1
Aufgaben
- Führen Sie den Versuch V1 durch und werten Sie ihn aus, indem Sie aus ihren Messwerten das Löslichkeitsprodukt KL von Natriumchlorid berechnen.
- Berechnen Sie, wie viele Kilogramm Salz im Pool gelöst werden können, bis der Pool gesättigt ist und beurteilen Sie, ob Jean-Pierres (Marie-Pierres) Skepsis berechtigt ist. Gehen Sie davon aus, dass der Pool 50 m3 Wasser enthält.
- Welcher Stoff ist für die Trübung der Lösung bei der Titration von Natriumchlorid mit Silbernitrat-Lösung verantwortlich? Formulieren Sie eine Reaktionsgleichung. Erklären Sie die Bildung dieses Stoffes mit Hilfe der Löslichkeitsprodukte.
- Nutzen Sie KI, um sich den Farbumschlag des verwendeten Indikators Fluorescein erklären zu lassen.
Lösungen
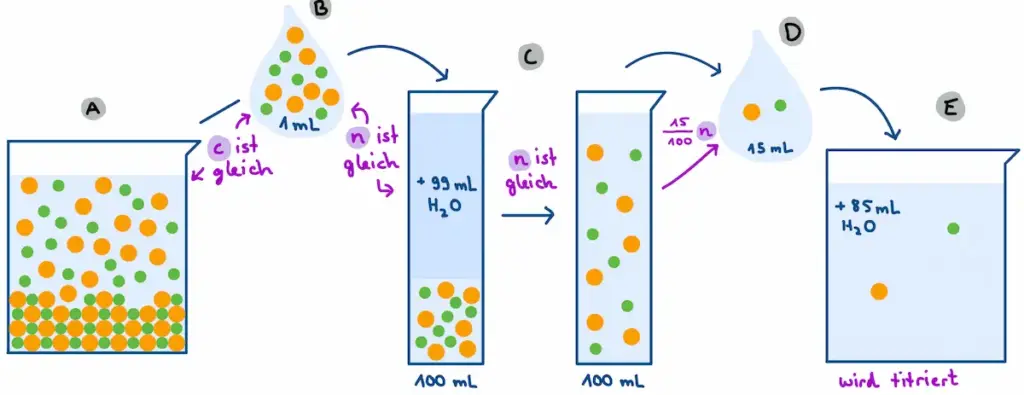
Visualisierung der Verdünnungen auf Teilchenebene.2
Erfahrungsgemäß wird ein Umschlag des Indikators bei ca. 9 mL zugeführter Silbernitrat-Lösung beobachtet. Da die Konzentration der Silbernitrat-Lösung bekannt ist, kann in einem ersten Schritt berechnet werden, wie groß die zugeführte Stoffmenge an Silber-Ionen war. Diese ist äquivalent zur Stoffmenge gelöster Chlorid-Ionen:
D.h. im Becherglas (E) waren folglich 0,0009 mol Chlorid-Teilchen enthalten. Diese Stoffmenge ist gleich der Stoffmenge an Chlorid-Teilchen in den zuvor von der Verdünnung entnommenen 15 mL (D). Die Stoffmenge in (C) lässt sich wie folgt berechnen:
Die berechnete Stoffmenge in (C) ist identisch mit der Stoffmenge in (B). Folglich lässt sich die Konzentration der Ionen in (A) berechnen:
Nun lässt sich das Ionenprodukt berechnen, da die Konzentration an Natrium- und Chlorid-Ionen identisch sind:
Gemäß der Rechnung zu Aufgabe A1 beträgt die Konzentration an gelöstem Natriumchlorid in einer gesättigten Lösung 6 mol/L. Mit diesem Wert lässt sich nun die Stoffmenge für den gesamten Pool berechnen:
Es können ca. 17,5 Tonnen Salz im Pool gelöst werden. Eine einzige LKW-Ladung reicht also aus, um das Wasser im Pool vollständig zu sättigen, es würde sogar ein kleiner Rest ungelöst am Bode liegen bleiben. Die Hotelgäste werden jedoch darauf nicht Bergsteigen können. Die Sorgen des Salzlieferanten/der Salzlieferanten sind also unbegründet. Jedoch muss man bedenken, dass der Berechnung die Wassertemperatur bei der Titration berücksichtigt und nicht die tatsächliche Temperatur im Hotel-Pool.
Versuch
Materialien
- Schutzbrille
- 10 mL Spritze
- 250 mL Bechergläser
- Magnetrührer mit Rührfisch
- Thermometer
- Glasstab
- 100 mL Messkolben
Chemikalien
- Silbernitrat-Lösung 0,1 mol/L
-
Fluorescein-Lösung
- 0,1 g in 100 mL Wasser lösen. Etwas Ethanol unterstützt die Auflösung.
- dest. Wasser
- Natriumchlorid (Kochsalz)
Herstellung der gesättigten Salzlösung
- Die gesättigte Salzlösung am besten am Vortag vorbereiten.
- 100 mL dest. Wasser in ein Becherglas füllen.
- 40 g Natriumchlorid unter ständigem Rühren löffelweise hinzugeben, bis ein deutlicher Bodensatz bestehen bleibt.
- Die Lösung für mindestens 10 Minuten mit Hilfe eines Magnetrühers rühren.
- Die Temperatur der gesättigten Lösung messen und notieren.
- Das Rührwerk ausschalten und warten, bis sich der Bodensatz vollständig abgesetzt hat.
Probenvorbereitung
- 1 mL der klaren, überstehenden Natriumchlorid-Lösung entnehmen.
- Die Probe in einen 100 mL Messkolben geben.
- Den Messkolben mit dest. Wasser bis zur Eichmarke auffüllen.
- Mit einem Glasstab vorsichtig rühren (homogenisieren).
Durchführung (Titration nach Fajans)
- Eine 10 mL Spritze mit Silbernitrat-Lösung befüllen.
- 15 mL der verdünnten Natriumchlorid-Lösung aus dem Messkolben in ein Becherglas pipettieren und auf 100 mL mit dest. Wasser auffüllen.
- 5 Tropfen Fluorescein-Indikatorlösung hinzugeben.
- Unter ständigem Schwenken portionsweise mit Silbernitrat-Lösung titrieren.
- Die Titration ist beendet, wenn die Lösung eine milchige, pfirsisch-orangene/lachsrote Färbung annimmt.
- Den Verbrauch an Silbernitrat notieren.
Entsorgung
- Alle Lösungen, die Silber-Ionen enthalten, werden im Behälter für Schwermetall-Abfälle gesammelt.
- Die Kochsalz-Lösungen ohne Silber-Ionen können über den Abguss entsorgt werden.
Hinweise zur Beobachtung
- Achten Sie darauf, dass bei der Entnahme der gesättigten Lösung kein fester Bodensatz in die Pipette gelangt.
- Der Farbumschlag bei der Titration ist sehr scharf, findet aber an den Feststoffpartikeln statt, nicht in der klaren Flüssigkeit.
- Die Lösung sollte während der Titration nicht im direkten Sonnenlicht stehen, da Silbersalze lichtempfindlich sind.
Salzgehalt in Kochbrühe
Weiteres
Das Prinzip der Fällungstitration lässt sich auch zur Analyse von Lebensmitteln einsetzen. In einer Lebensmittelkontrolle soll der Salzgehalt einer flüssigen Kochbrühe bestimmt werden.
10 mL der Kochbrühe wurden ohne weitere Verdünnung mit Silbernitrat-Lösung der Konzentration 0,1 mol/L nach Fajans titriert. Der Umschlag erfolgte bei einem Verbrauch von 12,5 mL.
Weiteres
Argentometrische Titration einer Kochsuppe.3
Weiteres
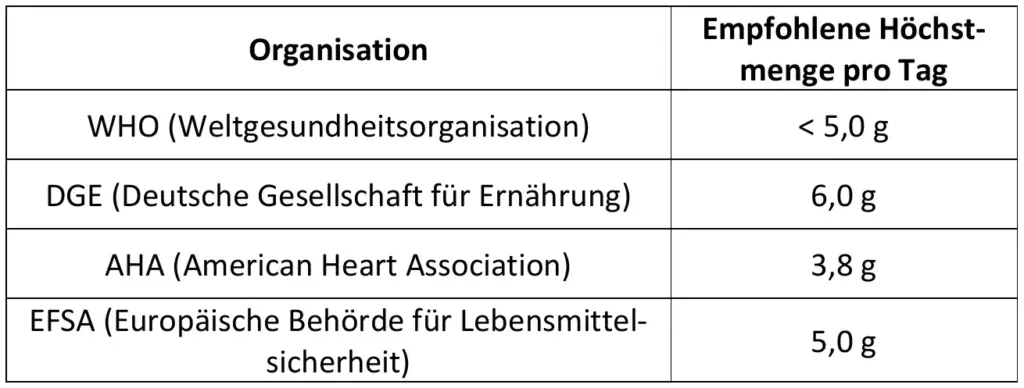
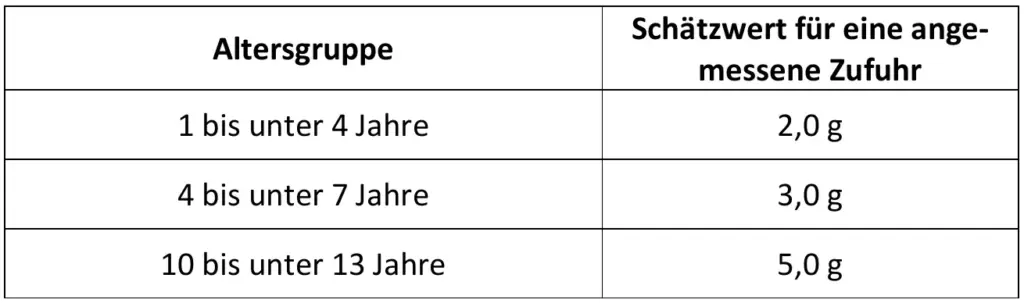
Empfehlungen zur maximalen täglichen Speisesalzzufuhr. Erwachsene und Kinder. Die Werte für Kinder stammen von der DGE. Die Empfehlungen der AHA und der WHO beziehen sich in den Originalquellen primär auf die Aufnahme von Natrium. Für diese Tabelle wurden die Werte in die entsprechende Menge Speisesalz (NaCl) umgerechnet. 4567
Anwendung & Übung
- Berechnen Sie die Masse an Natriumchlorid, die in einem Liter der in M2 genannten Brühe enthalten sind (Angabe in g/L).
- Beurteilen Sie, ob die Brühe den physiologischen Richtwert gemäß Tabelle 1 überschreitet, wenn eine Portion aus 250 mL Kochbrühe besteht.
- Berechnen Sie, welchen Prozentsatz der maximalen Tagesdosis nach DGE-Empfehlung ein Erwachsener oder ein Kind (7 Jahre) mit einer Portion deckt. Beurteilen Sie das Produkt kritisch in Hinblick auf die Ernährung.
- Geben Sie Szenarien an, in denen die Titrationsmethode nach Fajans an ihre Grenzen stößt.