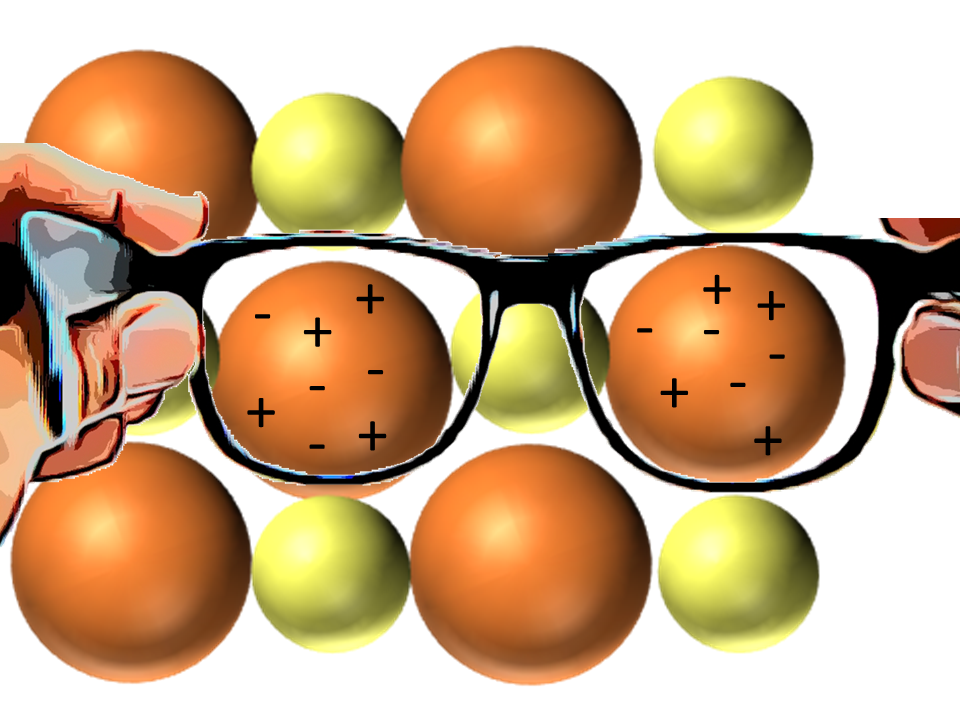
Wir setzen erneut unsere Modellbrille auf
Atome besitzen innere Bausteinen
Daltons Atommodell konnte die Massenerhaltung bei chemischen Reaktionen plausibel erklären. Zur Erklärung der von Dmitri Mendelejew 1869 erkannten Periodizität der Elemente war es jedoch keine Hilfe.
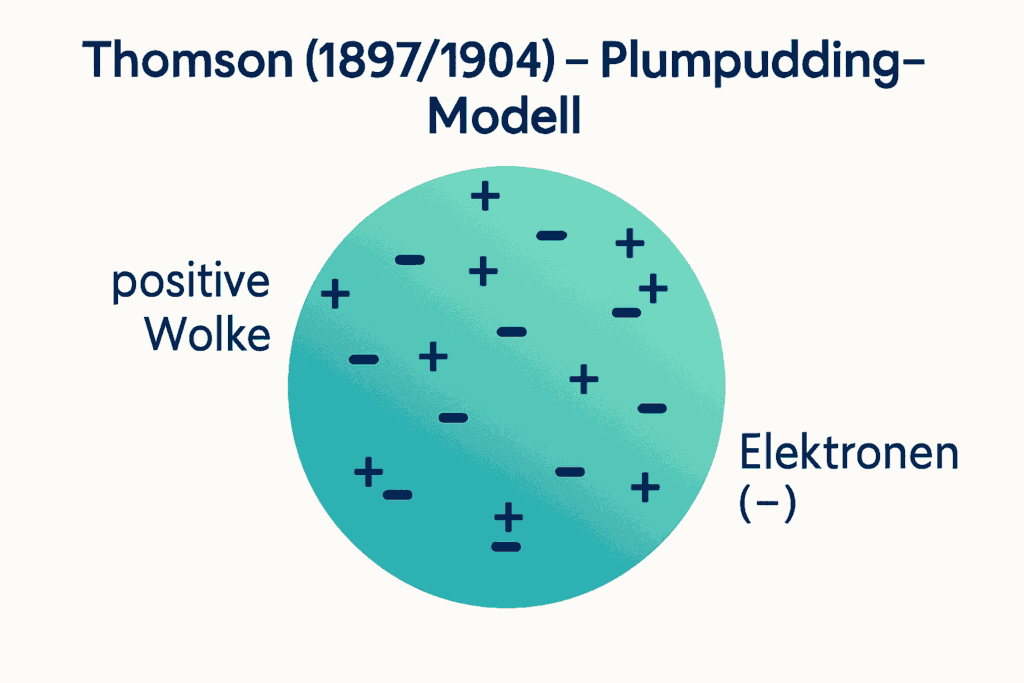
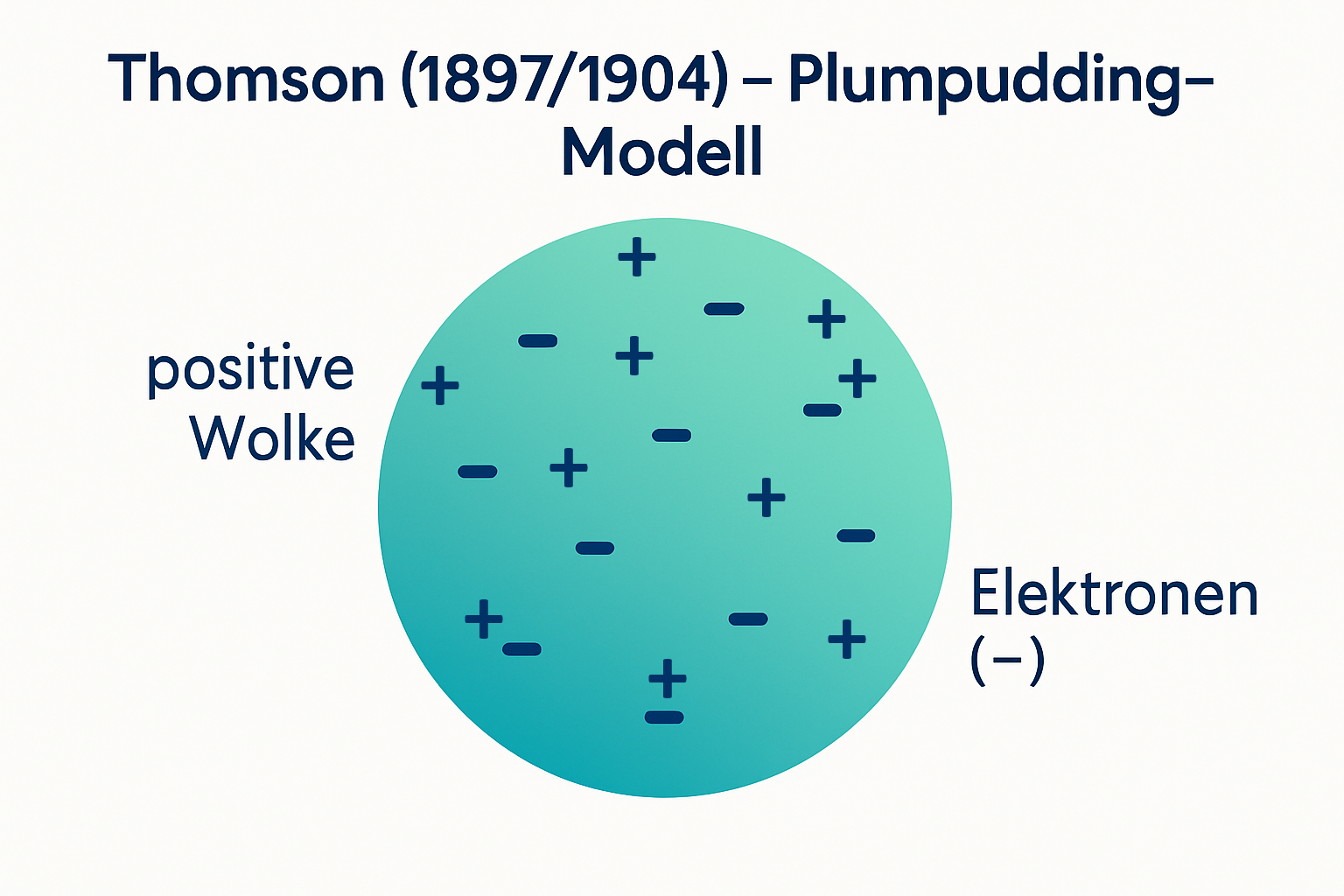
Um die Wende zum 20. Jahrhundert gewannen die Forschungen zum Atombau rasant an Fahrt: 1897 wies J. J. Thomson das Elektron als negativ geladenen Bestandteil aller Atome nach. 1904 schlug er das „Rosinenkuchen-“ bzw. „Plumpudding-Modell“ vor. Dieses Atommodell erklärte die Periodizität zwar auch nicht. Es war aber ein wichtiger Meilenstein für den Blick ins Innere der Atome. Deshalb betrachten wir es hier kurz einmal näher.
Ein erneuter Blick durch unsere Modellbrille
Unsere Modellvorstellungen werden „feiner“.1
Aufgaben
- Erkläre mit eigenen Worten, warum Daltons Kugelmodell die von Mendelejew erkannte Periodizität der Elemente nicht erklären kann. Benenne dazu noch einmal, worauf der Gedanke der Periodizität beruht.
- Führe V1 durch und protokolliere deine Beobachtungen ohne Fachbegriffe (makroskopisch).
- Nutze Thomsons Plumpudding-Modell aus Galerie 1 in M1, um modellhaft zu erklären, wie die in V1 beobachteten Anziehungs‑ oder Abstoßungsphänomene zustande kommen können. Erstelle eine beschriftete Skizze dazu.
- Erkläre basierend auf den heutigen Erkenntnissen die Aussage der Überschrift und der Unterüberschrift dieser Seite.
Anregungen
Alternativversuch zu V1: Puste zwei Luftballons auf und binde je einen an eine Schnur. Reibe die Ballons an deinen Haaren. Ziehe die Ballons nach oben weg. Halte sie danach an den Schnüren und versuche sie zusammen zu bringen.
Gegensätzliche Ladungen ziehen sich an, gleichnamige Ladungen stoßen sich ab.
Mögliche Satzstarter
- Beobachtung (makroskopisch, ohne Fachbegriffe): „Ich beobachte, dass …“
- Übergang: „Diese Beobachtung deute ich modellhaft so: …“
- Deutung mit Thomson (submikroskopisch/fachsprachlich): „Nach dem Plumpudding-/Rosinenkuchen‑Modell …“—
Wortfeld Makro vs. Modell
Makro (Alltagsbegriffe): anziehen, abstoßen, aufrichten, wegstehen, haften, nähern, entfernen, stärker/schwächer, sofort/langsam
Modell (Fachbegriffe): Elektronenübertragung, Ladungsüberschuss/-defizit, „positive Grundmasse“ (positive Wolke), gleichnamige/ungleichnamige Ladungen
Wir reiben Folien an Papier
Materialien
- Papier
- Schere
- Klarsichtfolie
Chemikalien
- keine
Aufbau
Schneide aus einer Klarsichtfolie wie abgebildet ein ca. 10cm x 10cm großes Stück heraus.
Durchführung
- Reibe etwa 20 Sekunden kräftig mit einem Stück Papier zwischen beiden Seiten der Klarsichtfolie. Ziehe das Papier dann langsam nach unten zwischen den Folienstreifen heraus.
- Hebe die Klarsichtfolie an der Lochseite hoch und beobachte, wie sich die beiden Plastikstreifen zueinander verhalten.
- Versuche das Papier wieder zwischen die Folienstücke zu führen und beobachte erneut.
Weitergedacht
- Betrachte das Video in M2. Stelle eine Vermutung auf, was dort passiert sein könnte.
- Wenn Du magst, kannst Du über den Unterricht hinaus ein wenig tiefer in die Forschungsgeschichte zum Atombau eindringen. Nutze dazu gerne als Aufgangspunkt die Informationen in M3
Feuer an der Tankstelle
Weiteres
Für alle, die es genauer recherchieren wollen
Wie es weiter gehen wird
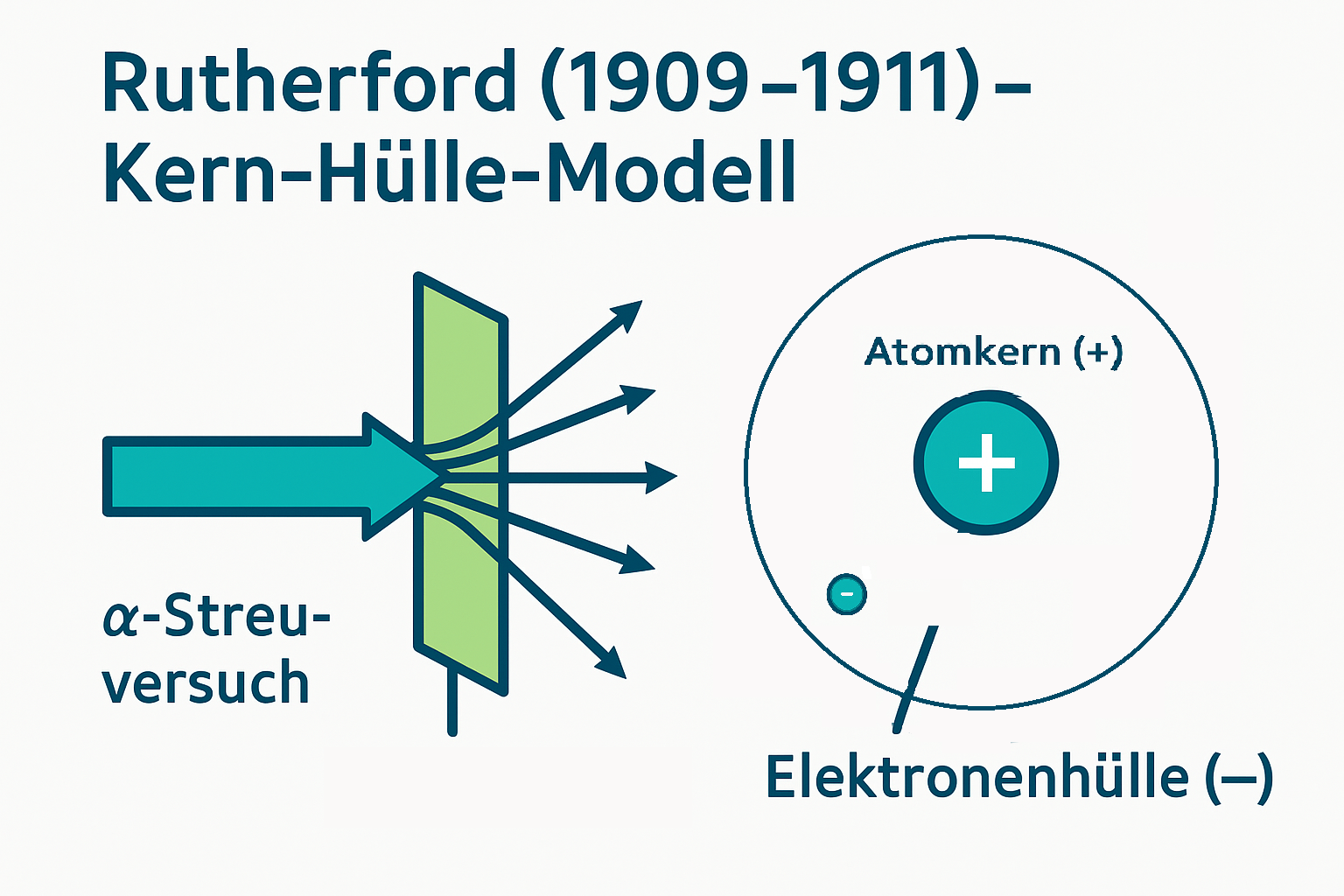
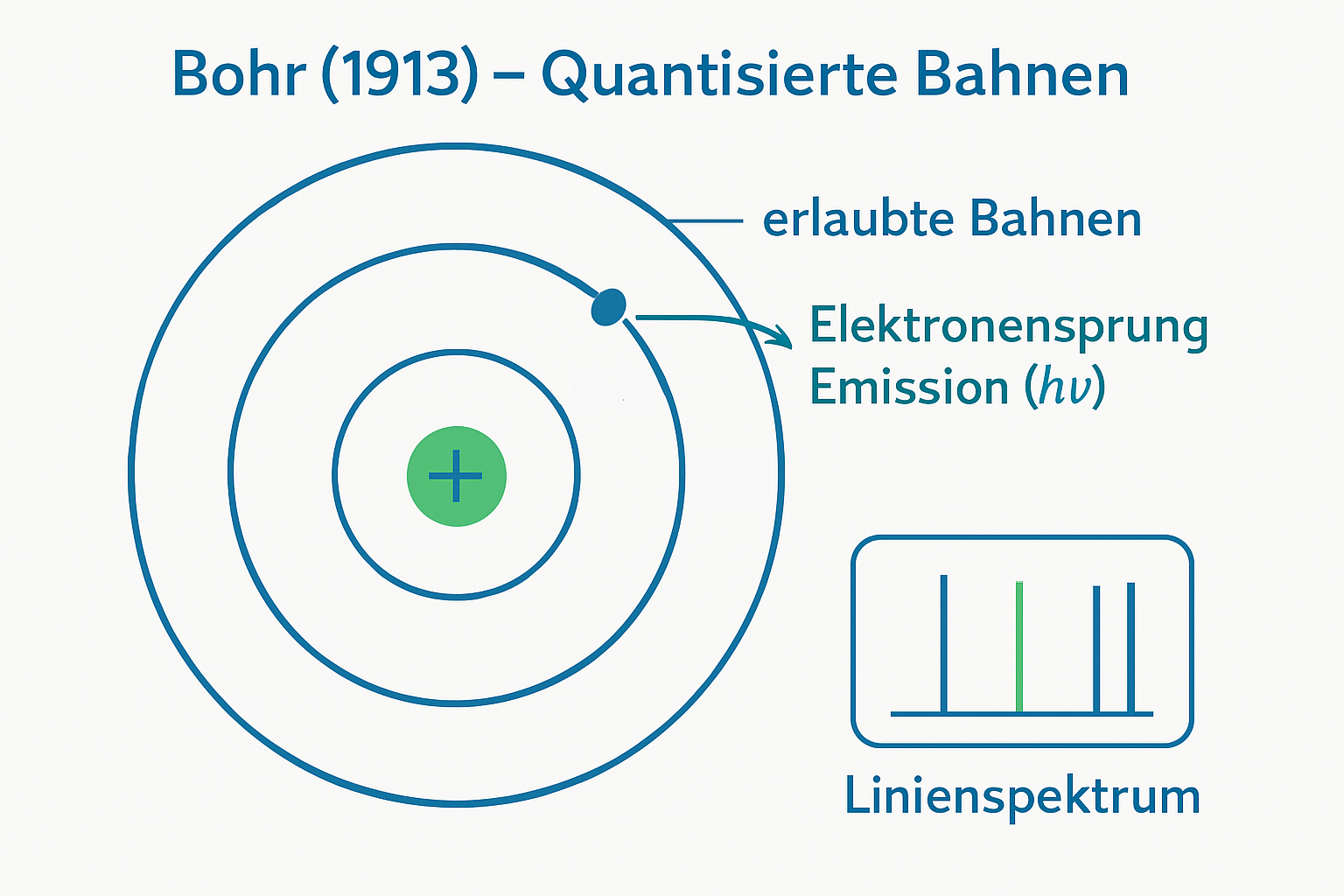
Kurz darauf führten Streuversuche (Ernest Rutherford, Hans Geiger, Ernest Marsden, 1909–1911) zum Kern‑Hülle‑Modell, auf dem 1913 Niels Bohr mit seinem Schalenmodell aufbaute. Diese Entwicklung werden wir in den nächsten Schritten aufgreifen.
Die Modelle stark vereinfacht dargestellt.1
Eine kleine Detektivgeschichte des Atoms geordnet nach den Forschenden
Die Idee, dass Elemente „periodisch“ angeordnet sind, kam lange vor dem modernen Atombild. Dmitri Mendelejew ordnete 1869 die Elemente nach ihren Eigenschaften und Atommassen – mit Lücken für noch Unbekanntes. Erst Henry Moseley zeigte 1913 mit Röntgenspektren, dass die Ordnungszahl (die positive Kernladung) die wahre Reihenfolge im Periodensystem bestimmt. Damit bekam die Periodizität ein physikalisches Fundament.
Der erste geladene Baustein, den man direkt nachwies, war das Elektron. In Gasentladungsröhren wurden „Kathodenstrahlen“ beobachtet, die sich in elektrischen und magnetischen Feldern ablenken ließen. J. J. Thomson zeigte 1897, dass diese Strahlen aus sehr leichten, negativ geladenen Teilchen bestehen – den Elektronen – und dass sie unabhängig vom verwendeten Gas oder den Elektrodenmaterialien entstehen: Elektronen gehören zu allen Atomen. Millikan bestimmte 1909–1911 die Elementarladung so genau, dass sich daraus die winzige Elektronenmasse ergab.
Parallel untersuchte man die „Gegenrichtung“: Eugen Goldstein sah 1886 in besonderen Röhren positiv geladene „Kanalstrahlen“. Wilhelm Wien und andere zeigten, dass es sich dabei um positiv geladene Ionen handelt – deutlich massereicher als Elektronen. Doch wo sitzt diese positive Ladung im Atom?
Die Antwort brachte Rutherfords berühmter Streuversuch (1909–1911): Wenn man Alpha-Teilchen auf dünne Goldfolie schießt, werden einige stark zurückgestreut. Das ist nur möglich, wenn fast die gesamte Masse und die positive Ladung in einem winzigen Zentrum konzentriert sind – dem Atomkern. Bei Kernreaktionen (1917–1919) beobachtete Rutherford, dass Wasserstoffkerne herausgeschlagen werden; 1920 prägte er für diesen positiven Kernbaustein den Namen Proton.
Es blieb ein Rätsel: Viele Atome waren schwerer, als „Protonen plus Elektronen“ erlaubten, und es gab Isotope – gleiche Elemente mit unterschiedlicher Masse. James Chadwick löste 1932 das Puzzle. Er zeigte, dass beim Beschuss von Beryllium eine neutrale, sehr durchdringende Strahlung entsteht, die aus ungeladenen Teilchen mit nahezu Protonenmasse besteht: den Neutronen. Damit war das Bild komplett.
Hilfe bei Fachtexten
Du verstehst einen Fachtext nicht vollständig?
Vom Periodensystem zum Atombau – Stichworte
- Periodizität (1869–1913): Mendelejew ordnete die Elemente nach wiederkehrenden Eigenschaften und sagte sogar neue voraus. Manche „Ausreißer“ (z. B. Iod/Tellur) blieben rätselhaft – bis Moseley 1913 zeigte: Entscheidend ist die Ordnungszahl (Anzahl positiver Ladungen im Kern), nicht die Atommasse. Der Platz im Periodensystem spiegelt also die Kernladung wider.
- Elektron (ab 1897): In Entladungsröhren erkannte man ablenkbare Strahlen. Thomson bestimmte 1897 das Verhältnis „Ladung/Masse“ und bewies: Das Elektron ist ein universeller, negativ geladener und extrem leichter Baustein aller Atome. Millikan (1909–1911) maß die Elementarladung und bestätigte die winzige Masse.
- Kern (1909–1911): Das „Rosinenkuchen“-Modell (Ladung gleichmäßig verteilt) scheiterte am Goldfolienversuch von Geiger, Marsden und Rutherford. Einige Alpha-Teilchen prallten stark zurück – ein Hinweis auf einen sehr kleinen, massereichen, positiv geladenen Kern. Damit entstand das Kern–Hülle-Modell: winziger Kern, weite Elektronenhülle.
- Proton (1917–1920): Es gibt eine positive Ladung im Kern – aber in welcher Form? Goldsteins Kanalstrahlen hatten schon positive Teilchen gezeigt. Rutherford beobachtete bei Kernreaktionen von Stickstoffatomen mit Alpha-Teilchen, dass Wasserstoffkerne freigesetzt werden. Er deutete sie als elementare positive Kernbausteine und nannte sie 1920 „Protonen“.
- Neutron (1932): Isotope (gleiches Element, andere Masse) und „fehlende“ Masse verrieten: Im Kern muss noch etwas sein. Chadwick wies durch Beryllium-Experimente ein ungeladenes Teilchen mit fast Protonenmasse nach – das Neutron. Es erklärt die Kernstabilität und die Existenz von Isotopen.
- Warum das alles später das PSE erklärt:
Die Anzahl der Protonen = Ordnungszahl = Position im PSE.
Die Elektronenverteilung (Außenelektronen) bestimmt die chemischen Eigenschaften und damit die Familienähnlichkeiten.
Neutronen variieren die Masse, ohne die Ordnungszahl zu ändern – so entstehen Isotope. - Ein Blick weiter: Das Bohrsche Schalenmodell (1913) ordnete die Elektronen in Energieniveaus und uns interessiert eigentlich nur die äußerste Schale. Moderne Modelle gehen darüber hinaus. Für uns und den Chemieunterricht bleibt aber: die Periodizität ist Ausdruck des Elektronenaufbaus im Atom. Und der ist wiederum festgelegt durch die Kernladung. Aus Mendelejews Ordnung wurde mit Elektron, Proton und Neutron ein stimmiges Bild: Der Kern (Protonen + Neutronen) definiert die Identität und Masse, die Elektronenhülle bestimmt die Art der Bindungen und damit die Chemie.