Zeit für eine Zwischenübersicht
Atombausteine
Rutherfords Versuch und weitere Versuche zeigten:
- Atome bestehen aus einem sehr kleinen, massereichen Kern und einer vergleichsweise großen Hülle.
- In der Atomhülle bewegen sich Elektronen mit negativer Ladung. Im Atomkern befinden sich positiv geladene Protonen.
- Da Atome neutral sind, muss es in einem Atom immer gleich viele Elektronen und Protonen geben.
Im Jahr 1932 wurde noch ein weiterer Baustein des Atoms entdeckt: das Neutron. Neutronen befinden sich ebenfalls im Atomkern. Ein Neutron hat eine ähnlich große Masse wie das Proton aber keine Ladung.
Zwischen Neutronen und Protonen gibt es auf sehr kurze Distanz eine Anziehungskraft, die sogenannte starke Wechselwirkung.
Die starke Wechselwirkung ist dafür verantwortlich, dass ein Kern überhaupt stabil sein kann, denn die elektrostatische Abstoßung zwischen den Protonen würde sonst einen Kern auseinander fliegen lassen.
Eine Übersicht
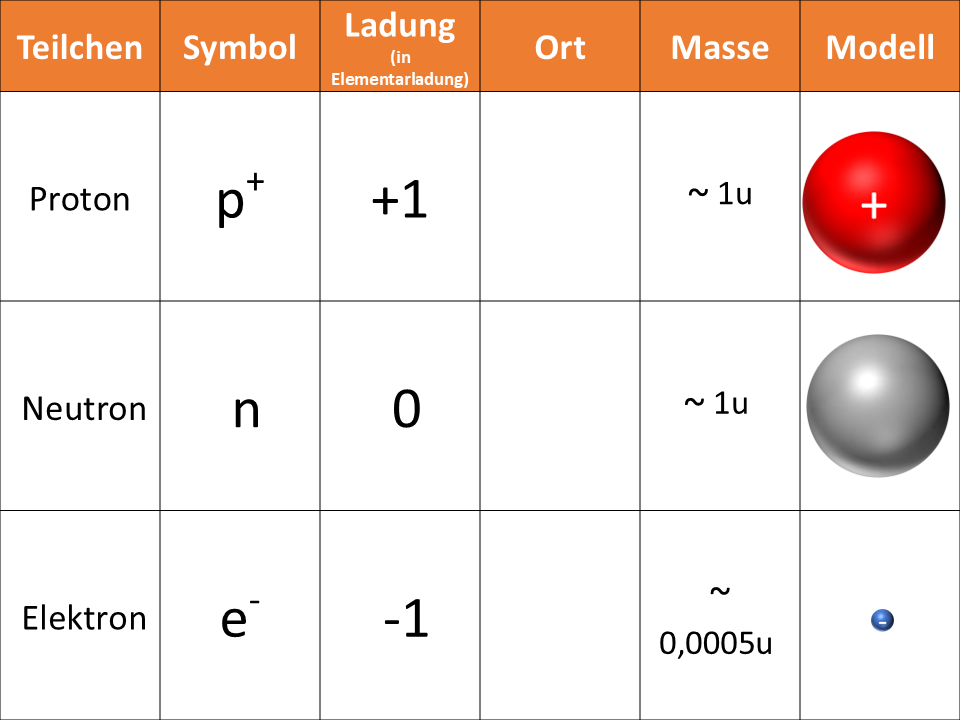
Bausteine eines Atoms.1
Neutron und Proton wiegen jeweils ca. 1u, aber Elektronen sind viel leichter. Sie wiegen nur ca. 0,005 u. Über die Größenverhältnisse haben wir bereits gesprochen.
Denke einmal über Folgendes nach: Wir bekommen in der Schule an der Tafel ein „Abbildungsproblem der Größen“ beim gleichzeitigen Darstellen von Kern und Hülle.
Aufgaben
- Lies M1, lade dir Tab. 1 herunter und fülle sie aus.
- Lies M2, lade dir Tab. 2 herunter und fülle auch sie aus.
- Schreibe zu allen Sprechblasen mit einem besonderen Icon (Fragezeichen oder Glühbirne) einen kurzen Abschnitt, der auf den Gedanken in der Sprechblase eingeht oder die Frage beantwortet.
Der Atombau und das Periodensystem - Teil eins: der Kern
Ein Blick in das Periodensystem
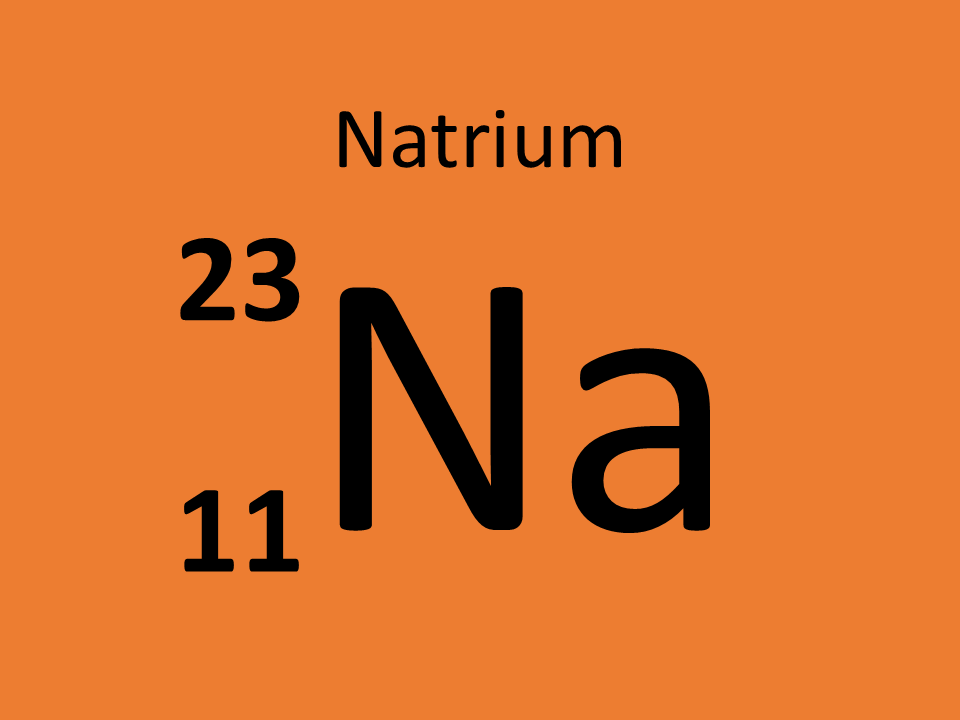
Ordnungszahl und Massenzahl.1
Die Ordnungszahl
Bisher haben wir gesagt: Alle Elemente bestehen aus einer Sorte Atome.
Das kann man etwas genauer sagen: Die Atome eines Elements haben immer die gleiche Anzahl an Protonen. Beispielweise haben Wasserstoffatome 1 Proton, alle Heliumatome 2 Protonen, …, und so weiter.
Die Elemente sind dadurch „geordnet“, man nennt diese Zahl die Ordnungszahl. Die Ordnungszahl Z, also die Zahl der Protonen, ist in der Regel im Periodensystem unten links am Elementsymbol angegeben.
Denke einmal über Folgendes nach: Warum wird man kein Element mehr entdecken, das im Periodensystem zwischen Wasserstoff und Helium stehen wird?
Warum kann man sagen, dass die Ordnungszahl nicht nur die Anzahl der Protonen, sondern auch die Anzahl der Elektronen angibt?
Die Massenzahl
Die Masse eines Atoms wird näherungsweise durch die Protonen und Neutronen zusammen gebildet. Im Periodensystem steht die Masse oft als Massenzahl A links oben am Elementsymbol. Ein Natriumatom wiegt beispielsweise 23u.
Kennt man die Anzahl der Protonen (durch die Ordnungszahl) und die Atommasse (über die Massenzahl) kann man sehr leicht ausrechnen, wie viele Neutronen im Atom vorhanden sind. Beispiel: Ein Natriumatom wiegt 23u. Es hat 11 Protonen, die zusammen 11u wiegen. Die restliche Atommasse von 12u muss durch die Neutronen zustande kommen. Da jedes Neutron 1u wiegt, müssen in einem Natriumatom also auch 12 Neutronen sein.
Erkläre kurz: Warum beeinflussen Elektronen die Massenzahl praktisch nicht?
Hast Du schon eine Idee, warum ein Telluratom im Mittel schwerer als ein Iodatom ist, obwohl Tellur die kleinere Ordnungszahl hat?
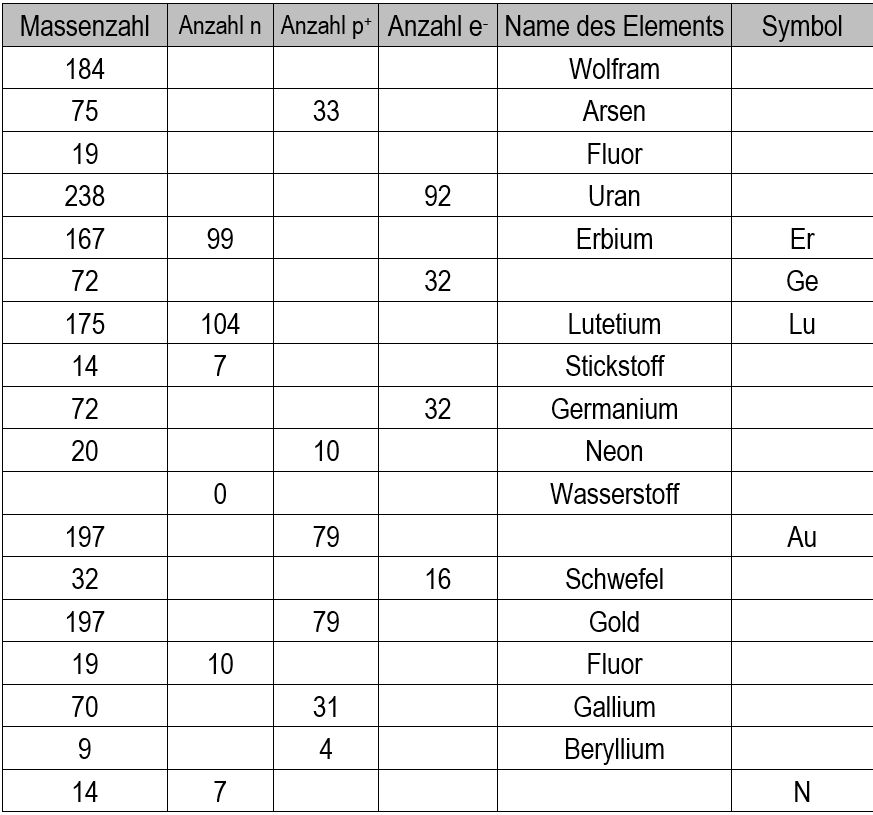
Eine Übung
Vorlage zum Ausfüllen.2
Isotope
Warum muss man sich die Anzahl der Neutronen immer so umständlich ausrechnen?
Man könnte doch neben das Elementsymbol im Periodensystem einfach auch schreiben, wie viele Neutronen bei diesem Element im Kern sind.
Das geht leider nicht immer. Beim Natrium wäre es einfach. Denn alle Natriumatome wiegen 23u. Aber schau einmal genau hin. Ein Boratom wiegt im Mittel 10,8u. Wie soll das gehen? Neutronen wiegen 1u, Protonen auch! Und so viele Elektronen sind nicht in einem Boratom!
Es ist ganz einfach: auf der Erde gibt es zwei Sorten von Boratomen. Eine Sorte hat 5 Protonen und 5 Neutronen und eine Sorte hat 5 Protonen und 6 Neutronen. Die einen Boratome wiegen 10u, die anderen 11u. Beide Atomsorten sind Boratome, denn sie enthalten 5 Protonen im Kern.
Man sagt: es gibt zwei Isotope von Bor. Da auf der Erde etwa 20% der Boratome 10u wiegen und etwa 80% der Boratome 11u wiegen, wiegt ein Boratom durchschnittlich 10,8u.
Von manchen Elementen gibt es sogar noch mehr Isotope. Kohlenstoffatome gibt es in drei Formen:
Was bedeutet das?
Und kannst Du mit einem Periodensystem im Internet herausfinden und benennen, welches der Isotope auf der Erde das häufigste ist?