Aufgaben
- Fassen Sie die wesentlichen Aussagen von M1 und M2 mündlich zusammen.
- Formulieren Sie wiederholend, was unter den Fachbegriffen Oxidation und Reduktion zu verstehen ist.
- Prüfen Sie für sich, ob Sie bei Ansicht der Reaktionsgleichung erkennen könnten, dass es sich bei der Umwandlung von Ethanol zu Ethanal um einen oxidativen Abbau handelt.
Ethanal, ein Oxidationsprodukt?
Risiken durch Ethanol und seine Abbauprodukte
Seit einiger Zeit gibt es ein Positionspapier der Deutschen Gesellschaft für Ernährung (DGE), in welchem sie betont, dass es keine sichere oder gesundheitsfördernde Menge an Alkohol gibt. Die Empfehlung lautet, grundsätzlich auf Alkohol zu verzichten.
Dort steht: „Der Konsum alkoholischer Getränke ist ein führender Risikofaktor für eine Vielzahl von Erkrankungen und vorzeitigen Tod […]. Die psychoaktiven und schädlichen Auswirkungen alkoholischer Getränke werden zum größten Teil dem darin enthaltenen Ethanol […] bzw. seinen im Körper entstehenden Abbauprodukten, insbesondere Acetaldehyd (Ethanal), zugeschrieben.“ 2
Dass Ethanol gefährlich ist, wusste ich. Aber was ist Ethanal? Und wie entsteht das im Körper?
Laut Fachleuten entsteht es durch Oxidation. Im Ethanal sehen einige Wissenschaftler den eigentlichen Verursacher des sogenannten Katers, also Übelkeit, Erbrechen, hämmernde Kopfschmerzen etc.3
Bisher Bekanntes und Unbekanntes zur Oxidation
Oxidationen und auch Redoxreaktionen kennen wir bereits aus einem anderen Zusammenhang, z. B. der Elektrochemie.
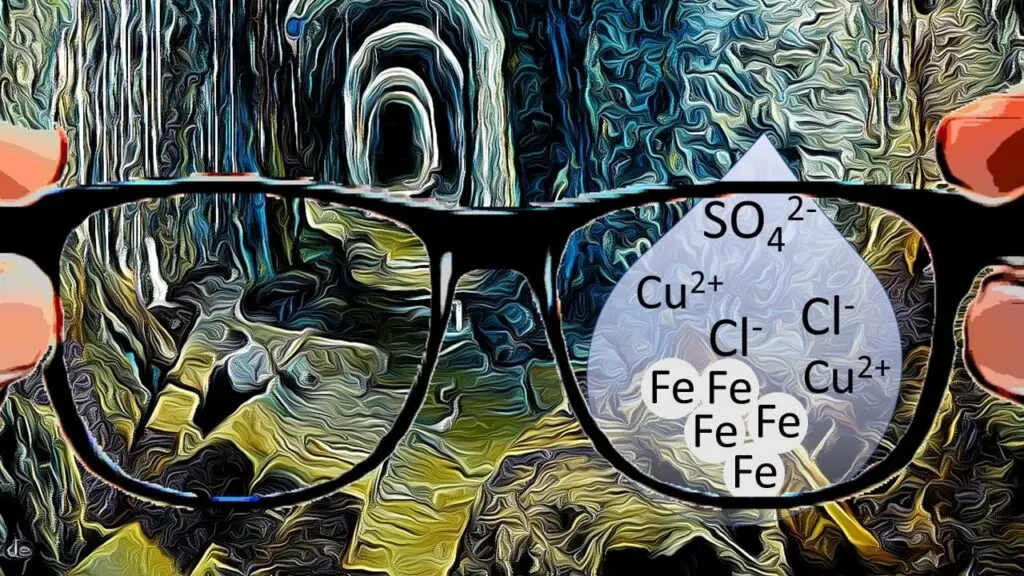
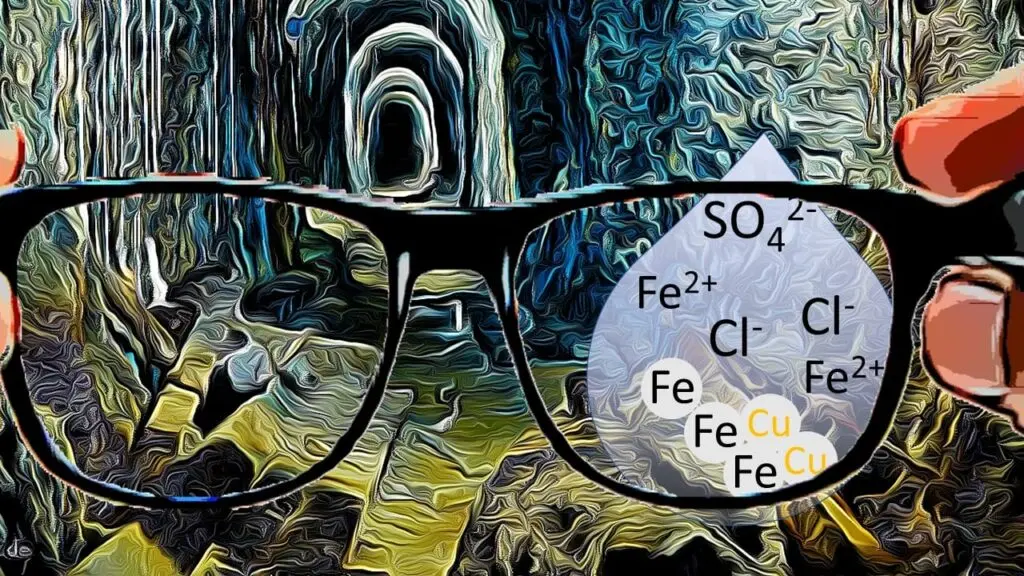
Redoxreaktionen an einer Eisenleiter in einer Kupfermine.4
Bei Redoxreaktionen, an denen Ionen beteiligt sind, ist der Elektronenaustausch relativ leicht zu erkennen, denn da kann man die Zahl der abgegebenen bzw. aufgenommenen Elektronen direkt aus der Ladung der einzelnen Ionen ablesen.
Redoxreaktionen, also ein Elektronenaustausch, gibt es auch zwischen Molekülen.
Aber wie kann man hier Oxidation und Reduktion erkennen?
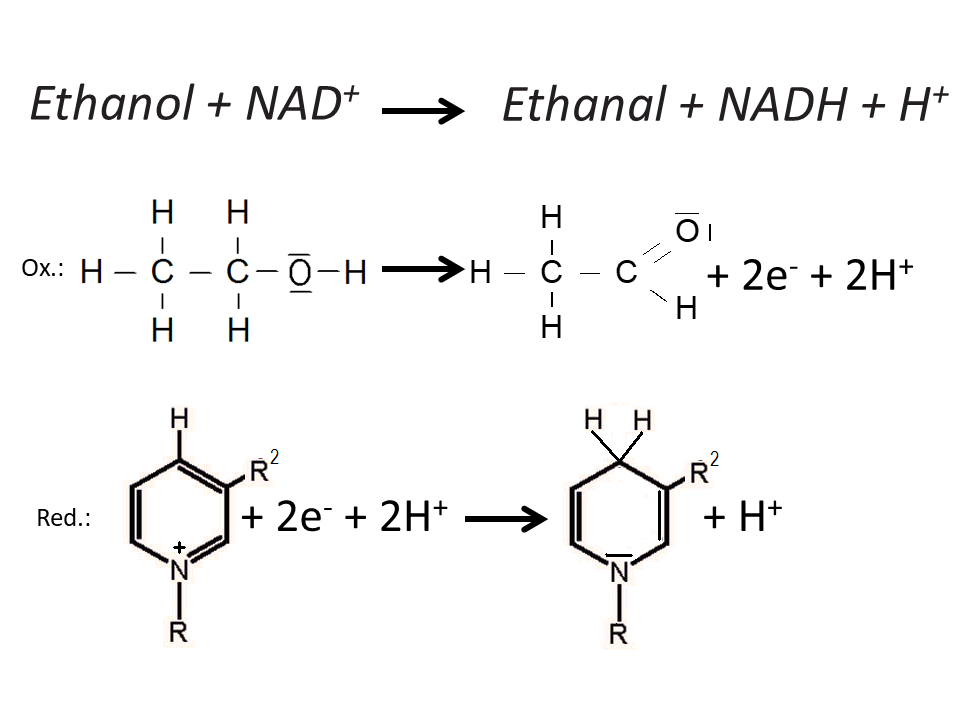
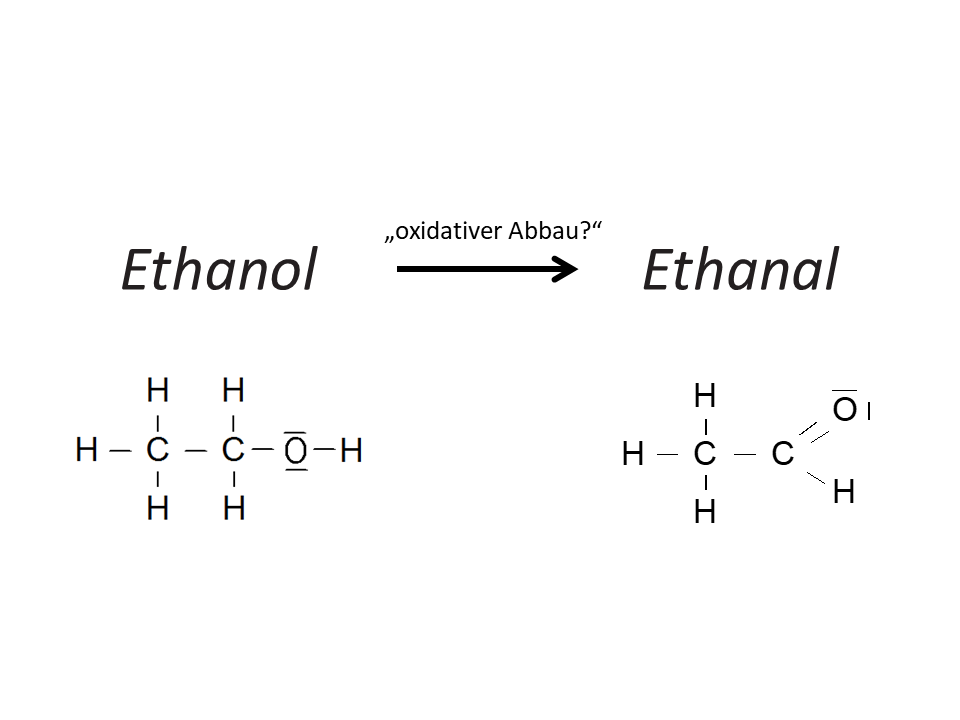
Reaktionsgleichungen zur Redoxreaktion im Körper.5
Was können wir schon erklären?
- In M2 wird von zwei Versuchen gesprochen. Notieren Sie nach Ansicht des Videos und unter Beachtung der Informationen für beide Reaktionen möglichst alle jeweiligen Edukte und Produkte in ihren Strukturformeln (think – pair – share).
- Versuchen Sie bei allen ionischen Verbindungen bereits eventuelle Ladungen zu bestimmen.
Eine Frage zum Setting
- Stellen Sie abseits davon eine begründete Vermutung auf, warum wir im Modellexperiment im Labor Propan-1-ol anstelle von Ethanol verwenden.
Wir nähern uns an: Zwei Modellexperimente
Weiteres
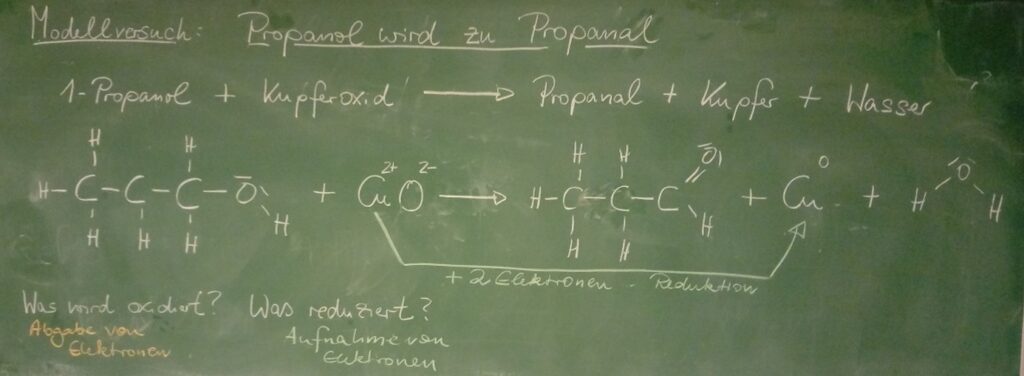
Um den Begriff der Oxidation in diesem Zusammenhang besser zu verstehen, schauen wir uns eine ähnliche Reaktion im Labor an. Auch hier oxidieren wir einen Alkohol, ersetzen aber Ethanol durch Propan-1-ol und NAD+ durch Kupferoxid:
Eintauchen von heißem Kupferoxid in Propan-1-ol6
Weiteres
Bei dem Demonstrationsexperiment handelt es sich streng genommen um zwei Versuche:
- Zunächst wird Kupfer in der Brennerflamme durch Sauerstoff aus der Luft zu Kupferoxid (CuO) oxidiert.
- Dann wir das erhitzte Drahtnetz mit dem Kupferoxid in Propan-1-ol getaucht. Dabei entstehen Propanal und Wasser.
Beide Produkte ließen sich eindeutig nachweisen. Darauf wird hier verzichtet.
Bei der gemeinsamen Auswertung der beiden Versuch lernst du, Elektronenübertragungen mit Hilfe von sogenannten Oxidationszahlen sichtbar zu machen.
Wir wollen dazu erst einmal zusammen schauen, was wir bereits erkennen und an welcher Stelle in der Beschreibung der Redoxvorgänge wir im Moment noch scheitern (müssen).
Oxidationszahlen bestimmen und nutzen
- Vollziehen Sie das Beispiel aus M3 nach.
- „Thinking classroom“: Wenden Sie das Konzept der Oxidationszahlen auf die Reaktion von Propan-1-ol mit Kupferoxid an. Ermitteln Sie, welcher Reaktionspartner Elektronendonator und welcher Reaktionspartner Elektronenakzeptor ist. Beziehen Sie gemeinsam eine begründete Position, die Sie auch vorstellen können.
- Für Schnelle: Skizzieren Sie 2-Butanol und 2-Methyl-2-butanol in ihrer Valenzstrichformel und bestimmen Sie alle Oxidationszahlen im Molekül.
Anregungen und Lösungen
Die Bindungselektronen eines jeden Atoms werden dem elektronegativeren Bindungspartner zugeordnet. Besitzen beide Bindungspartner dieselbe Elektronegativität, so werden jedem die Hälfte der Bindungselektronen zugeordnet. Mit einer gestrichelten Linie kennzeichnen wir im Ethanol-Molekül die den Atomen zugeordneten Elektronen:
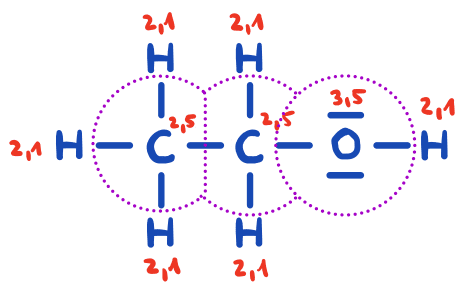
Die Angabe der Oxidationszahlen erfolgt in römischen Zahlen. Negative Oxidationszahlen ergeben sich, wenn die Summe der Elektronen, die einem Atom zugesprochen wurde, größer ist als die Anzahl der Valenzelektronen gemäß dem Periodensystem. Bei positiven Oxidationszahlen verhält es sich genau umgekehrt. Bezogen auf Ethanol ergibt sich:
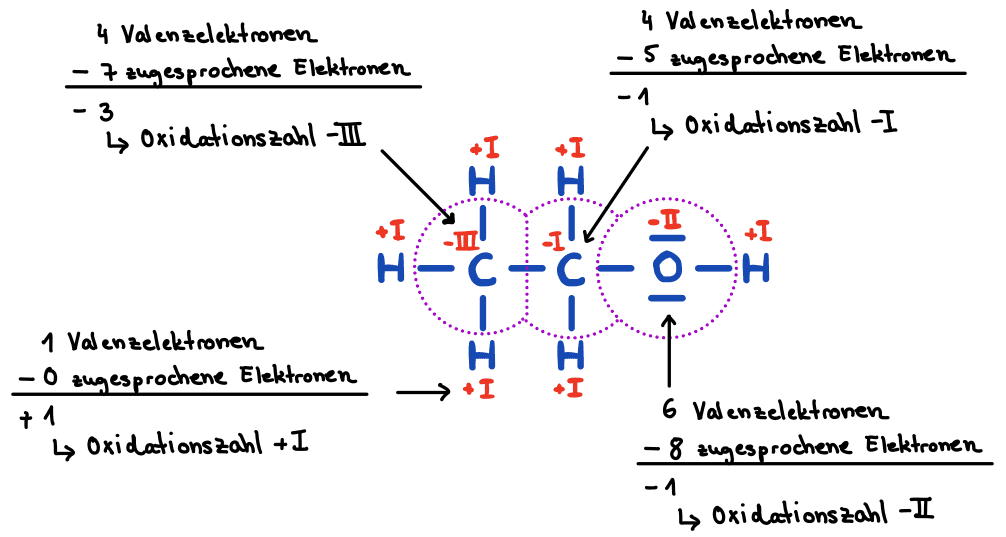
Propan-1-ol (1-Propanol) reagiert mit Kupferoxid (CuO) zu Propanal, Kupfer und Wasser gemäß der folgenden Reaktion. Zur Lösung der Aufgabe 8 gehen Sie nun wie folgt vor:
- Bestimmen Sie für jedes Atom in der Reaktionsgleichung die Oxidationszahl.
- Vergleichen Sie die Oxidationszahlen der Edukte mit denen der Produkte. An zwei Stellen muss eine Änderung vorliegen!
- Beim Vergleich zwischen Edukt und Produkt: Welche Änderung in der Oxidationszahl entspricht einer Reduktion oder einer Oxidation?
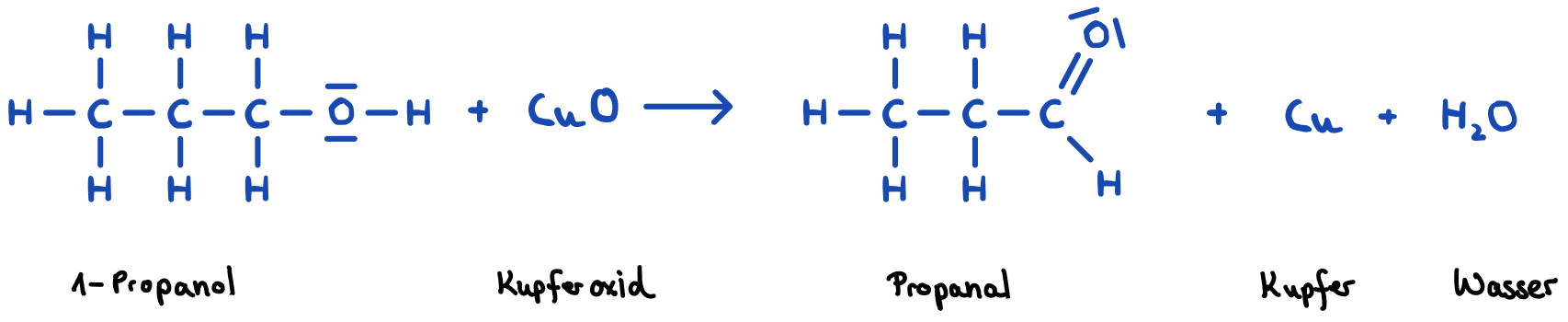
Nachfolgend sind alle Oxidationszahlen für die Reaktion von Propan-1-ol (= 1-Propanol) mit Kupferoxid (CuO) zu Propanal, Kupfer und Wasser angegeben. Doch an welcher Stelle liegt eine Änderung in den Oxidationszahlen vor?
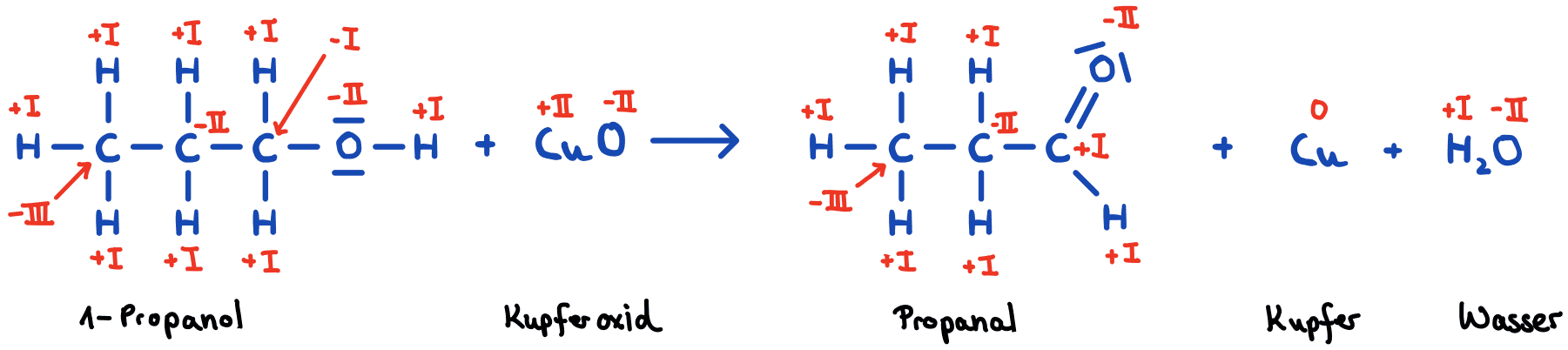
In der Reaktion von Propan-1-ol (1-Propanol) mit Kupferoxid wird Propan-1-ol zu Propanal oxidiert. Dies erkennt man an der Änderung der Oxidationszahl am Kohlenstoffatom, welches die Alkoholgruppe (Hydroxygruppe) gebunden hat. Hier ändert sich die Oxidationszahl von -I zu +I, was gleichzusetzen ist mit der Abgabe von 2 Elektronen (= Oxidation).
Kupferoxid wird zu Kupfer reduziert. Dies erkennt man an der Änderung der Oxidationszahl am Kupfer von zuvor +II auf 0, was gleichzusetzen ist mit der Aufnahme von 2 Elektronen (= Reduktion).
Bei der vorliegenden Reaktion handelt es sich also um eine Elektronenübertragungsreaktion (= Redoxreaktion) von Propan-1-ol auf Kupferoxid. Wasser entsteht als Nebenprodukt.
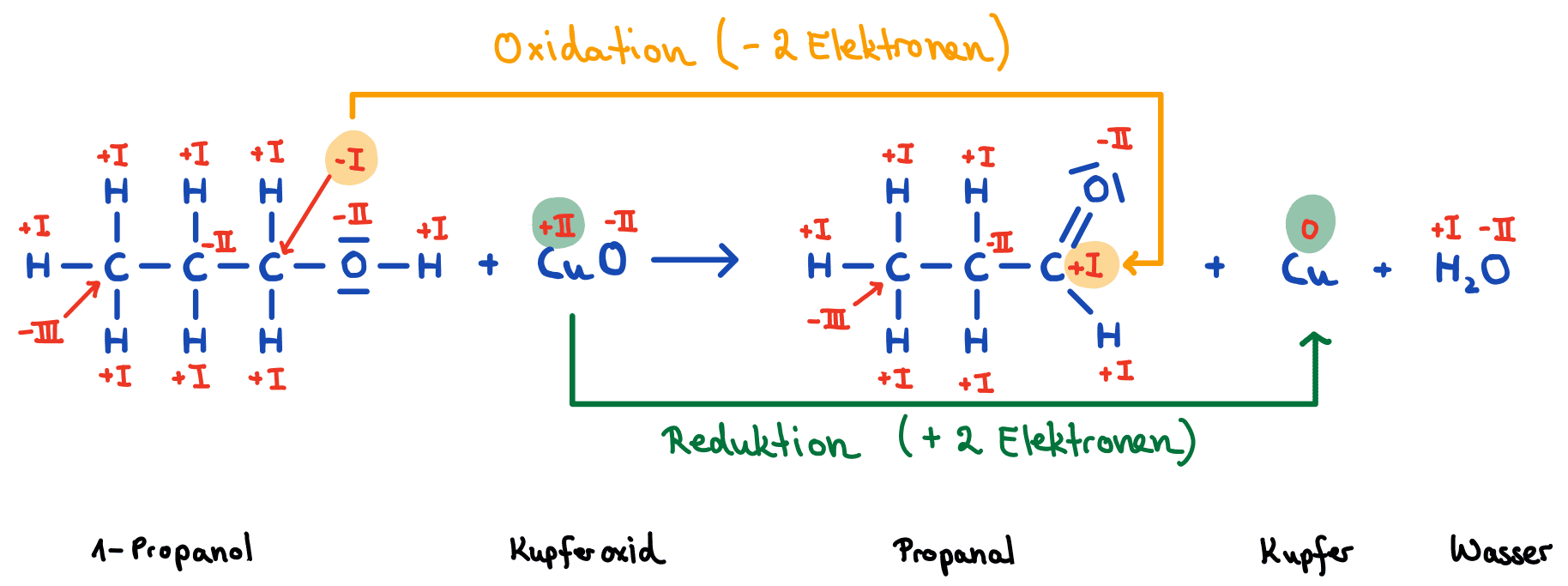
Das Konzept der sogenannten Oxidationszahlen
Redoxreaktionen mit Molekülen
Bei vielen (bio)chemischen Reaktionen handelt es sich um Redoxreaktionen, d.h. in irgendeiner Form werden Elektronen ausgetauscht.
Das ist anfänglich schwer zu erkennen, da die Atome in Molekülen oft keine echten Ladungen aufweisen. Hier helfen die sogenannten Oxidationszahlen. Diese beschreiben an Stelle von echten Ladungen „fiktive“.
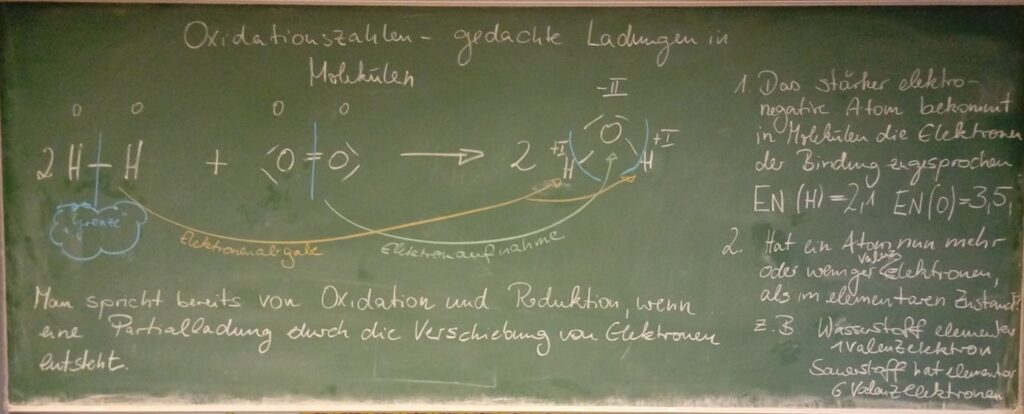
Wie man Oxidationszahlen ermittelt und benutzt betrachten wir einmal an der Beispielreaktion von Wasserstoff mit Sauerstoff zu Wasser.
Oxidatonszahlen - ein einfaches Beispiel
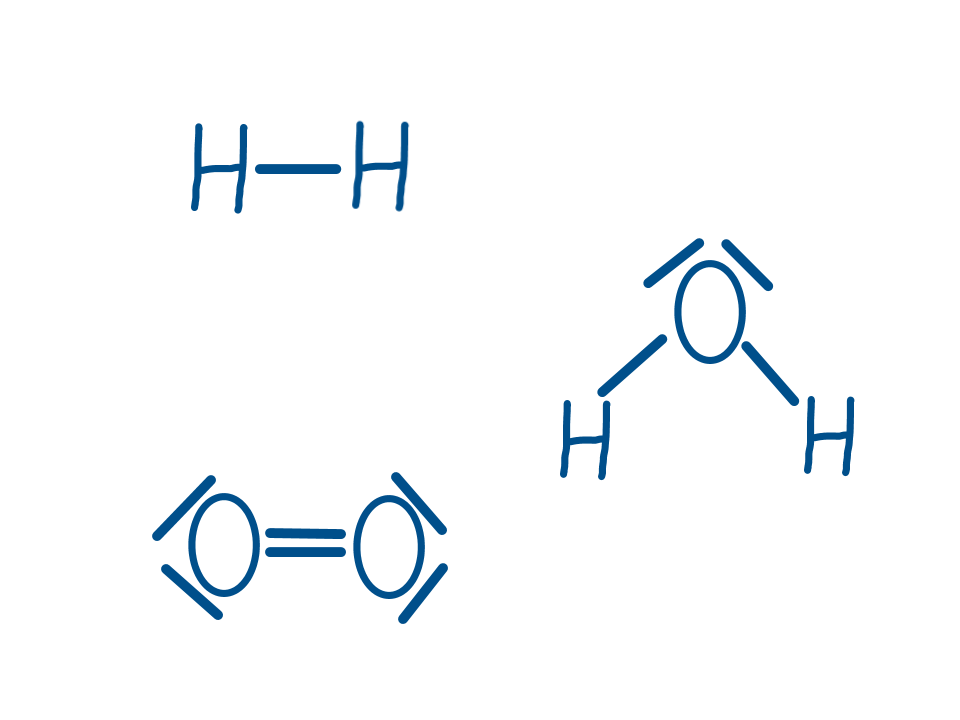
Oxidationszahlen aus Strukturformeln ableiten.7
Wie gehen wir vor?

Erklärung der Methode.7
Oxidationszahlen bestimmen - Vorgehensweise detaillierter erklärt
Betrachte in der Strukturformel die bindenden Elektronenpaare. Für die Aufstellung von Oxidationszahlen prüfe, ob die Elektronen vollständig einem der beiden Atome zugeordnet werden können.
- gleiche Elektronegativität → Elektronen werden gerecht geteilt.
Haben zwei Atome dieselbe Elektronegativität, bekommt jeder Partner gedanklich ein Elektron aus dem gemeinsamen Paar.
Beispiel: H–H in H2 → beide Wasserstoffatome erhalten je 1 Elektron → Oxidationszahl: 0. - unterschiedliche Elektronegativität → Das elektronegativere Atom „zieht“ die Bindungselektronen stärker an und bekommt deshalb beide Elektronen zugeordnet. Beispiel H2O: Sauerstoff (EN = 3,5) ist deutlich elektronegativer als Wasserstoff (EN = 2,1). → In jeder O–H-Bindung ordnen wir beide Elektronen dem O-Atom zu.
Oxidationszahlen aus der Zuordnung ableiten (Vergleich zum elementaren Atom)
Wasserstoff:
Ein einzelnes Wasserstoffatom besitzt 1 Valenzelektron. Im Wassermolekül bekommt es aus der O–H-Bindung kein Elektron mehr zugeordnet. → Es „verliert“ ein Elektron im Vergleich zum elementaren Zustand (Oxidationszahl 0) → Oxidationszahl: +I
Sauerstoff:
Ein einzelnes Sauerstoffatom besitzt 6 Valenzelektronen. Im Wassermolekül werden ihm durch beide O–H-Bindungen zwei zusätzliche Elektronen zugeordnet. → Es „gewinnt“ zwei Elektronen im Vergleich zum elementaren Zustand (dort Oxidationszahl 0) → Oxidationszahl: –II
Mache am Ende eine schnelle Kontrolle über die Gesamtladung:
Die Oxidationszahlen der beiden Wasserstoffatome (+I und +I) und des Sauerstoffatoms (–II) im Wassermolekül ergeben zusammen 0 → passt zur Gesamtladung eines neutralen Wassermoleküls.
Oxidationszahlen benutzen
Wechselt ein Atom im Laufe einer chemischen Reaktion die formale Ladung, also seine Oxidationszahl, so entspricht das – gleichbedeutend mit dem Wechsel einer echten Ladung – einer Aufnahme bzw. Abgabe von Elektronen.
Also kann man Oxidationen und Reduktionen nicht nur am Wechsel echter, sondern auch am Wechsel formaler Ladungen erkennen: Oxidation bei steigender Oxidationszahl, Reduktion bei sinkender Oxidationszahl!