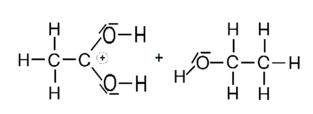Ist das plausibel?
Weiteres
Kann es wirklich sein, dass in dem geschlossenen Gefäß sowohl eine Estersynthese als auch eine Esterspaltung stattfinden?
Wechseln wir einmal auf die molekulare Ebene und schauen uns Schritt für Schritt die Reaktionen im Einzelnen an, die vermutlich1 nacheinander ablaufen.
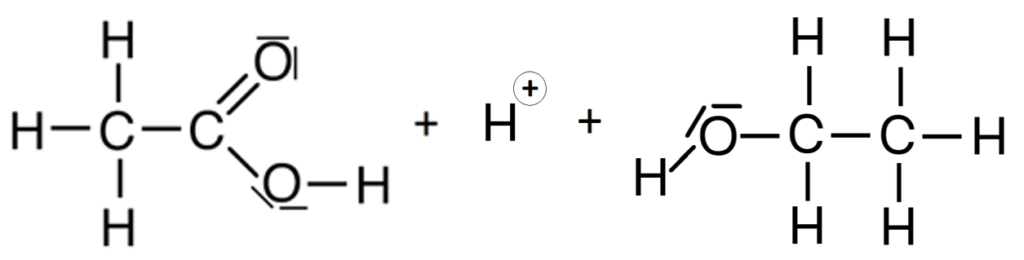
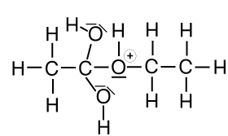
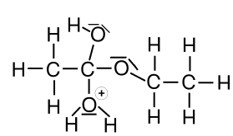
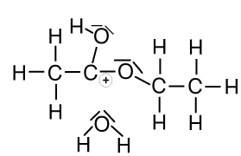
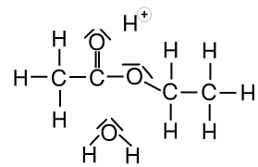
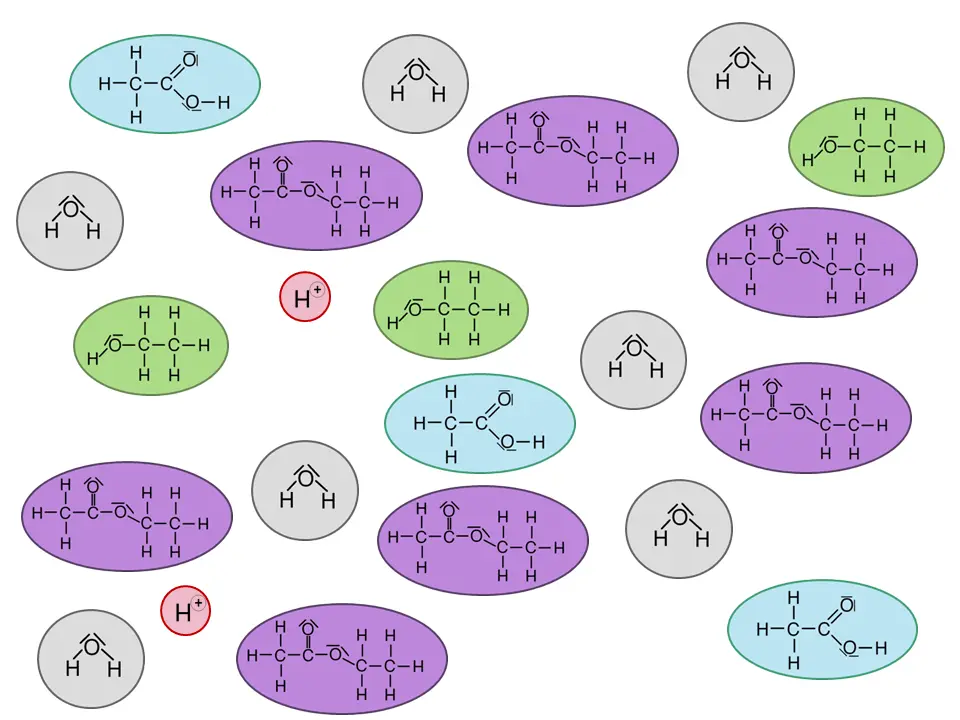
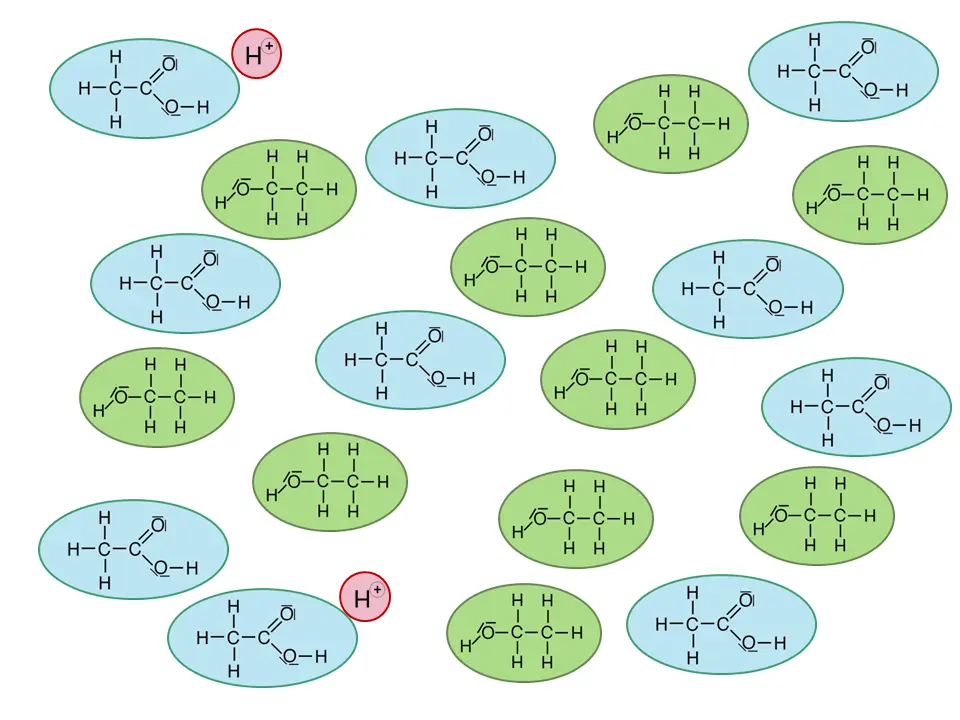
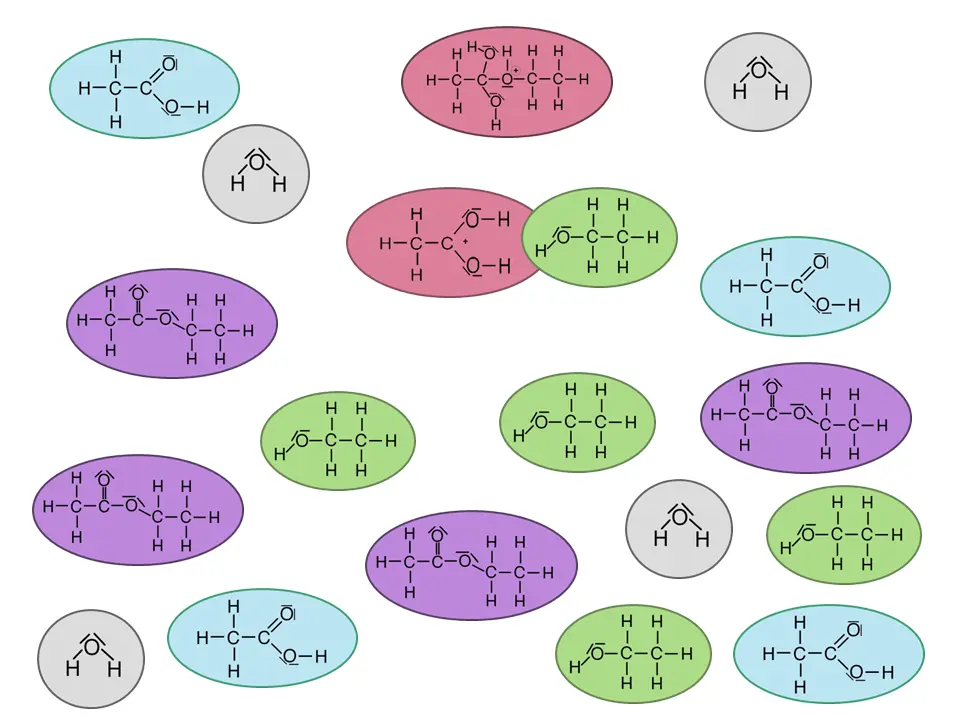
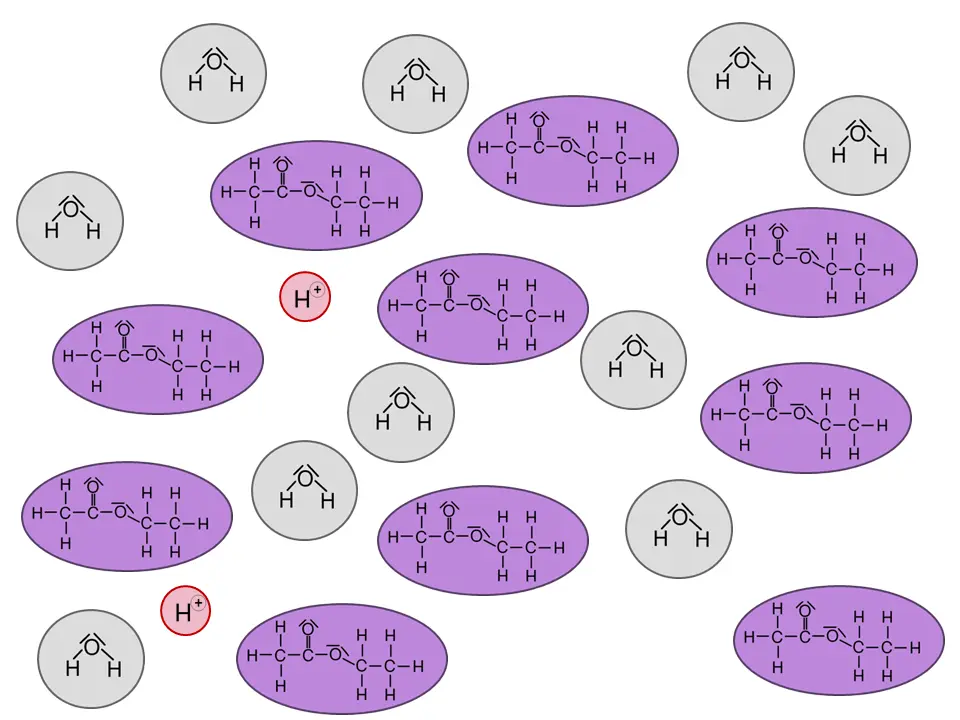
In Galerie 1 sind ausgehend von Ethansäure und Ethanol Strukturformeln gezeichnet. Man sieht, wo der Katalysator am Anfang bindet und welche Zwischenprodukte entstehen. Am Ende entstehen die Produkte Ethansäureethylester und Wasser sowie der wieder freigesetzte Katalysator.
Weiteres
Klick dich einmal „vorwärts“ durch die einzelnen Schritte der Reaktion und dann „rückwärts“. Was sagst Du?
Die Reaktion mit Zwischenprodukten.
Okay, das ist plausibel. Aber es ist noch kein Beweis.
Aufgaben
- Überlegen Sie kurz, wie man experimentell einfach prüfen kann, dass die Rückreaktion tatsächlich stattfindet.
- Werten Sie im Anschluss M2 diesbezüglich aus.
Esterspaltung im geschlossenen Gefäß
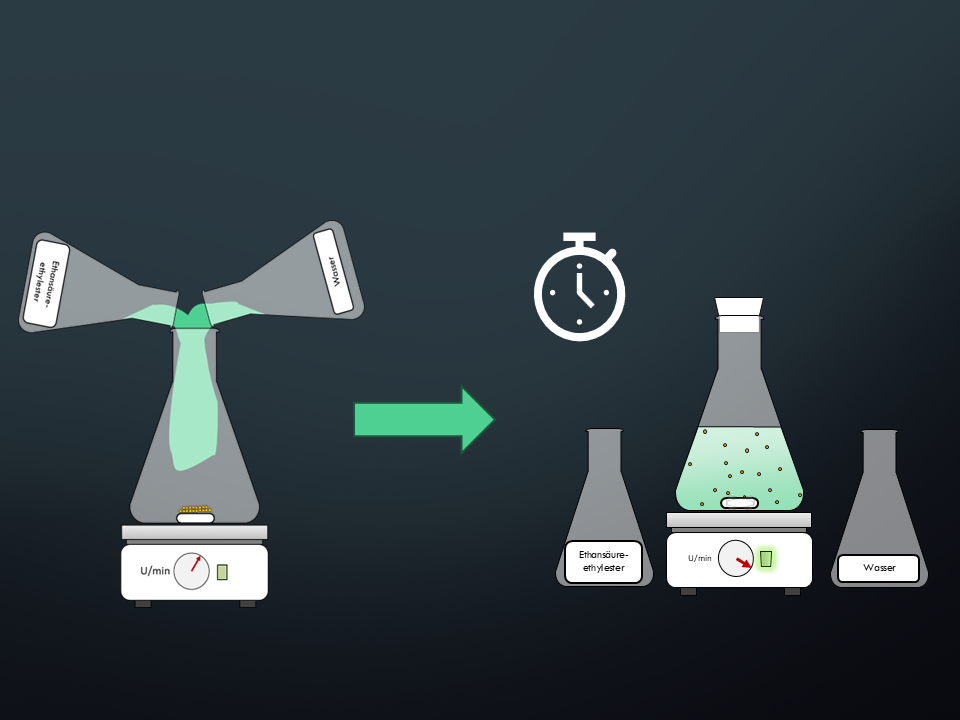
Der Aufbau
Schaue dir an, was in folgendem Versuch, der sogenannten „Esterhydrolyse„2, gemacht wird.
Versuchsaufbau3
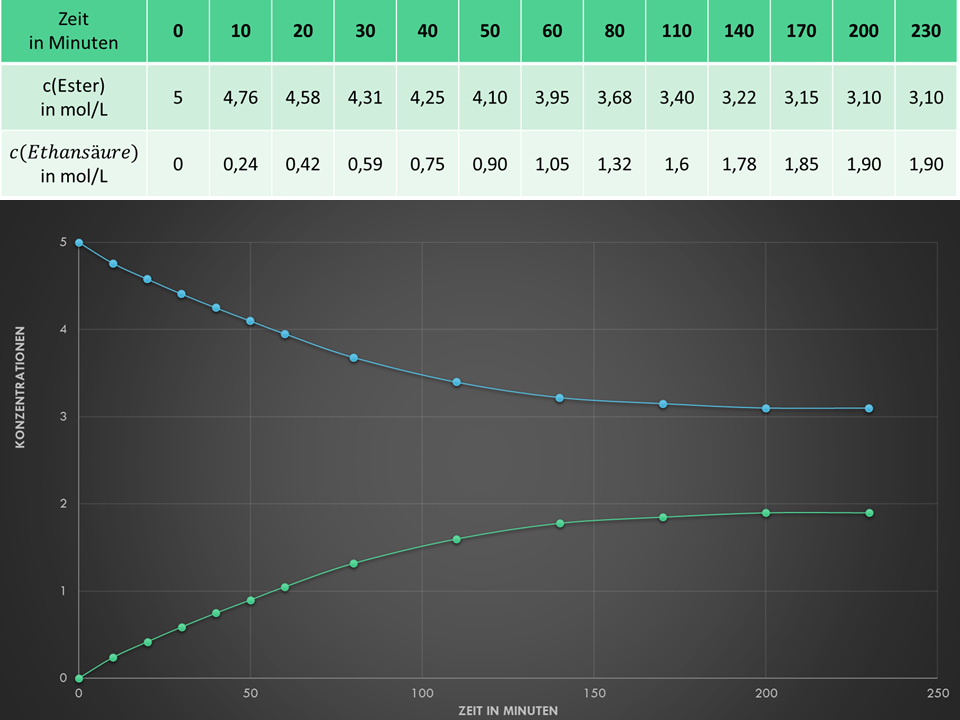
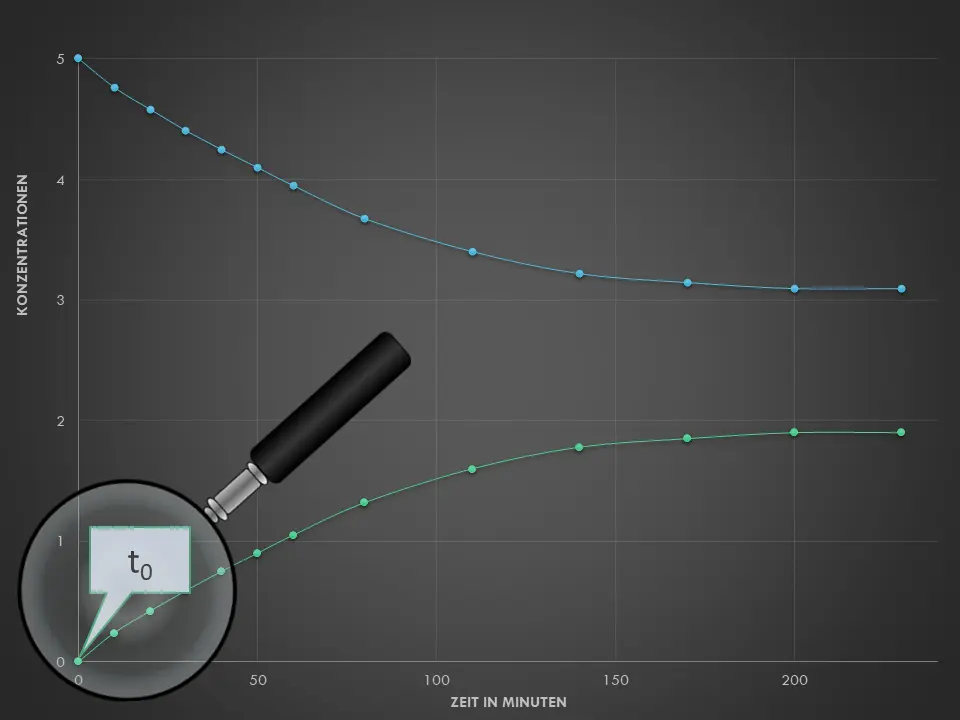
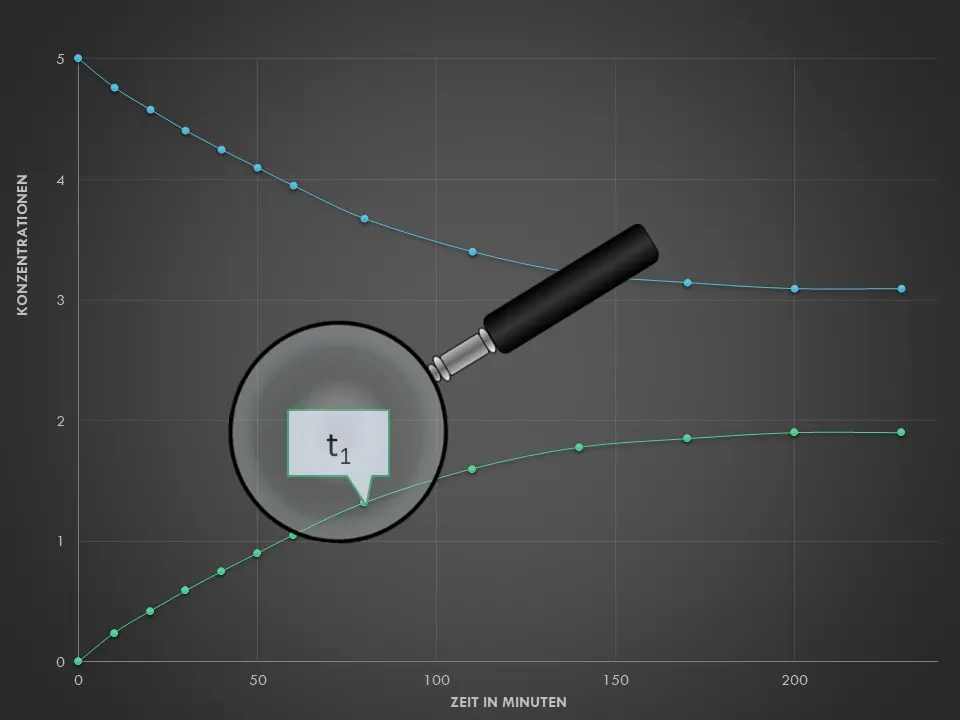
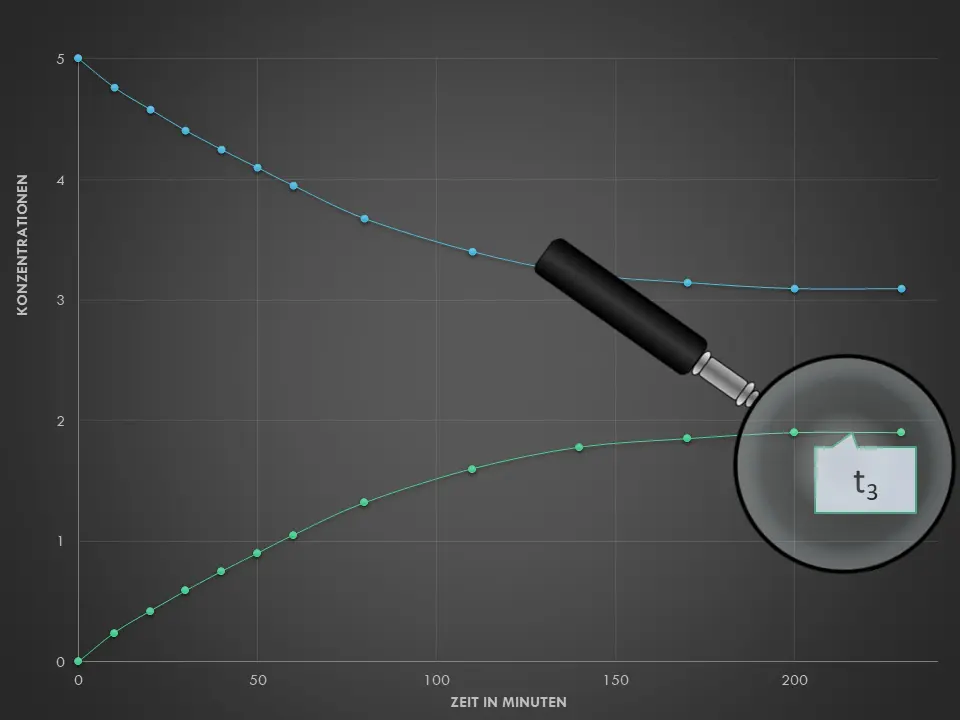
Die Anfangskonzentration des Ethansäureethylesters und die Anfangskonzentration von Wasser sind gleich. Sie beträgt jeweils 5 mol/L. Damit ist sichergestellt, dass der gesamte Ester reagieren könnte.4
Aufgaben
- Erkläre nun, warum in einem geschlossenen Gefäß niemals alle Ethansäure mit Ethanol vollständig zu Ethansäureethylester reagiert.
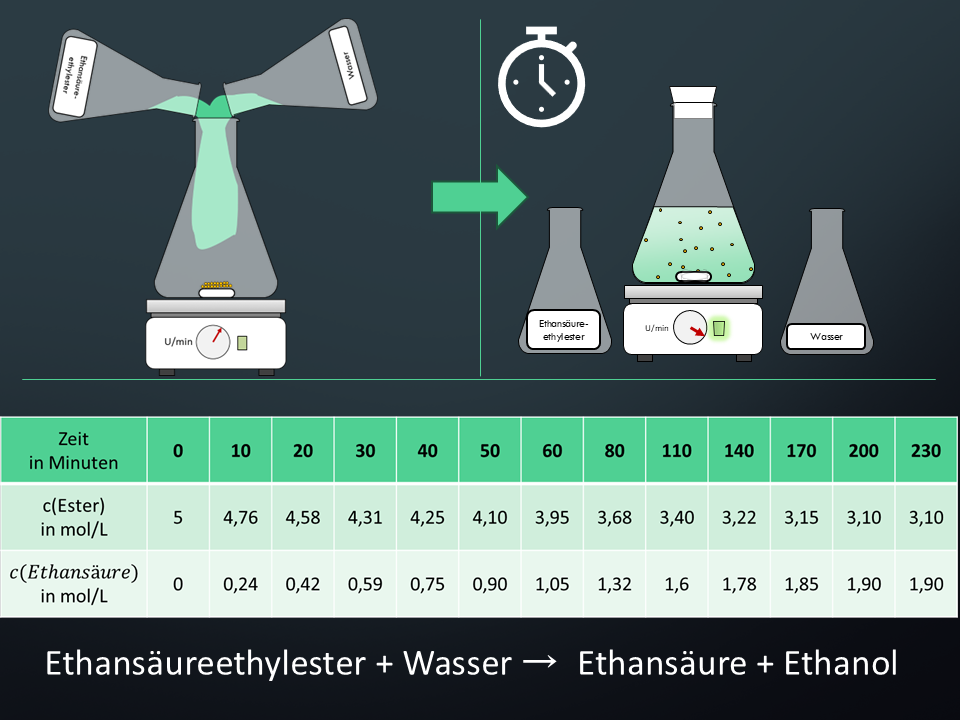
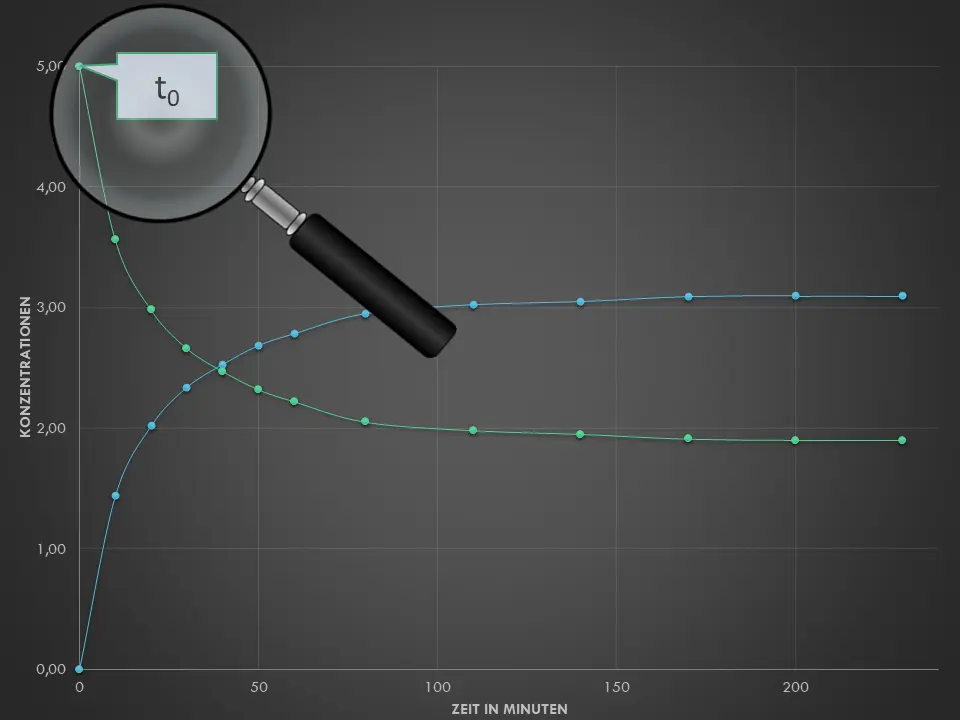
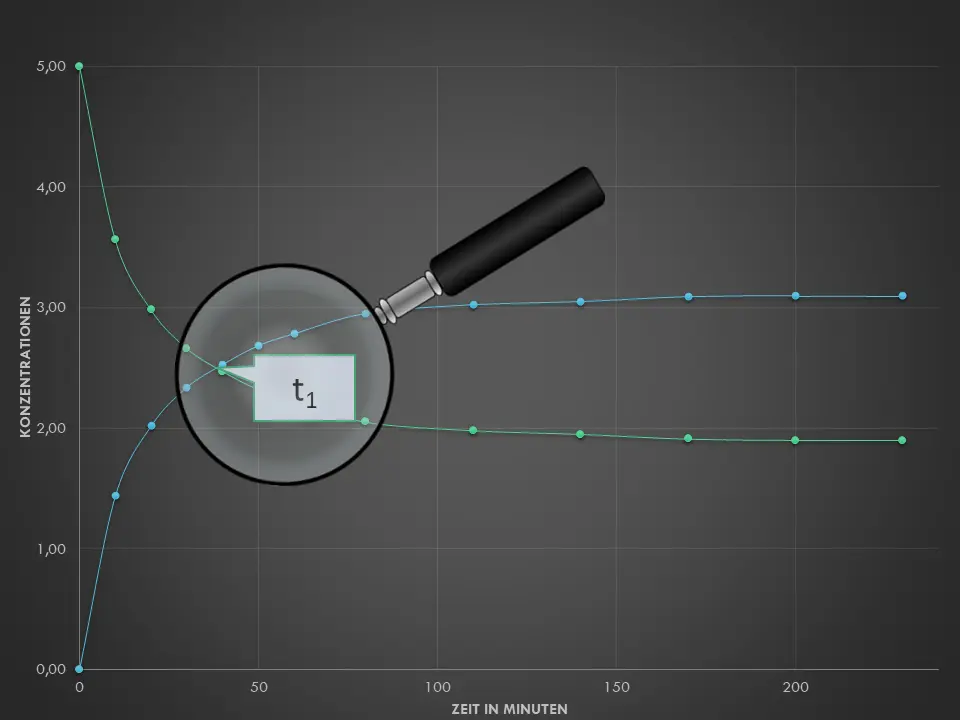
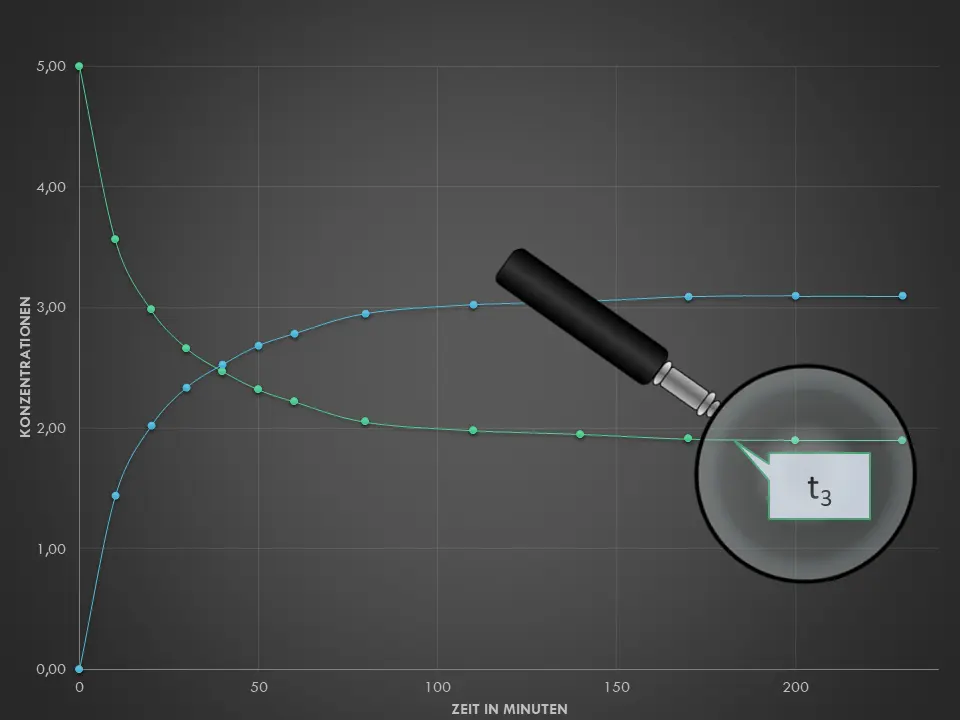
- Beschreibe mit Hilfe von M3, was man unter einer Hin- und Rückreaktion versteht. Erkläre den Begriff des chemischen Gleichgewichts an diesem Beispiel. Achte dazu auf Details in Abb. 2 – fällt dir etwas bezüglich der Konzentrationen auf?
- In M4 sind Zeitpunkte in den Messung, Modelle auf Teilchenebene, Formeln mit ausgewählten Gleichgewichtspfeilen sowie Texte zusammengestellt. Suchen Sie stets vier passende zusammen.
Hinreaktion - Rückreaktion - chemisches Gleichgewicht
Weiteres
Wir haben die Esterbildung (Veresterung, Estersynthese) und die Esterspaltung (Esterhydrolyse) einzeln betrachtet. Nun wollen wir sie zusammen anschauen.
Weiteres
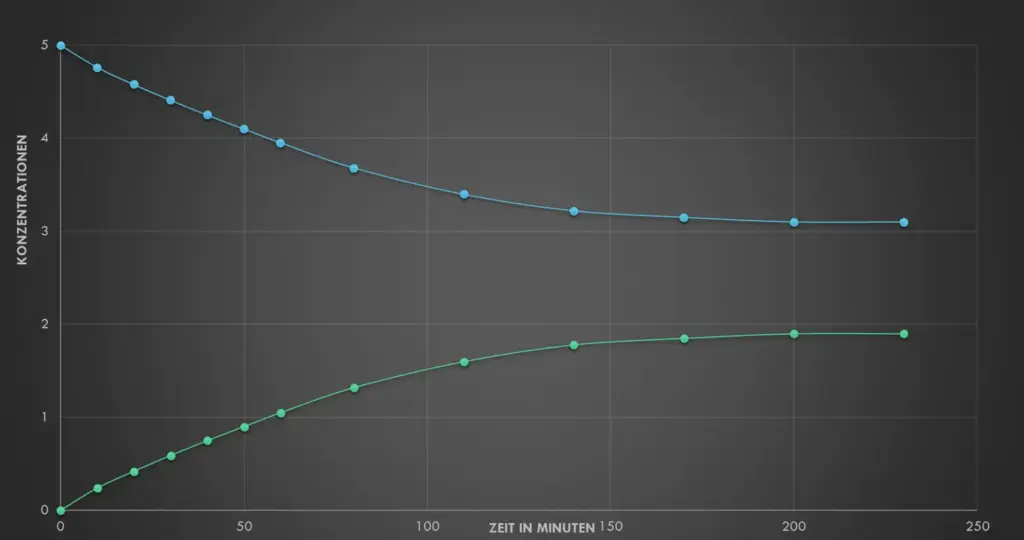
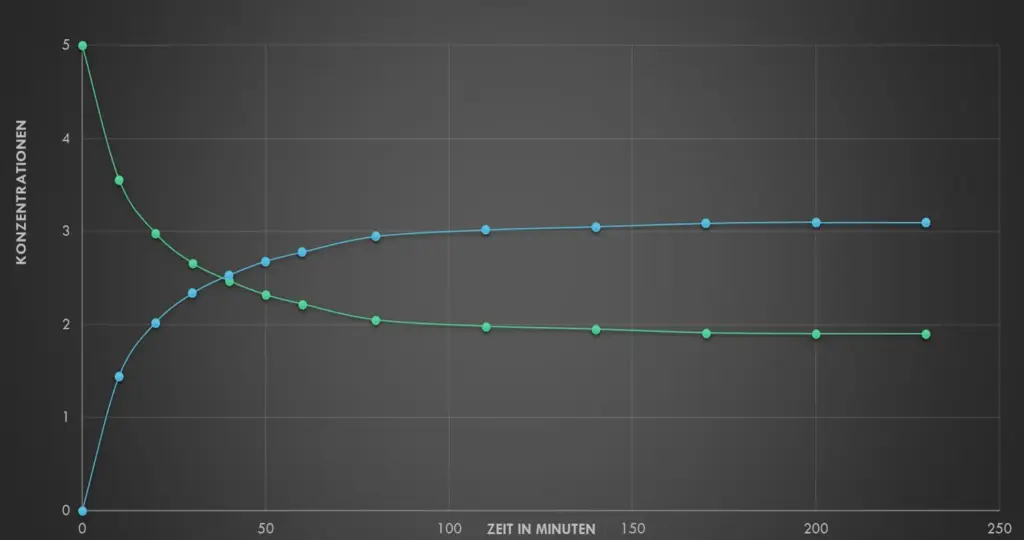
Messungen zu den Reaktionen im geschlossenen Gefäß3
Chemisches Gleichgewicht: eine Verständnisübung
Ausgewählte Zeitpunkte
Reaktionsgleichungen
Teilchenmodelle
Aussagen
Kein Stoff ist vollständig umgesetzt. Die Geschwindigkeit der Hinreaktion und der Rückreaktion sind genau gleich. Dauernd kommt es zu „erfolgreichen Stößen“ – aber wir messen keine Veränderungen der Konzentrationen mehr. Ein chemisches Gleichgewicht hat sich eingestellt.
Ethansäure reagiert mit Ethanol zu Ethansäureethylester und Wasser. Die Reaktionsgeschwindigkeit dieser Reaktion ist groß.
Ethansäureethylester und Wasser reagieren zu Ethansäure und Ethanol. Die Reaktionsgeschwindigkeit dieser Reaktion ist groß.
Es ist bereits eine merkliche Menge Ethansäureethylester entstanden. Dieses reagiert nun auch mit Wasser zurück zu Ethansäure und Ethanol.
Es ist bereits eine merkliche Menge Ethansäure entstanden. Dieses reagiert nun mit Ethanol auch wieder zu Ethansäureethylester und Wasser.