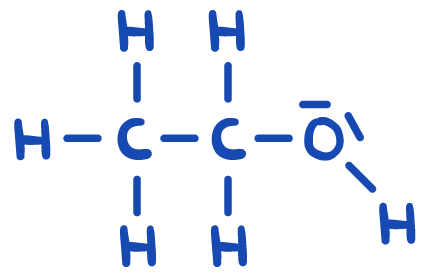Methanol neben Ethanol?
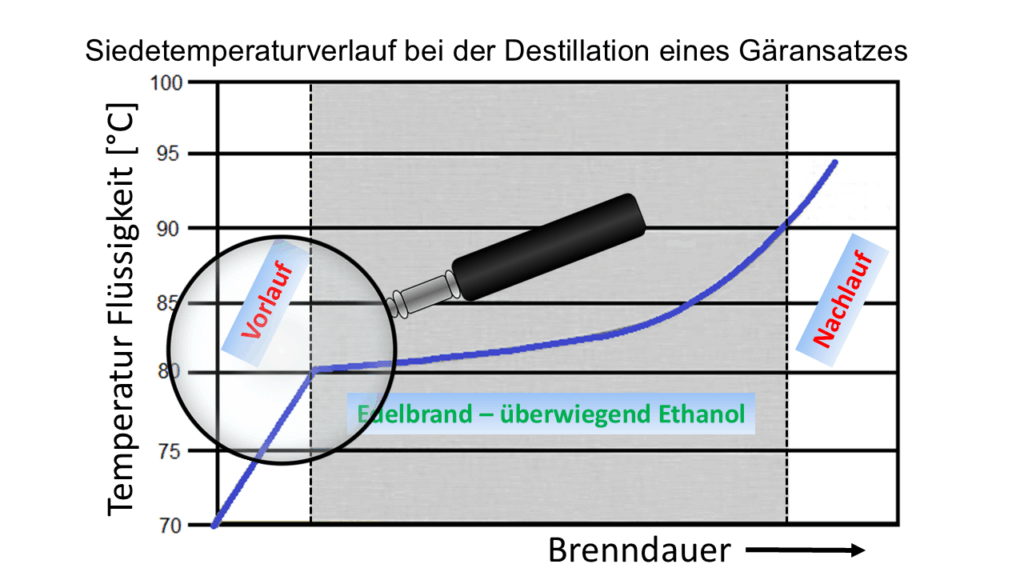
Im Ratgeber Schnapsbrennen als Hobby wird erwähnt, dass der Vorlauf bei einer Destillation eines Gäransatzes unbedingt verworfen werden sollte. Weißt Du warum?
Ich habe mal gehört, dass er neben Ethanol auch Methanol enthalten kann.
Hobbyratgeber
Ein Blick an eine andere Stelle.1
Aufgaben
- Prüfen Sie die Stichhaltigkeit der Aussage in M1 unter Verwendung der Informationen in M2.
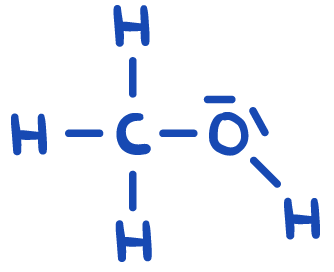
- Erläutern Sie unter Zuhilfenahme von M3, warum die Stoffe Ethanol und Methanol ähnliche, aber letztlich verschieden große Siedetemperaturen haben, indem Sie …
- … beide Flüssigkeiten im Teilchenmodell darstellen und die polaren Bindungen in den Strukturformeln kennzeichnen.
- … erklären, warum der unpolare Teil der Moleküle einen Einfluss auf die Siedetemperaturen haben muss.
- … das Zustandekommen der sog. Van-der-Waals-Kräfte in eigenen Worten beschreiben. Tipp: formulieren Sie zu den Abbildungen mehrere „Wenn-Dann-Sätze“).
- … die Stärke aller möglichen zwischenmolekularen Kräfte zwischen den jeweiligen Molekülen diskutieren.
Informationen zu Methanol und Ethanol
Wie entsteht Methanol? Was passiert im Körper damit?
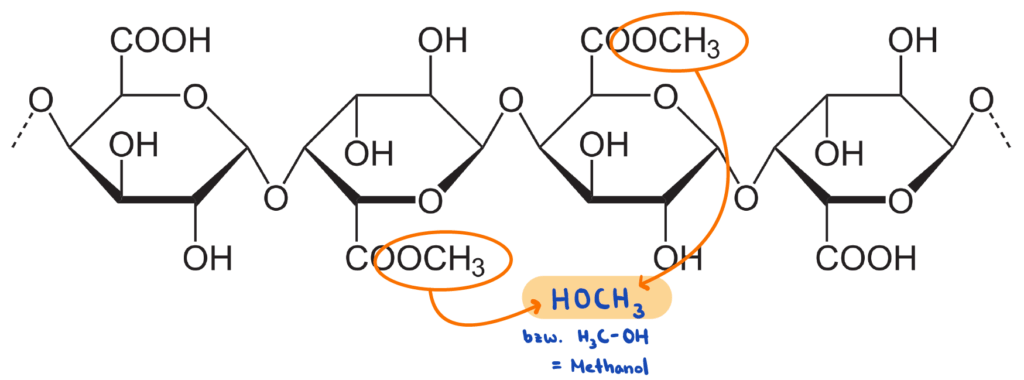
Neben Zucker bauen Hefen auch andere Kohlenhydrate ab, wie z. B. das Pektin, das in pflanzlichen Zellwänden enthalten ist. Im Verlauf von komplexen Stoffwechselprozessen werden dabei neben Ethanol zahlreiche flüchtige Verbindungen gebildet, die charakteristisch für das Aroma sind und von Spirituose zu Spirituose variieren. Eine dieser Verbindungen ist Methanol. Vor allem in Branntweinen aus Kernobst kann Methanol in größeren Mengen auftreten.
Abbau im Körper
Beim Abbau des Methanols im menschlichen Körper, den wir im Unterricht noch gesondert betrachten werden, entsteht zunächst das toxische Methanal, welches anschließend zu Methansäure (Ameisensäure) umgesetzt wird. Diese Ameisensäure schädigt insbesondere Nervenzellen und kann bei einer entsprechend hohen Konzentration zu Erblindungen und auch zum Tod führen.
Selbstgebrannte Schnäpse können aus Unwissenheit oder aus Gründen der Gewinnmaximierung zu viel Methanol enthalten.
Daten zu Ethanol
Ethanol (C2H5OH) hat eine Siedetemperatur von 78 °C und ist beliebig mit Wasser oder Heptan mischbar.
- Oral LD50(Ratte) = 7060 mg/Kg
- Oral LDLo(Mensch) = 1400 mg/Kg
- H225: Flüssigkeit und Dampf leicht entzündbar.
- H319: Verursacht schwere Augenreizung.
- H336: Kann Schläfrigkeit und Benommenheit verursachen.
Der LD50-Wert gibt die Menge einer Substanz an, die bei 50 % der Versuchstiere zum Tod führt. Je geringer dieser Wert ist, desto giftiger ist die Substanz. Ein LDLo-Wert beziffert die niedrigste publizierte (Fachbegriff für veröffentlichte) Dosis mit Todesfolge beim Menschen.
Daten zu Methanol
Methanol (CH3OH) hat eine Siedetemperatur von 65 °C und ist beliebig mit Wasser oder Ethanol mischbar.
- Oral LD50(Ratte) = 5628 mg/Kg
- Oral LDLo(Mensch) = 143 mg/Kg
- H225: Flüssigkeit und Dampf leicht entzündbar.
- H301: Giftig bei Verschlucken.
- H311: Giftig bei Hautkontakt.
- H331: Giftig bei Einatmen.
- H370: Verursacht Schäden an den Organen.
Hast Du eine Erklärung dafür, warum man selten neue LD50-Werte, mitunter aber schon mal aktualisierte LDLO-Werte für Stoffe in Gefahrstoff-Datenbanken findet?
Die Van-der-Waals-Kraft
Ausgangspunkt: Temporärer Dipol
Auch zwischen Atomen, Molekülen oder Molekülteilen, die wir als unpolar einstufen, können Anziehungskräfte wirken. Korrekt spricht man hier von nicht-permanenten Dipolen, also Dipolen, die nicht dauerhaft bestehen.
Wie diese Anziehungskräfte entstehen, lässt sich am einfachsten am Beispiel von zwei Atomen erklären. Das Gesagte gilt aber ebenso für Moleküle oder deren Teilbereiche!
Die negativ geladenen Elektronen in einem Atom sind in ständiger Bewegung. Dadurch kann es kurzfristig zu einer ungleichmäßigen Ladungsverteilung innerhalb des Atoms kommen.
Das Atom wird so für einen kurzen Moment zu einem temporären (also kurzzeitigen) Dipol – es entstehen positive und negative Teilladungen (Partialladungen).
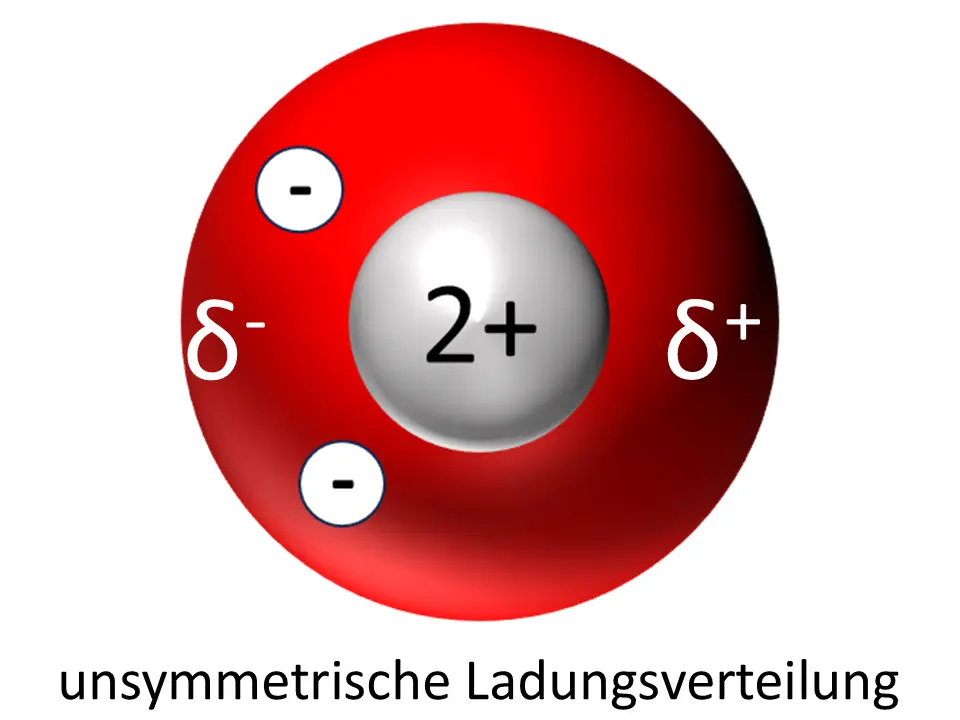
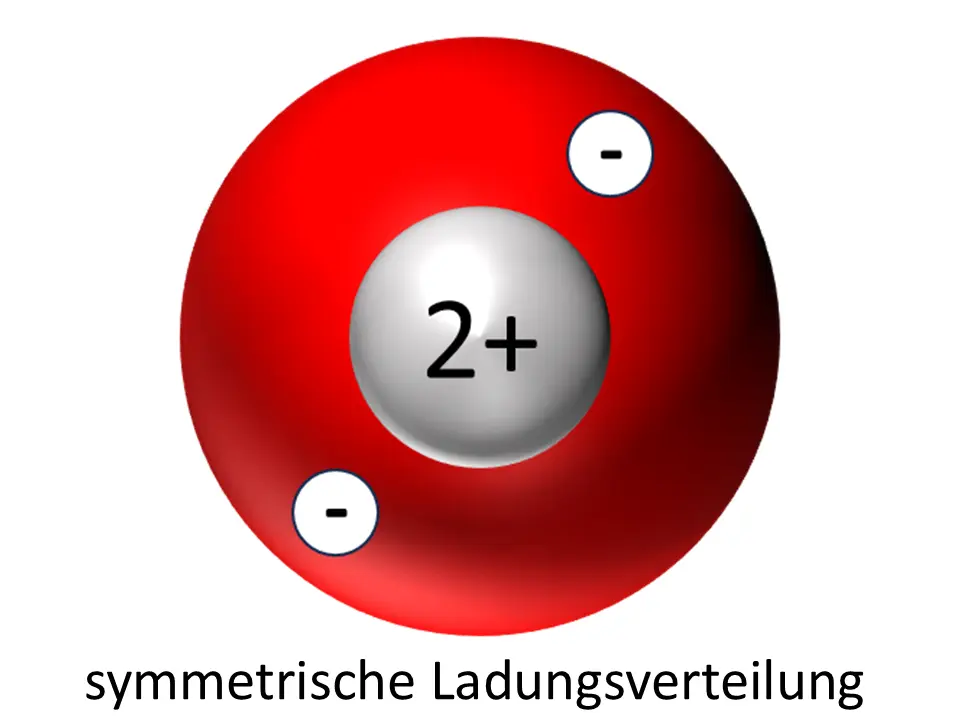
In einem Heliumatom ist die Ladung symmetrisch verteilt, im anderen hat sich zufällig ein temporärer Dipol gebildet.
Induzierter Dipol
Nähern sich nun zwei Atome genügend an, kann Folgendes passieren: Ein temporärer Dipol trifft auf ein ungeladenes Atom und bewirkt (induziert) bei diesem ebenfalls einen Dipol. So entsteht eine Anziehungskraft zwischen den beiden Atomen – diese wird als van-der-Waals-Kraft bezeichnet.
Die elektrische Anziehung ist allerdings schwach und wirkt nur über eine sehr kurze Entfernung.
Damit die van-der-Waals-Kraft überhaupt wirksam werden kann, müssen sich zwei Atome oder Moleküle sehr nahe kommen. Das funktioniert umso schlechter, je mehr Bewegungsenergie die Teilchen besitzen – also je höher die Temperatur in der Stoffprobe ist.
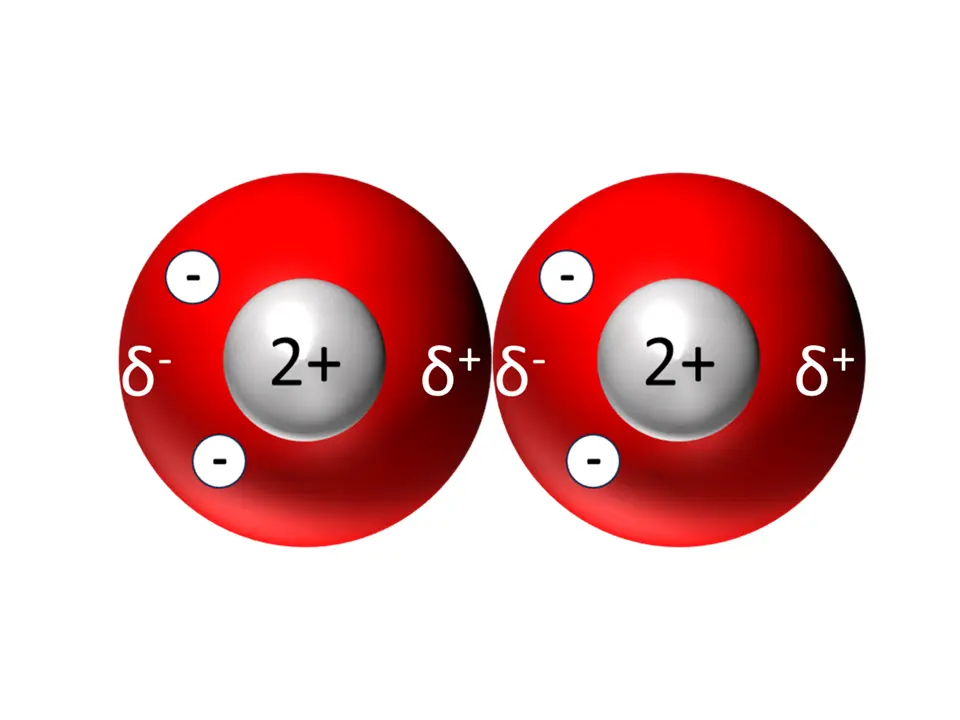
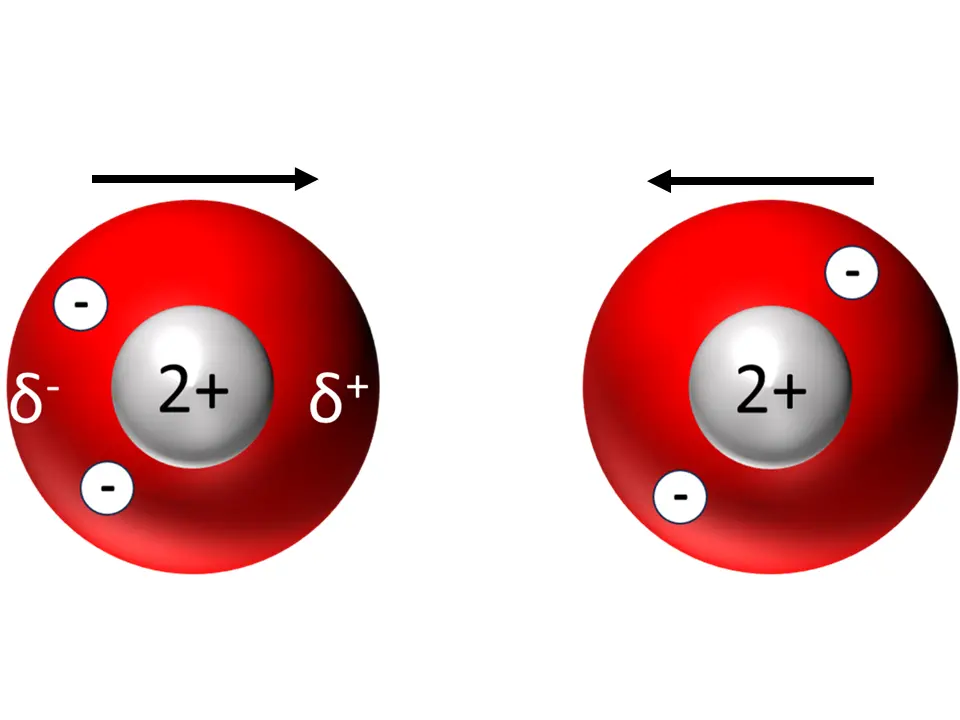
Der temporäre Dipol im Atom links sorgt bei Annäherung dafür, dass in einem Nachbaratom rechts ebenfalls kurzzeitig ein Dipol entsteht. Beide Atome ziehen sich nun kurzzeitig an.
Stärke der Kraft
Grundsätzlich nimmt die Van-der-Waals-Kraft mit wachsender Masse und Oberfläche der Moleküle zu. Deshalb kann sie bei großen, unpolaren Molekülen oder entsprechenden Molekülteilen sehr stark werden.

Geckos können scheinbar mühelos glatte und senkrechte Oberflächen erklimmen. Grund dafür ist die Van-der-Waals-Kraft.2
Geckos nutzen übrigens die van-der-Waals-Kraft, um an senkrechten Flächen zu haften. Die Haftballen an ihren Füßen sind mit feinsten Härchen besetzt, was die Kontaktfläche enorm vergrößert. So entstehen genügend starke van-der-Waals-Kräfte, dass sie selbst an senkrechten oder sehr glatte Oberflächen „haften“.
Weitergedacht
- Entschlüsseln Sie in M4 die Farbcodierung und beurteilen Sie, ob die Darstellungen dort unsere Vorstellungen der Polaritäten in den Molekülen stützen.
- Formulieren Sie Vorschläge, mit denen wir experimentell prüfen können, ob in unserem Gäransatz neben Ethanol möglicherweise auch Methanol entstanden ist.
Das elektrochemische Potenzial
Wie verteilt sich die Ladung im Molekül?
Auf der Internetseite von chemie-interaktiv.net gibt es einen Molekülbetrachter, mit dessen Hilfe sich ausgewählte Moleküle dreidimensional anzeigen lassen. Zudem lässt sich das elektrochemische Potenzial eines Moleküls farblich hervorheben, wie zum Beispiel in Abb. 6.
Wenn man die Farbcodierung versteht, kann man etwas über die Polarität im jeweiligen Molekül aussagen. Basierend darauf kann man dann etwas über die zwischenmolekularen Wechselwirkungen zwischen zwei solcher Moleküle sagen. Versuche es fachsprachlich korrekt einmal.
Weiteres
Ethanolmolekül und Methanolmolekül.3
Lesetipps
Was passiert bei einer Methanolvergiftung?
Etwas ausführlicher: Methanolvergiftung – Wie groß ist die Gefahr für jeden Einzelnen?
Wie kommt der Gecko die Wand hoch?
Vertiefend und ausführlich – eines von vielen interessanten Max-Wissen Angeboten.
Vergiftung durch K.O. Tropfen
K.O.-Tropfen haben nichts mit Methanol zu tun, werden aber mitunter heimlich Getränken beigemischt und wirken zusammen mit Alkohol. Manchmal sieht eine Vergiftung mit K.O.-Tropfen sogar wie eine Alkoholvergiftung aus. Es ist daher wichtig zu wissen, worauf man achten sollte und wie man sich schützen kann.