Im Tieftemperaturlabor von Kammerlingh Onnes
Flüssiges Helium
Zu Beginn des 20 Jahrhunderts gab es geradezu einen Wettlauf darum, Gase zu verflüssigen. Am 10. Juli 1908 gelang dies dem späteren Nobelpreisträger Kammerlingh Onnes samt seinem Team mit dem „letzten Gas: Helium“.
In folgendem Hotspot findest du eine zusammenfassende Beschreibung dieses aufregenden Tages.1

Kamerlingh Onnes vor seinem Luftverflüssiger in Leiden 1913.2
Zurück zur Verflüssigung der genannten Gase. Fokussieren wir darauf, was wir daraus über Kräfte zwischen Molekülen Neues lernen und wie wir uns den Zusammenhalt eigentlich unpolarer Atome und Moleküle erklären können.
Aufgaben
- Mache dich mit Hilfe von M1 mit den Umständen der ersten Verflüssigung von Helium vertraut.
- Auf dem Weg zum flüssigen Helium (He) wurden zuvor Sauerstoff (O2), Stickstoff (N2) und Wasserstoff (H2) verflüssigt. Erkläre, was nach unserem bisherigen Kenntnisstand über die zwischenmolekularen Kräfte das Besondere an der Verflüssigung genau dieser vier Gase ist.
- Erläutere basierend auf M2, wie es zu Anziehung zwischen Heliumatomen und folglich zur Verflüssigung von Helium kommen kann. Fertige dazu eine beschriftete Skizze an, die du auch vorstellen kannst.
Weitergedacht (ggf. für die Arbeit zu Hause oder in der kommenden Stunde)
- Erkläre die zunehmenden Siedetemperaturen der Edelgase mit steigender Atommasse basierend auf den Informationen in M2.
- Vergleiche die Dipol-Dipol-Wechselwirkungen mit den Van-der-Waals-Kräften. Nutze dazu je eine Skizze von zwei Wassermolekülen und zwei Stickstoffmolekülen, in die du mit Text, Pfeilen und anderen Symbolen Erläuterungen einfügst. Benenne Gemeinsamkeiten und Unterschiede.
Die Van-der-Waals-Kraft
Ausgangspunkt: Temporärer Dipol
Auch zwischen Atomen, Molekülen oder Molekülteilen, die wir als unpolar einstufen, können Anziehungskräfte wirken. Korrekt spricht man hier von nicht-permanenten Dipolen, also Dipolen, die nicht dauerhaft bestehen.
Wie diese Anziehungskräfte entstehen, lässt sich am einfachsten am Beispiel von zwei Atomen erklären. Das Gesagte gilt aber ebenso für Moleküle oder deren Teilbereiche!
Die negativ geladenen Elektronen in einem Atom sind in ständiger Bewegung. Dadurch kann es kurzfristig zu einer ungleichmäßigen Ladungsverteilung innerhalb des Atoms kommen.
Das Atom wird so für einen kurzen Moment zu einem temporären (also kurzzeitigen) Dipol – es entstehen positive und negative Teilladungen (Partialladungen).
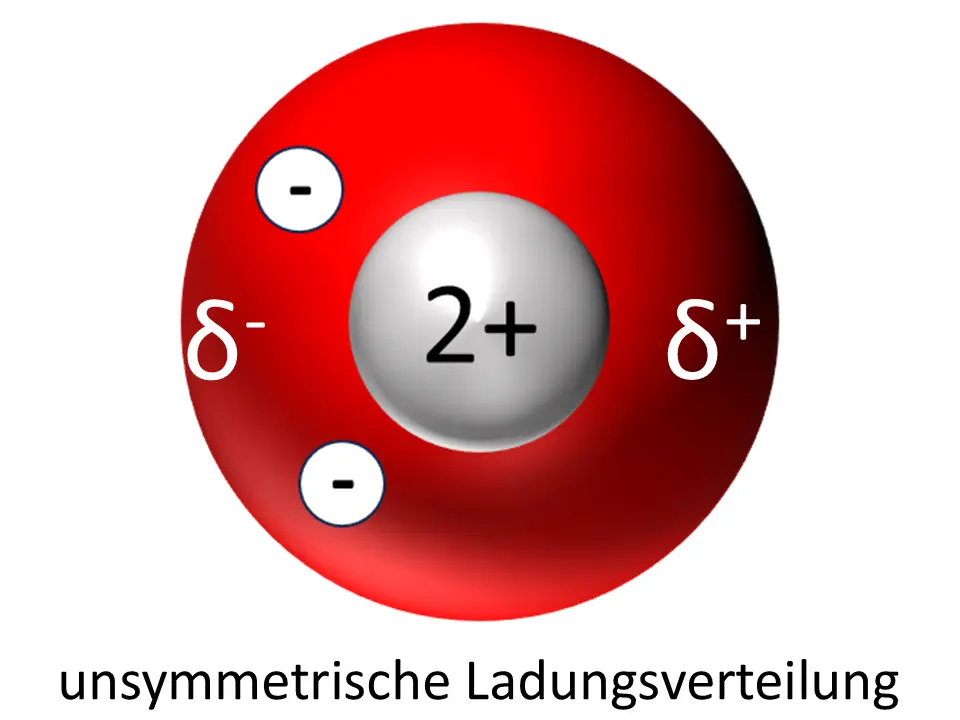
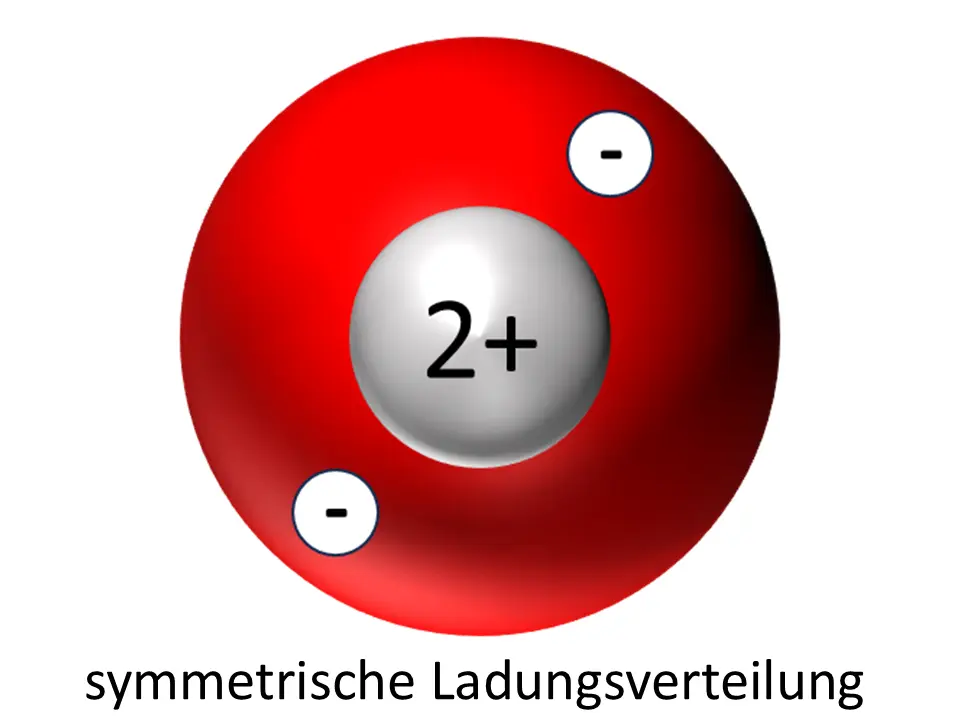
In einem Heliumatom ist die Ladung symmetrisch verteilt, im anderen hat sich zufällig ein temporärer Dipol gebildet.
Induzierter Dipol
Nähern sich nun zwei Atome genügend an, kann Folgendes passieren: Ein temporärer Dipol trifft auf ein ungeladenes Atom und bewirkt (induziert) bei diesem ebenfalls einen Dipol. So entsteht eine Anziehungskraft zwischen den beiden Atomen – diese wird als van-der-Waals-Kraft bezeichnet.
Die elektrische Anziehung ist allerdings schwach und wirkt nur über eine sehr kurze Entfernung.
Damit die van-der-Waals-Kraft überhaupt wirksam werden kann, müssen sich zwei Atome oder Moleküle sehr nahe kommen. Das funktioniert umso schlechter, je mehr Bewegungsenergie die Teilchen besitzen – also je höher die Temperatur in der Stoffprobe ist.
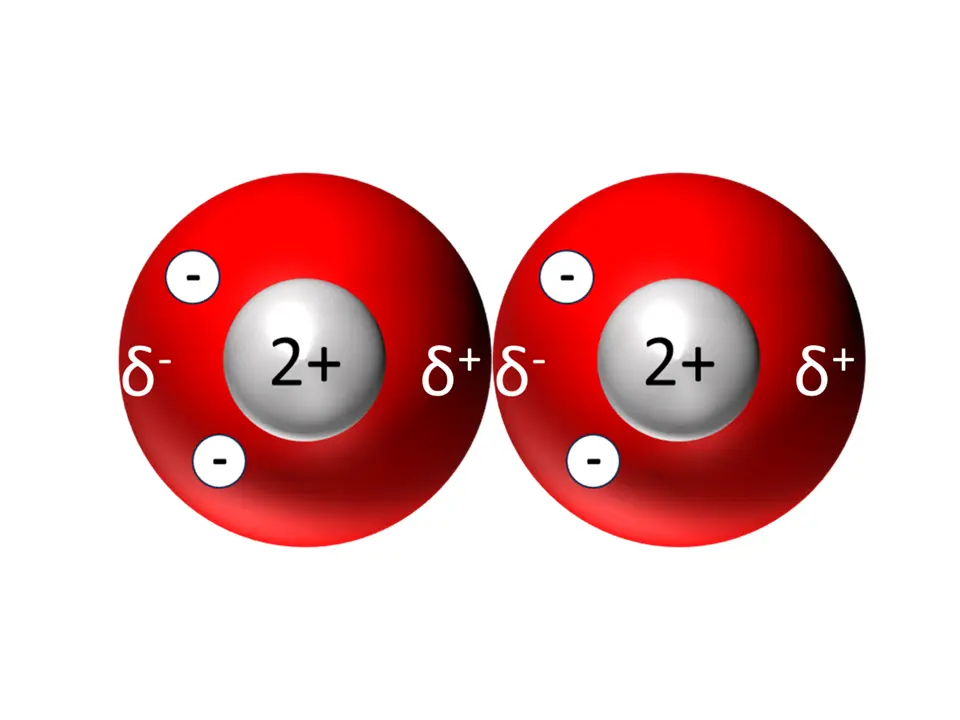
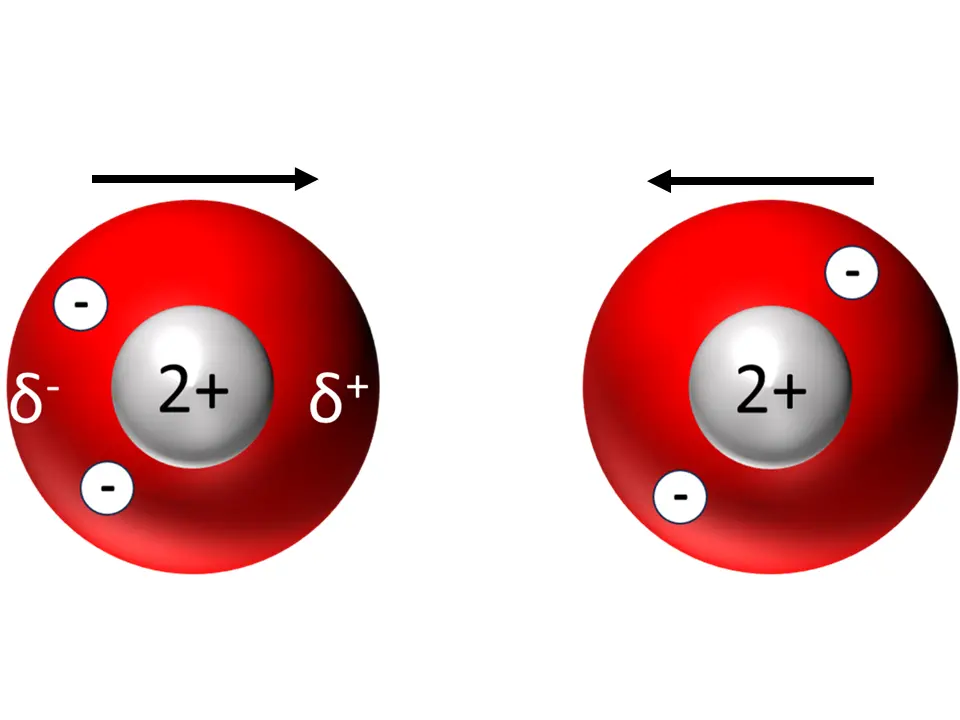
Der temporäre Dipol im Atom links sorgt bei Annäherung dafür, dass in einem Nachbaratom rechts ebenfalls kurzzeitig ein Dipol entsteht. Beide Atome ziehen sich nun kurzzeitig an.
Stärke der Van-der-Waals-Kraft
Grundsätzlich nimmt die Van-der-Waals-Kraft mit wachsender Masse und Oberfläche der Moleküle zu. Deshalb kann sie bei großen, unpolaren Molekülen oder entsprechenden Molekülteilen sehr stark werden.
Geckos können scheinbar mühelos glatte und senkrechte Oberflächen erklimmen. Grund dafür ist die Van-der-Waals-Kraft.7
Geckos nutzen übrigens die van-der-Waals-Kraft, um an senkrechten Flächen zu haften. Die Haftballen an ihren Füßen sind mit feinsten Härchen besetzt, was die Kontaktfläche enorm vergrößert. So entstehen genügend starke van-der-Waals-Kräfte, dass sie selbst an senkrechten oder sehr glatte Oberflächen „haften“.
Literaturtipp zum Weiterlesen: Gecko- Haftapparat bei max-wissen.de – aus der Forschung direkt in die Schule
Die Siedetemperaturen der Edelgase im Vergleich
Der Zusammenhang von zunehmender Van-der-Waals-Kraft bei zunehmender Elektronenzahl bzw. Polarisierbarkeit wirkt sich auch auf die Siedetemperaturen der Edelgase aus.
Siedetemperaturen von Helium bis Xenon im Vergleich.8



