Moleküle sind wichtig!
Das Leben beruht auf Molekülverbindungen
Alle Lebewesen bestehen überwiegend aus Molekülen! Wie sind solche Moleküle prinzipiell aufgebaut?
Z. B. die DNA oder Proteine. Das sind riesige Moleküle. Wir fangen einmal ganz klein an. Keine Sorge – du wirst das direkt verstehen!
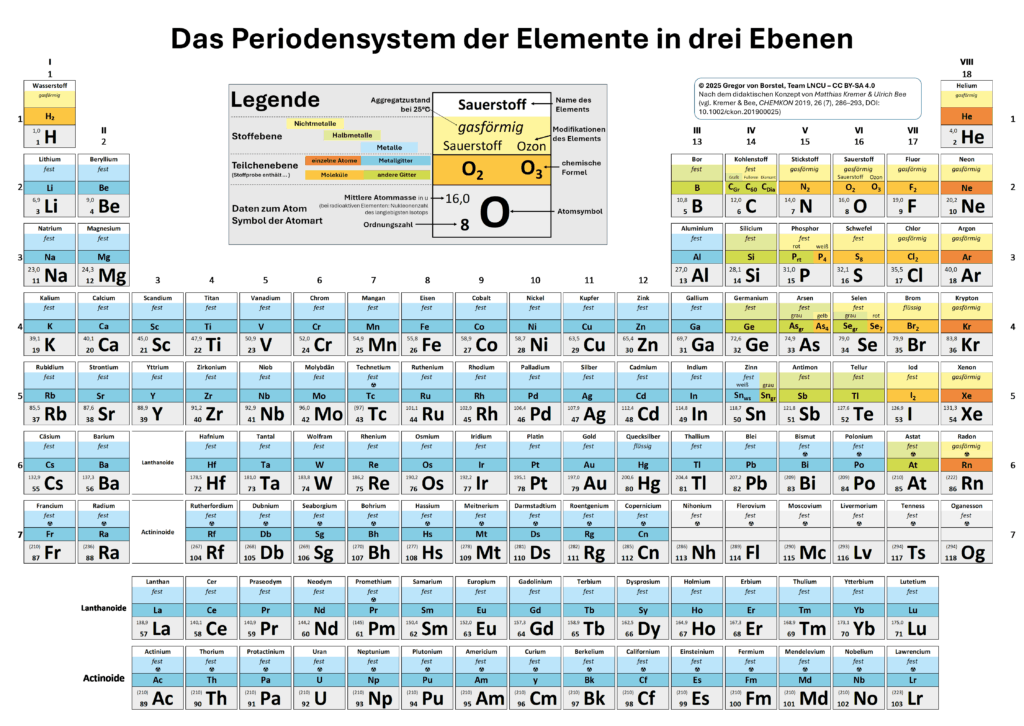
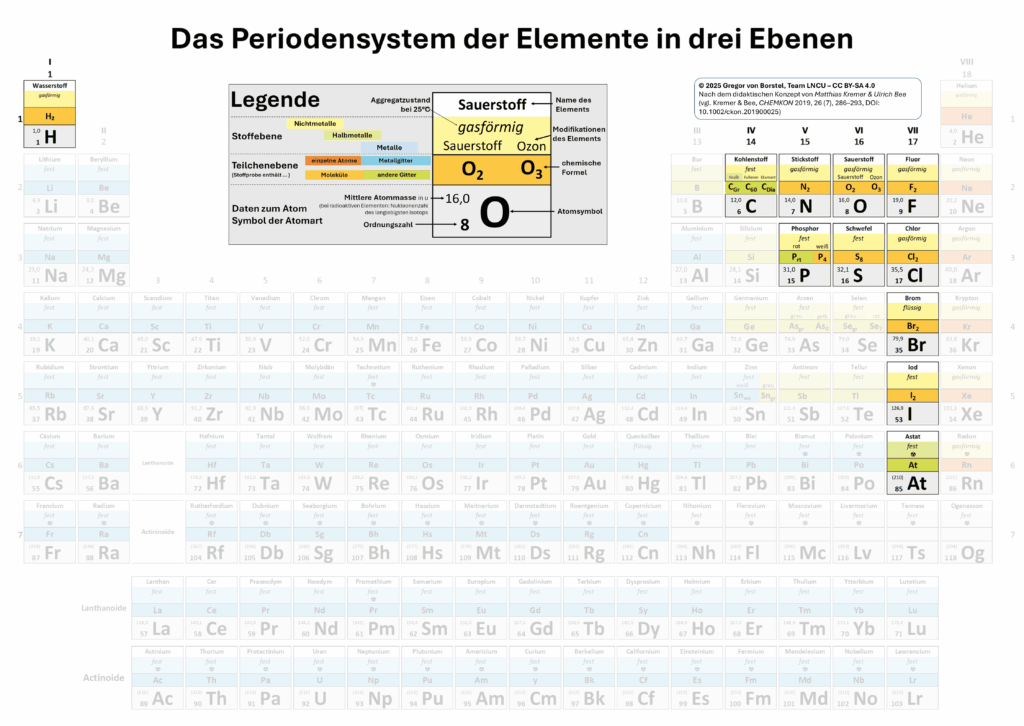
Wirf noch einmal einen Blick in das PSE3. Suche heraus, welche Art von Elementen auf Teilchenebene Moleküle bilden. Schau genau hin: Aus wie vielen Atomen sind die Moleküle der Elemente der 2. Periode zusammengesetzt?
Ein erneuter Blick in das PSE
Das PSE³ kennst du bereits aus den Materialien zu den Elementfamilien, der metallischen Bindung und den Edelgasen.
Aufgaben
Wir arbeiten zuerst gemeinsam mit M2 ein Beispiel für die Bildung eines Moleküls durch. Du hast drei Aufgaben dabei:
- Vollziehe nach, was bei der Bildung des Wasserstoffmoleküls auf subatomarer Ebene passiert.
- Deute die Farbcodierung. Was bedeuten die verwendeten Farben?
- Es entsteht H2, aus dem sich aber dann nicht H3 etc. bildet. Suche nach einer plausiblen Erklärung dafür. Betrachte jedes Atom im Molekül und mache eine Aussage zur Elektronenkonfiguration bei diesem Atom.
Das einfachste Beispiel
In Molekülen teilen sich Atome Elektronen
Stellen wir uns vor, Nichtmetallatome treffen aufeinander. Was wird passieren?
Nun, wenn ihre Valenzschale noch nicht ganz gefüllt ist, teilen sie sich mit anderen Atomen ein oder mehrere Valenzelektronen. Die miteinander geteilten Elektronen bilden eine Verbindung zwischen den Atomrümpfen und halten so die Atome zusammen. Dadurch entstehen kleine Moleküle mit einer bestimmten Gestalt!
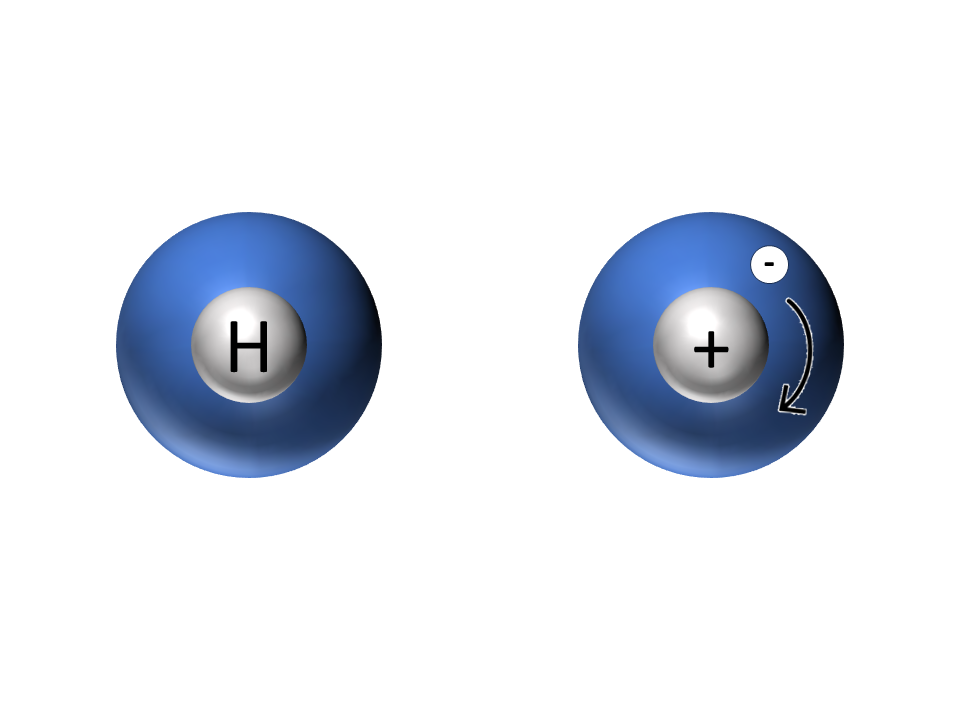
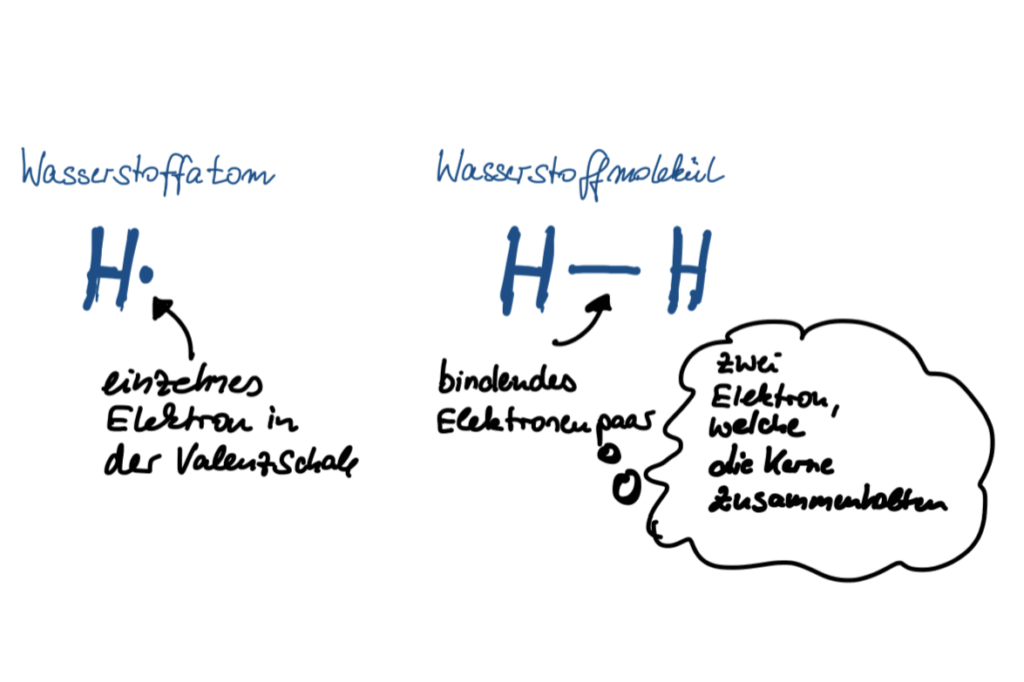
Das klingt komplizierter als es ist. Stellen wir es uns einmal an einem einfachen Beispiel vor: dem Wasserstoffatom. Das kann man verschieden darstellen.
Zwei Darstellungen eines Wasserstoffatoms1
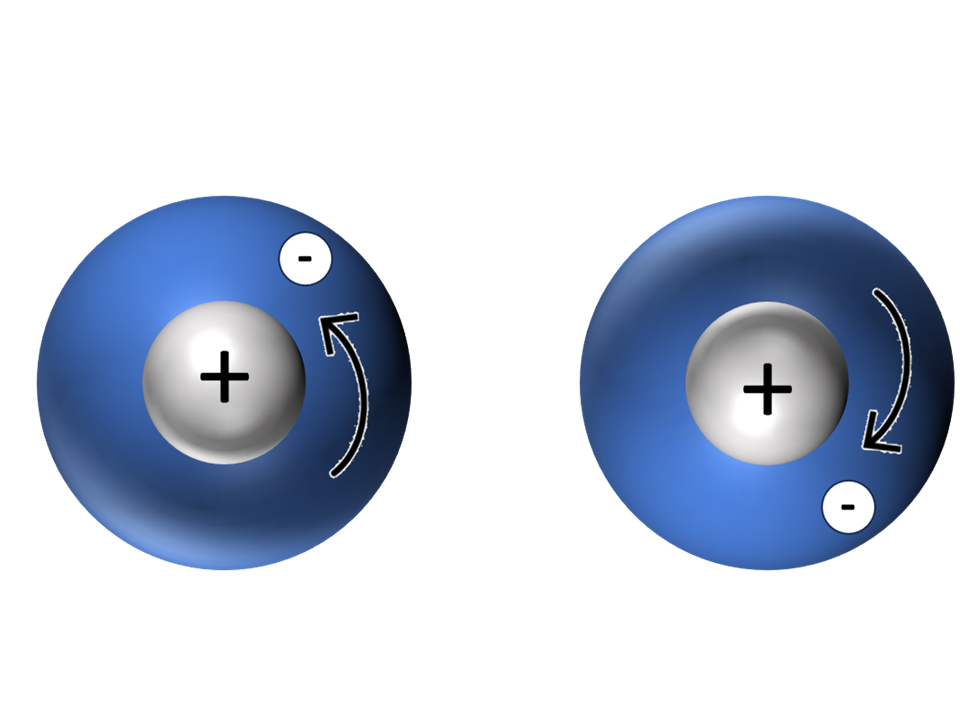
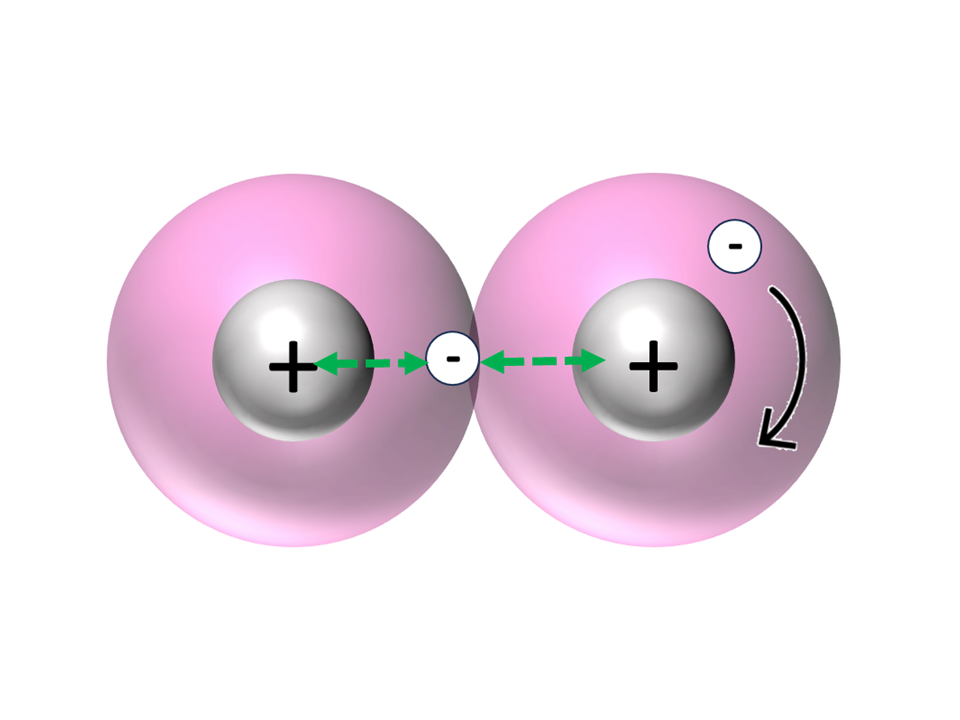
Treffen sich zwei Wasserstoffatome ...
Modellvorstellung – was passiert, wenn sich zwei Wasserstoffatome annähern?2
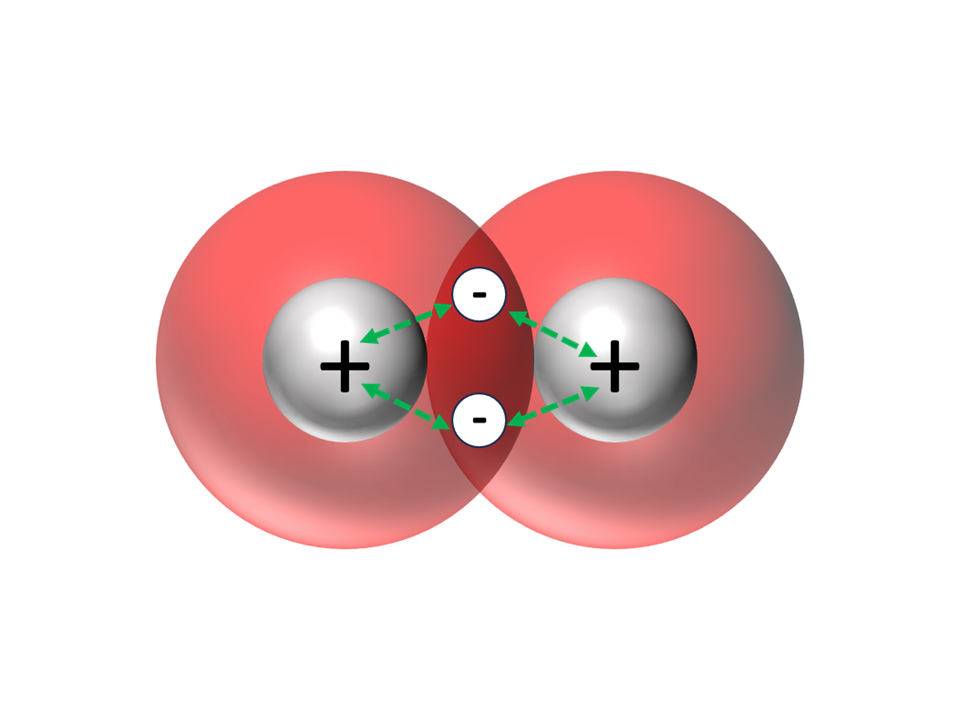
Ein "fertiges" Wasserstoffmolekül in verschiedenen Darstellungen
Gleiches Prinzip - anderes Atom - Kugelwolkenmodell
- Mache dich (noch einmal) mit dem Kugelwolkenmodell vertraut.
- Lasse im Modell ein Fluormolekül entstehen. Zeichne dazu zunächst zwei Fluoratome, die in einem zweiten Bild zu einem Fluormolekül werden. Wenn du nicht räumlich zeichnen kannst, zeichne es einfach „planar“.
- Beschreibe und erkläre: Was ist deiner Abbildung ähnlich zum Wasserstoffmolekül? Was ist neu? Erklärt das Modell die Tatsache, dass das Fluormolekül die Zusammensetzung F2 hat?
- Schreibe das Fluormolekül in der Lewisformel-Darstellung auf.
- Baue es mit dem Molekülbaukasten. Mache ein Foto für deine Unterlagen. Benenne, was wodurch dargestellt wird und was vielleicht fehlt.
Molekülbau für Fortgeschrittene
- Mache es nun das Gleiche für das Sauerstoffmolekül und das Stickstoffmolekül. Schaue zuvor in das PSE3 aus wie vielen Sauerstoffatomen (Stickstoffatomen) sich im einfachsten Fall ein Sauerstoffmolekül (Stickstoffmolekül) bildet?
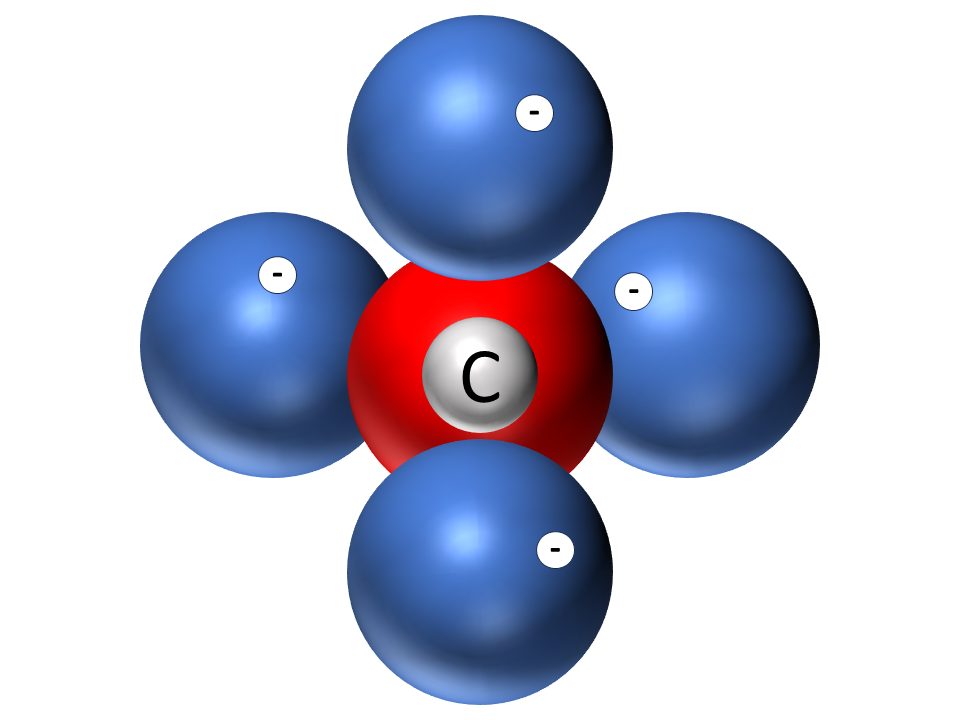
- Betrachte das Kohlenstoffatom im Kugelwolkenmodell und auch im Modell aus dem Molekülbaukasten. Erkläre, warum es kein C2-Molekül gibt.
Anregungen
Vielleicht hilft es dir bei der Aufgabe, wenn du folgende Darstellung eines Sauerstoffmoleküls siehst, die mit einem Molekülviewer basierend auf real gemessenen Daten erstellt wird.
Vielleicht hilft es dir bei der Aufgabe, wenn du folgende Darstellung eines Stickstoffmoleküls siehst, die mit einem Molekülviewer basierend auf real gemessenen Daten erstellt wird.
Nachgedacht
- Erkläre abschließend, warum das Kugelwolkenmodell hilfreich sein kann, wenn man erläutern oder voraussagen will, wie ein Molekül zusammengesetzt ist.
Die Nichtmetalle der 2. Periode im Kugelwolkenmodell
Weiteres
Im Kugelwolkenmodell sind die Valenzschalen in „Wolken“ (Räume) unterteilt und diese Räumen als bereits vollbesetzt oder noch nicht voll besetzt gekennzeichnet.
Die Valenzschale von Wasserstoff und Helium besteht aus einer Wolke mit maximal zwei Elektronen.
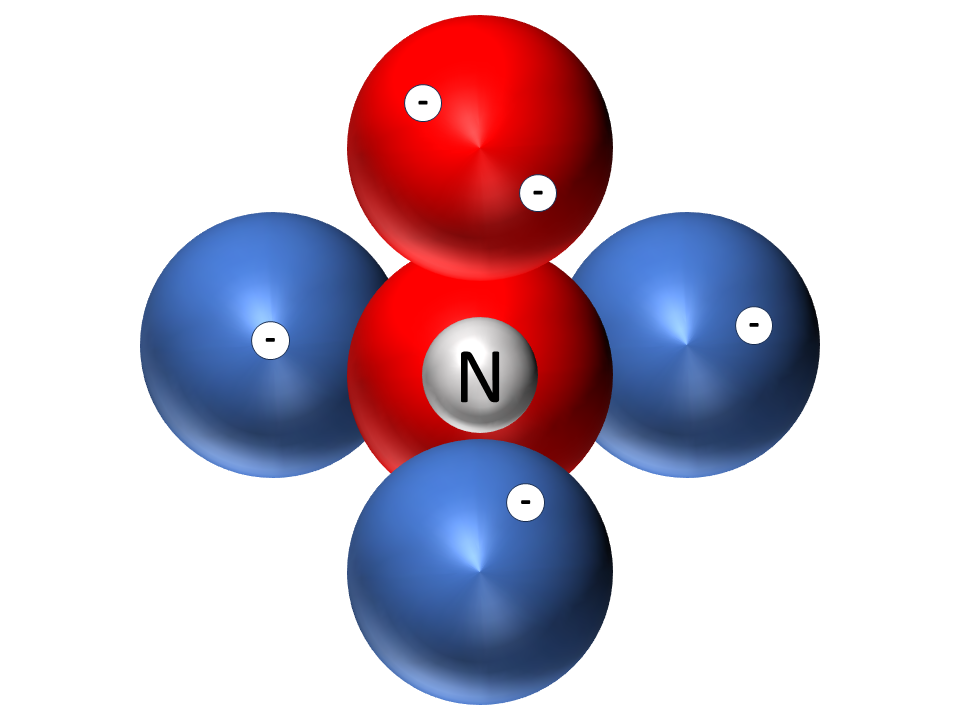
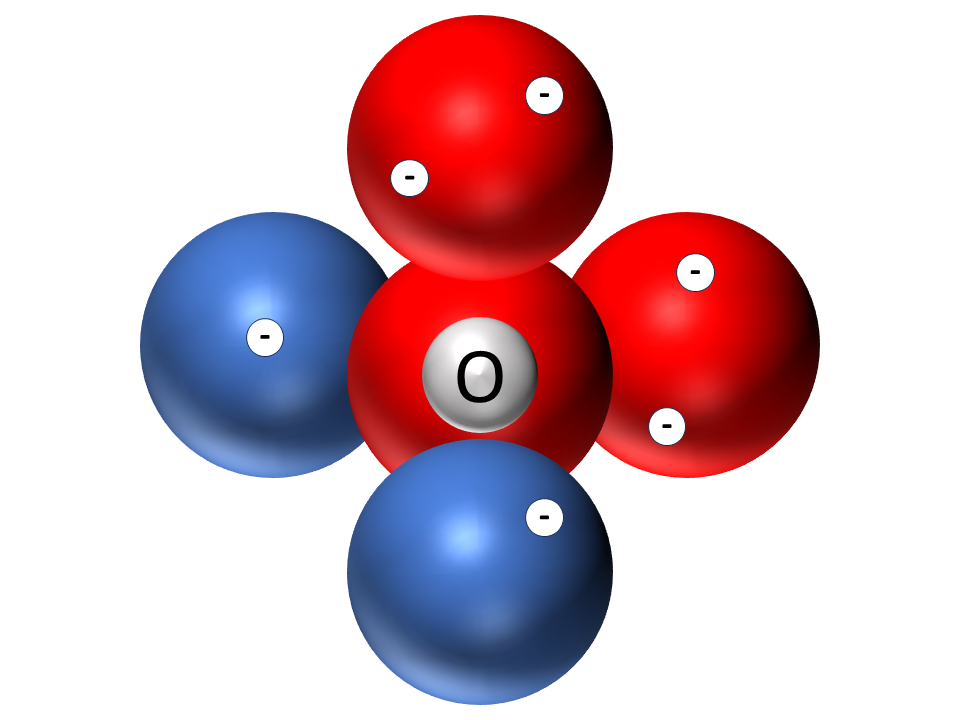
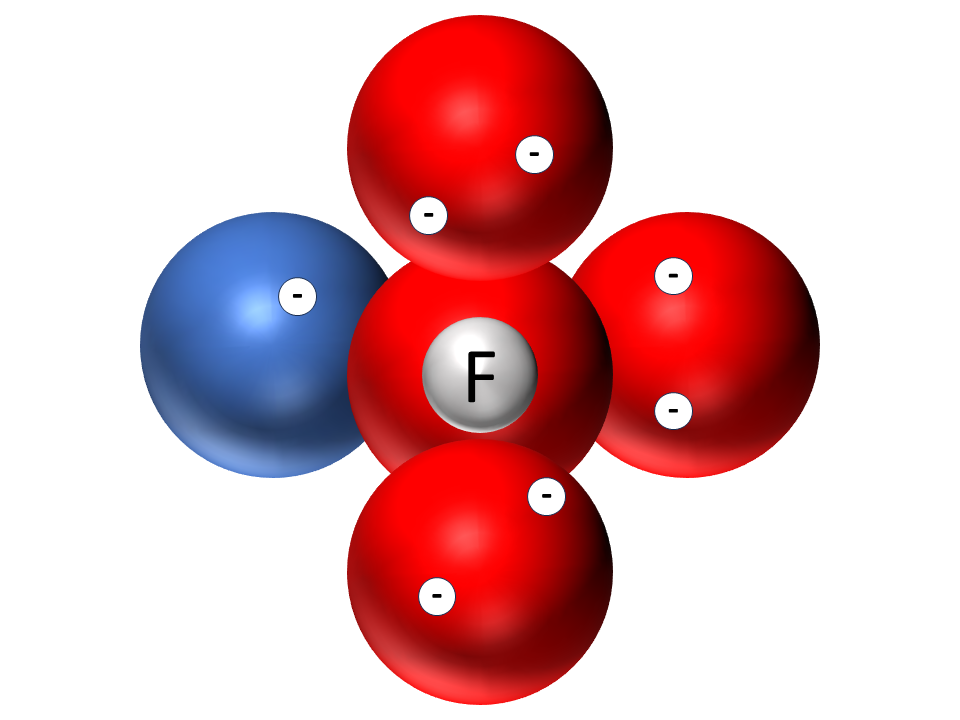
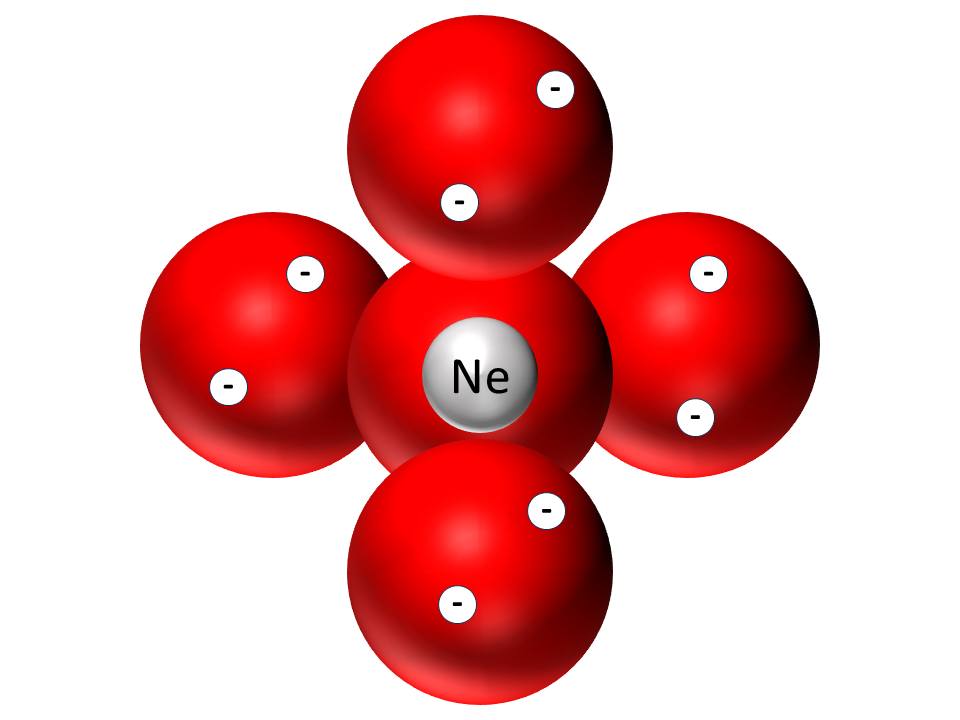
Die Valenzschalen aller anderen Nichtmetallatome der 2. Periode Abb. 4 sind unterteilt in vier Räume in Kugelwolkenform. In jede Kugelwolke passen maximal 2 Elektronen.
Weiteres
Kugelwolkenmodelle der Atome von Helium, Kohlenstoff, Stickstoff, Sauerstoff, Fluor und Neon1
Lust auf mehr?
- Erstelle mit dem Molekülbaukasten Modelle der Moleküle mit den Summenformeln H2O, CO2, NH3 oder CH4.
- Zeichne die Lewisformeln für alle diese Moleküle.
- Prüfe, ob jedes Atom in deinen Molekülmodellen „Edelgaskonfiguration“ erreicht hat.
Moleküle zerbrechen und bilden sich neu
Weiteres
Elektronenpaarbindungen können prinzipiell auch wieder brechen. Es bedarf dazu aber Energie. Auf diese Weise können die von uns betrachteten Moleküle, die nur aus einer Atomsorte bestehen, „zerbrechen“ und es können auch Moleküle mit Atomen mehrerer Elemente bilden. Für das Leben, wie wir es kennen, unerlässlich!
Das Aufbrechen und Neubilden von Molekülen passiert permanent. In Pflanzen entstehen z. B. aus Kohlenstoffdioxid und Wasser und Energie aus der Sonne Glucose und Sauerstoff. Im Körper wiederum entstehen wieder Kohlenstoffdioxid und Wasser und wir nutzen die freigesetzte Energie.
Weiteres
Hier mal ein simples Beispiel: die sogenannte Knallgasprobe. Wasserstoff und Sauerstoff reagieren miteinander. Die Moleküle der Elemente zerbrechen dabei und es bilden sich neue Moleküle mit stabileren Elektronenpaaren: Wassermoleküle.
Knallgasprobe3