Wellness aus dem Toten Meer?
Was steckt in Badesalz?
Badesalz aus dem Toten Meer wird seit Jahren als besonderes Wellness-Produkt verkauft. Es soll die Haut pflegen, die Muskeln entspannen und ein „Spa-Gefühl“ nach Hause bringen. Viele Menschen greifen deshalb gezielt zu solchen Produkten – oft, ohne genauer auf die Inhaltsangaben zu achten.
Ein Blick auf die Verpackung zeigt jedoch: Dort ist genau aufgelistet, was im Badesalz enthalten ist. Neben geläufigen Elementnamen wie Natrium oder Calcium erscheinen auch weniger bekannte Fachbegriffe sowie chemische Symbolschreibweisen.
Was steckt hinter diesen Angaben? Und was sagt diese Liste eigentlich über den Stoff aus, der sich in der Packung befindet?
Weiteres
Badesalzmischung aus verschiedenen Salzen.1
Welche Salze könnten in diesem Badesalz enthalten sein?
Jede Tischgruppe erhält ein Kation vom Etikett des Badesalzes M1 zugeteilt.
- Benennt mögliche Salze, indem ihr
- sinnvolle Kombinationen aus eurem zugeteilten Kation mit jedem Anion vom Etikett bildet,
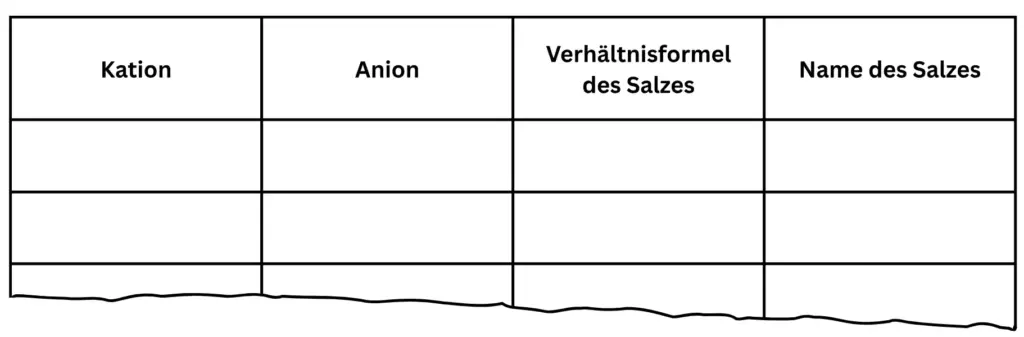
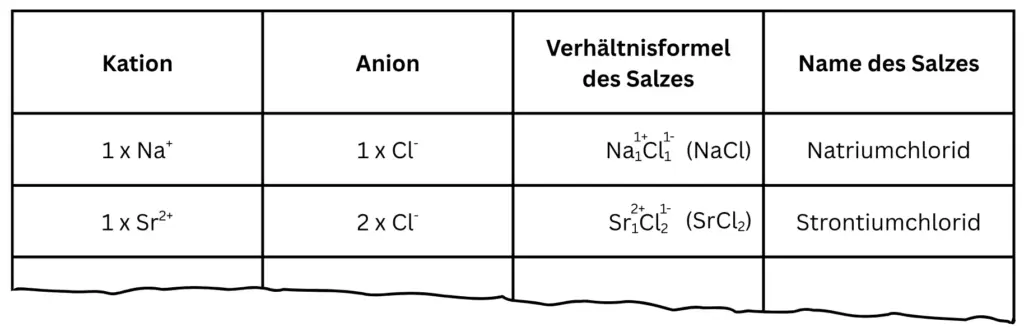
- zu jedem kombinierten Salz die Verhältnisformel sowie den Namen des Salzes notiert.
- Haltet eure Ergebnisse tabellarisch fest und orientiert euch dabei an den Tabellen aus den Anregungen.
Alles klar?
Weiteres
Erkläre warum die Formel von Calciumchlorid CaCl2 lautet und nicht CaCl?
Weiteres
Die folgenden Verhältnisformeln von Salzen sind fehlerhaft. Überprüfe und korrigiere sie:
Begründe deine Korrekturen kurz fachsprachlich.
Weitergedacht
- Mache dich mit den Namen und Summenformeln einzelner Molekül-Ionen vertraut. Versuche alleine anhand der wenigen Beispiele eine Regelmäßigkeit bei der Benennung zu erkennen.
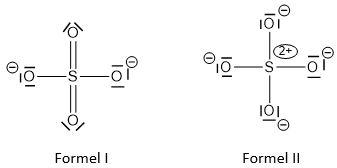
- Wenn du magst, schau dir einmal ausgewählte Strukturformeln an und erkläre, wie man anhand der Strukturformel von Sulfat auf die Ladung des Moleküls schließen kann.
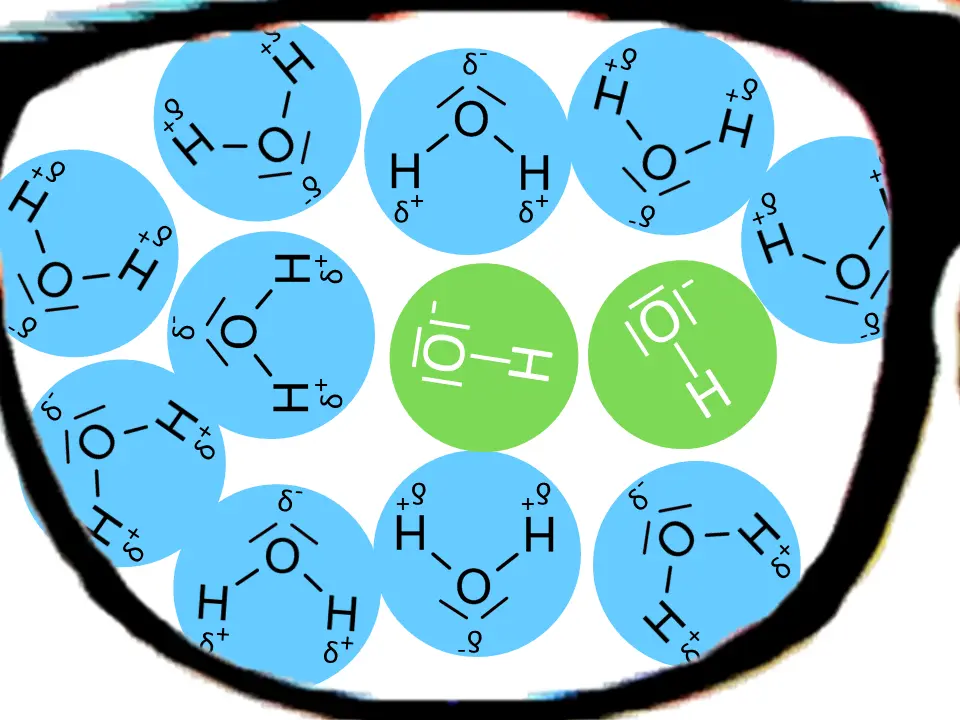
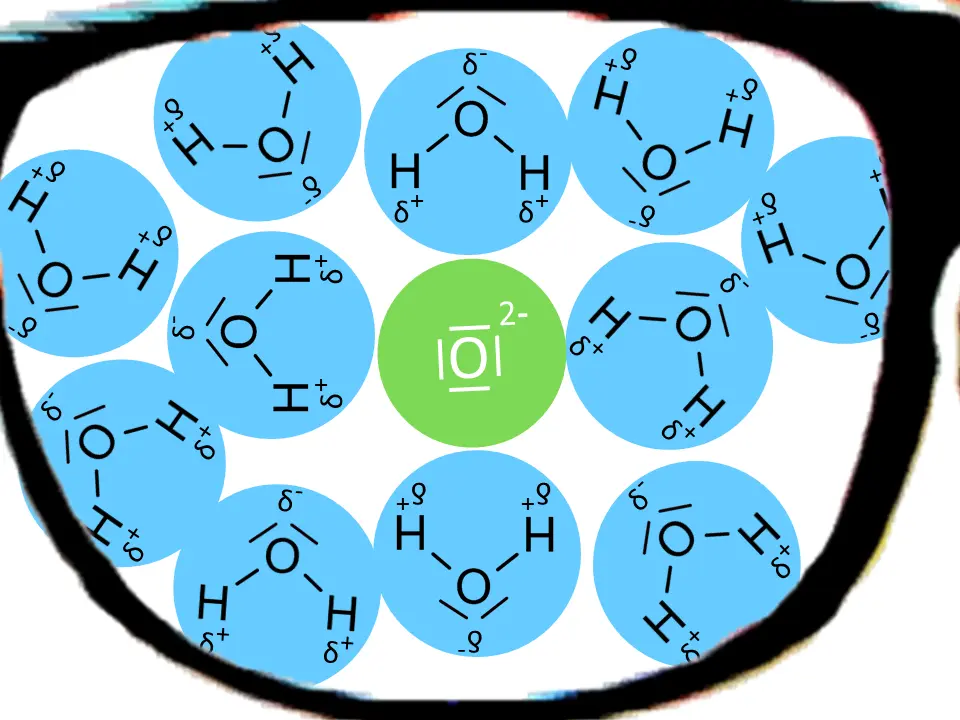
- Erläutere mit Hilfe von Abb. 3, warum Oxid-Ionen in wässriger Lösung nicht vorkommen.