Was wäre zu erwarten?
Titriert man Salzsäure mit Natronlauge, so verändert sich mit Zugabe von immer mehr Lauge die Leitfähigkeit der Lösung. Dies kann man mit einem geeigneten Gerät, einem so genannten Konduktometer, messen und aufzeichnen.
Weiteres
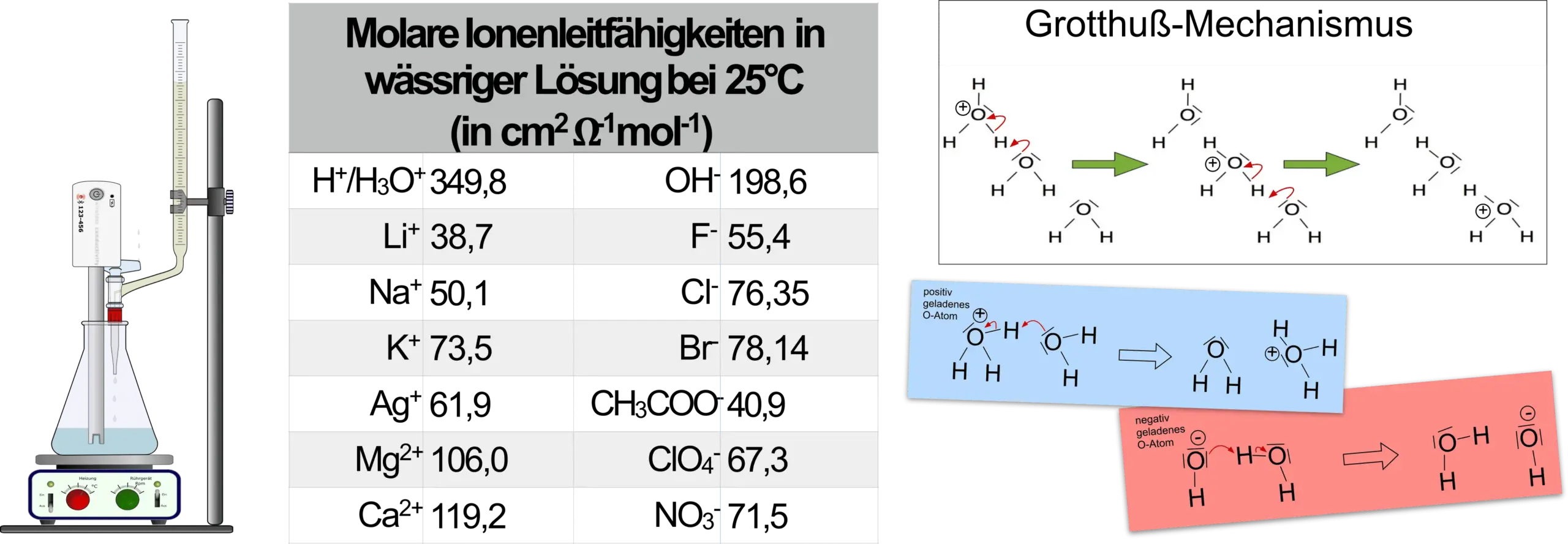
Leitfähigkeiten verschiedener Ionen und der Grotthuß-Mechanismus. 1
Aufgaben
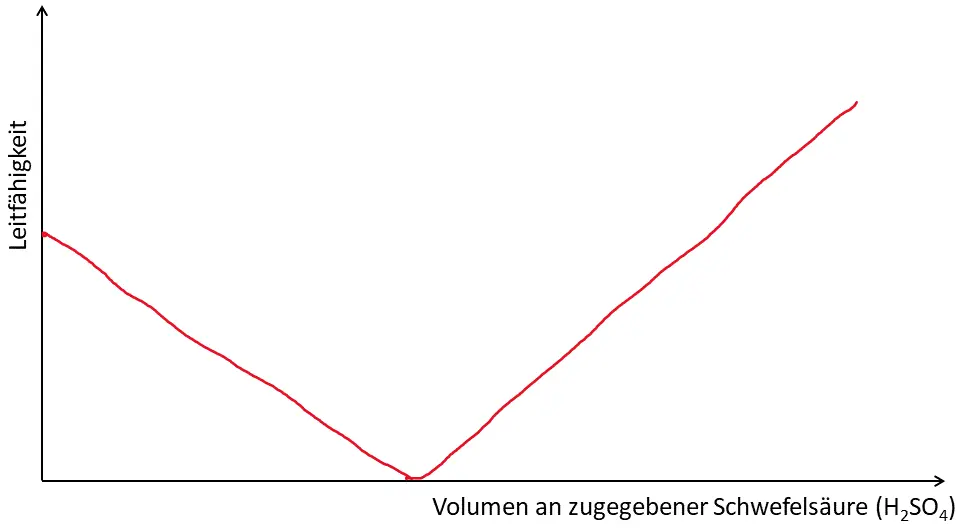
- Stellen Sie mittels M1 eine begründete Vermutung auf, wie der Kurvenverlauf bei einer Salzsäure-Natronlauge-Titration aussehen könnte, wenn anstelle des pH-Wertes die Leitfähigkeit der Lösung gemessen wird.
- Prüfen Sie ihre Vermutung, indem Sie Versuch V1 durchführen.
- Werten Sie ihre Titrationskurve aus, indem Sie…
- Passende Reaktionsgleichungen aufstellen
- Prägnante Punkte markieren und benennen
- Abschnitten im Graphen die in der Lösung befindlichen Ionen zuordnen
- Den Verlauf des Graphen mit Hilfe der Ionenleitfähigkeiten aus Abb. 1 erklären
Konduktometrische Säure-Base-Titration
Materialien
- Schutzbrille
-
Stativmaterial
- Stativ, Stativklemmen, Stativmuffen
-
Bürette
- Nur in Versuchsaufbau B in Abb. 2
-
Spritzentechnik
- Nur in Versuchsaufbau A in Abb. 2
- 50 mL Messzylinder
- Weithals-Erlenmeyerkolben oder Becherglas
- Magnetrührer mit Rührfisch
Chemikalien
- Salzsäure < 0,05 mol/L
-
Essigsäure 0,1 mol/L
- Alternativ zur Salzsäure
- Natronlauge 0,1 mol/L
- dest. Wasser
Mit einer Konzentration von weniger als 0,05 mol/L für Salzsäure oder 0,1 mol/L für Essigsäure und einer Natronlauge mit 0,1 mol/L wird die Messkapazität des Leitfähigkeitsgerätes nicht überschritten.
Durchführung
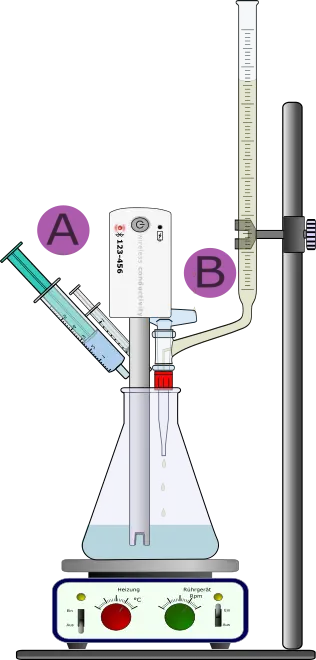
- Apparatur gemäß Abb. 2 aufbauen.
- 50 mL Säure in den Erlenmeyerkolben geben.
- Leitfähigkeitsmessgerät in der Säure fixieren, sodass dieses tief genug eintaucht, den Rührfisch jedoch nicht berührt.
- Magnetrührer einschalten.
- Unter kontinuierlichem Rühren in 1 mL Portionen Natronlauge zugeben und die Leitfähigkeit aufzeichnen. Insgesamt 50 mL Natronlauge zugeben!
Aufräumen
- Gegebenenfalls Reste vereinen und über den Abguss entsorgen.
- Alles mit Wasser spülen und an den Ursprungsort zurückstellen.
Aufbau
Versuchsaufbau. A: Mit Spritzentechnik. B: Mit Bürette. 2
Weitergedacht
- Erläutern Sie das Besondere an der Fällungstitration in M2.
Eine Fällungstitration
Weiteres
Eine Beschriftung.3
Das Löslichkeitsprodukt KL von Bariumsulfat ist sehr sehr klein. In diesem Beispiel fällt Bariumsulfat im Verlauf der Titration als schwerlößliches Salz aus. Wir werden in einer eigenen Sequenz noch einmal genauer auf das Löslichkeitsprodukt schauen!