Inhalte und Bezüge
Auszug KLP NRW
„Organische Stoffe verschiedener Stoffklassen spielen im Leben des Menschen in mehrfacher Hinsicht eine entscheidende Rolle. Neben vielfältigen Anwendungen im Alltag, beispielsweise als Lösemittel und Inhaltsstoffe in kosmetischen Produkten, nehmen sie als Genussmittel oder Konservierungsstoffe auch Einfluss auf die Gesundheit. Ein tiefergehendes Verständnis solcher Zusammenhänge bedarf einer Durchdringung grundlegender chemischer Sachverhalte, auch im Hinblick auf die Ausbildung eines fachlich fundierten Urteilsvermögens. Dieses trägt zur Entscheidungsfindung beispielsweise in Fragen der eigenen Gesunderhaltung ebenso bei wie in Fragen der Umweltverträglichkeit und unterstützt ein kritisches Hinterfragen der Darstellung chemischer Zusammenhänge in unterschiedlichen Medien.“1
Schwerpunkte NRW
- funktionelle Gruppen verschiedener Stoffklassen und ihre Nachweise: Hydroxygruppe, Carbonylgruppe, Carboxygruppe und Estergruppe
- Eigenschaften ausgewählter Stoffklassen: Löslichkeit, Schmelztemperatur, Siedetemperatur
- Elektronenpaarbindung: Einfach- und Mehrfachbindungen, Molekülgeometrie (EPA-Modell)
- Konstitutionsisomerie
- intermolekulare Wechselwirkungen
- Oxidationsreihe der Alkanole: Oxidationszahlen
- Estersynthese2
Advance Organizer
Inhalte, konkretisierte Kompetenzerwartungen, Anmerkungen
Der Alkoholkonsum und seine Folgen
Neben der rein stofflichen oder molekularen Betrachtung von Ethanol birgt das Themenfeld viele weitere Annäherungsmöglichkeiten!
Der offene Einstieg über „Genussmittel vs. Krankmacher“ ist sinnvoll, denn viele Jugendliche erleben oder beobachten in ihrem Alter die Folgen des Alkoholkonsums. Das Material „Kenn-dein-Limit“ erschließt dieses Themenfeld und die Schüler:innen bearbeiten es parallel auch zu Hause.
Eine erschöpfende Bearbeitung des Internetauftrittes der Bundeszentrale für gesundheitliche Aufklärung (BzgA) ist nicht intendiert. Der offene Einstieg darf zur Beschäftigung und zum gezielten Fragen anregen.
Hefen produzieren Ethanol
Wie entsteht Alkohol, was ist Gärung, warum macht Hefe dies?
Ein Gärungsversuch wird angesetzt, der parallel immer wieder betrachtet werden kann. Parallel lenkt sog. „Federweißer“ den Blick auf die Hefe als Produzenten und die Gärungsbedingungen.
Energiegewinn? Bildung neue (polarer) Bindungen!
Über den Nachweis des entstehenden Kohlenstoffdioxids, den Geruch oder z. B. fakultativ auch die Dichteveränderung wird zunächst die stoffliche Veränderung betrachtet.
Aus der Frage nach der Sinnhaftigkeit des anaeroben Stoffwechsels ergibt sich ein Wechsel auf die molekulare Ebene und einer tiefergehenden Betrachtung des Energie (hier „ATP“)-Gewinns im Vergleich von aerobem und anaerobem Abbau.
Der Energiegewinn wird hier vereinfachend mit der Bildung kleinerer Moleküle und der Neuknüpfung (nun polarer) Bindungen begründet, um immanent fachliche Aspekte aus der Sekundarstufe I wie polare Elektronenpaarbindungen zu wiederholen, die wenig später bei den zwischenmolekularen Wechselwirkungen wichtig werden! Prinzipiell werden dabei auch die Begriffe Entropie und Enthalpie angelegt.
Destillation in der Praxis: Wie gewinnt man Hochprozentiges?
Die Hefe stirbt bereits bei max. 18-Vol% Alkohol ab. Wie kommt man zu einem höheren Volumenanteil an Ethanol? Durchführung einer Destillation mit dem eigenen Gäransatz unter Messung der Temperatur.
Vergleich von Siedekurven: Wasser vs. Ethanol
Unter Verwendung von einfachen und komplexen (hier Lösung aus zwei Substanzen) Siedediagrammen wird der Blick auf den „Nachlauf“ gerichtet. Auf molekularer Ebene werden erneut polare Elektronenpaarbindungen betrachtet und die nahe beieinanderliegenden Siedetemperaturen mit ähnlich starken, aber nicht gleichen Anziehungskräften zwischen den Molekülen mit permanenten Dipolen (hier Wasserstoffbrückenbindungen) erläutert.
Wurde zuvor die Polarität von Bindungen wiederholt, rücken nun daraus resultierende Betrachtungen von Kräften zwischen Molekülen in den Blick. Die Einführung von zwischenmolekularen Wechselwirkungen anhand der Siedetemperaturen (und nicht der Löslichkeit) ist deutlich leichter, da hier nur Kräfte zwischen jeweils gleichen Molekülen betrachtet werden. Ein Einstieg über die permanenten Dipole macht Sinn, da ihre Bildung bereits bekannt ist und einfach nachzuvollziehen ist.
Vergleich von Siedekurven: Methanol vs. Ethanol
Könnte der Vorlauf verworfen werden, da das potenziell tödlich Methanol und Ethanol ähnliche Siedetemperaturen haben? Wieso haben Methanol und Ethanol ähnliche, aber nicht gleiche Siedetemperaturen? Für einer Erläuterung des Sachverhalt müssen dem Prototyp folgend die unpolaren Reste der Moleküle Ethanol und Methanol verglichen und die Van-der-Waals-Kräfte genutzt werden.
Enthält unser Destillat Methanol?
Fakultativ kann man im Destillat neben Ethanol nach Methanol forschen, z. B. mit einem Low-Cost-GC. Anstelle des realen Versuch ist auch eine reine Datenauswertung möglich, z. B. verpackt in einen fiktiven Kriminalfall.
Retentionszeiten und Flächen unter den Peaks werden exemplarisch in den Blick genommen und lassen qualitative und quantitative Aussagen zu.
Gleiches mischt sich mit Gleichem? Genauer hingeschaut!
Hier steht nicht die unterschiedliche Mischbarkeit verschiedener Alkanole mit Wasser im Mittelpunkt, sondern sukzessiv komplexere Mehrphasensysteme teilweise mit Ethanol als Lösemittel.
- Warum mischen sich Wasser und Heptan nicht dauerhaft?
Am Prototyp Wasser/Heptan wird der Phasenbegriff eingeführt und der Wechsel auf die molekulare Ebene geübt.
- Wasser und Heptan als Lösemittel
Das Lösen von polaren und unpolaren Farbstoffen in eben diesen Lösemitteln ist gut sichtbar und bringt je eine weitere Komponente hinzu.
- Ethanol als universales Lösemittel?
Das Lösen der beiden Farbstoffe in dann nur einer Phase macht klar, dass Ethanol polare wie unpolare Eigenschaften vereint und als grenzflächenaktiver Stoff wirkt.
- Lecithin in Milch, Seifen, Louche-Effekt oder Zellmembranen
Emulgatoren, Tenside, polare und unpolare Moleküle in der Zusammenschau zeigen auf, wie stabile Emulsionen etc. entstehen.
Was bedeutet Oxidation eines Moleküls?
Wie entsteht der Kater? Ethanol wird Ethanal!
Die Entstehung von Ethanal als Beispiel für einen oxidativen Abbau von Alkoholen zu Alkanalen greift den roten Faden der Reihe auf. Deutlich müssen neben dem Wechsel auf den Modellversuch (Begründung z. B. über Toxizität, Reduktion wird erkennbar) auch die Grenzen des bekannten Oxidationsbegriffs (Ionen, Molekülen) herausgestellt werden.
Aromastoffe? Gefahrstoffe? Die Carbonylgruppe in Aldehyden und Ketonen
Mit der Betrachtung der Carbonylgruppe als gemeinsamen Strukturmerkmal auf Teilchenebene können diverse Stoffeigenschaften für exemplarische Vertreter der Alkanale (Propanon, Methanal) und Alkanone recherchiert werden.
Wissen vernetzt: Oxidationsprozesse in Nachweisreaktionen
Materialien zu Nachweisreaktionen (Tollens, Benedict oder Fehling Probe) führen den Oxidationsbegriff und die Stoffklassen zusammen.
Weitere Oxidationsvorgänge lassen Alkansäuren entstehen
Oxidation von primären und sekundären Alkoholen über Alkanale/Alkanone zu Alkansäuren.
Fakultativ: Veresterung
Eine kurze Einheit zur Veresterung kann sich hier anschließen, weil dies logisch passt. Sie kann aber auch an den Beginn der Betrachtung von Gleichgewichtsreaktionen etwas später rücken.
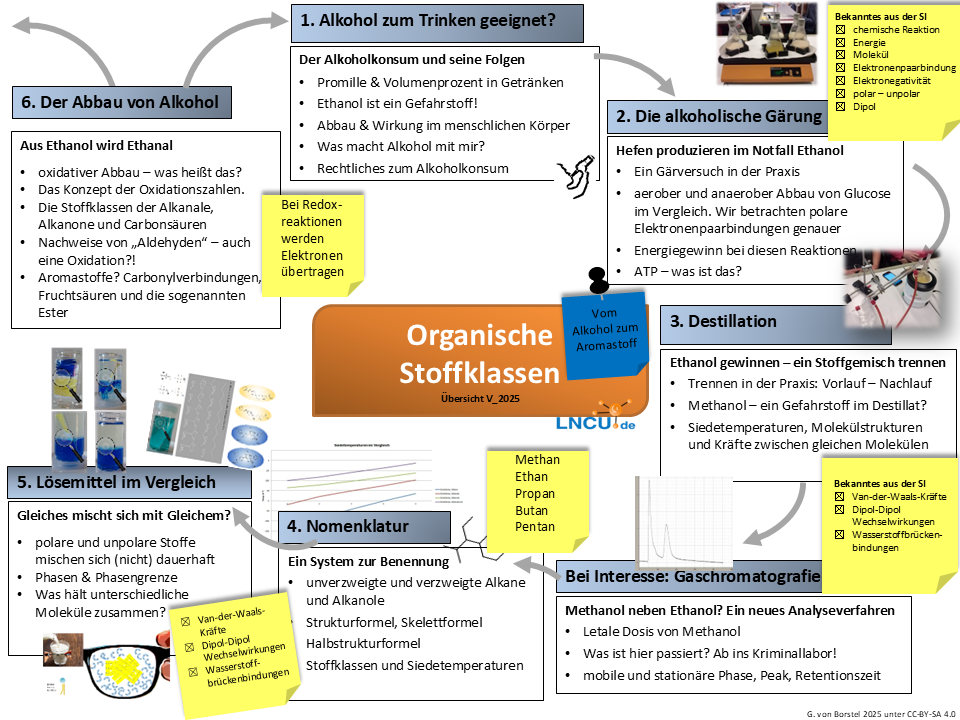
Reihenübersicht und konkretisierte Kompetenzerwartungen.3


