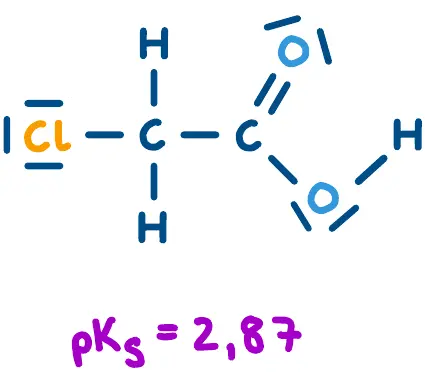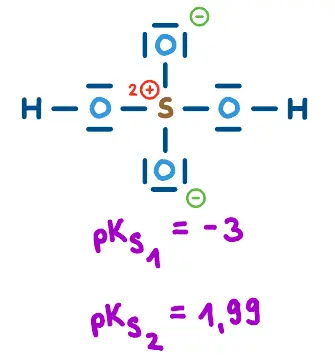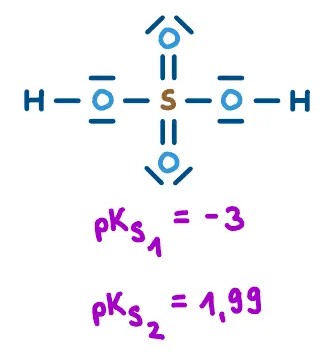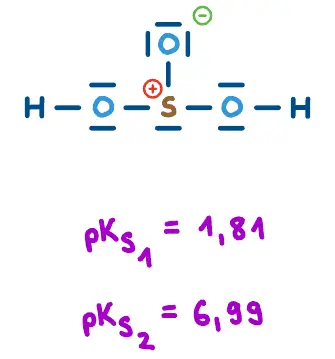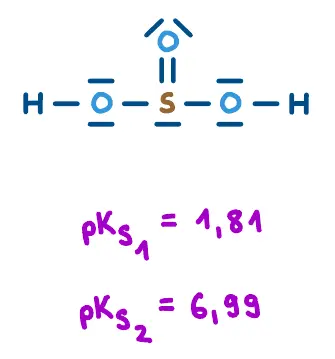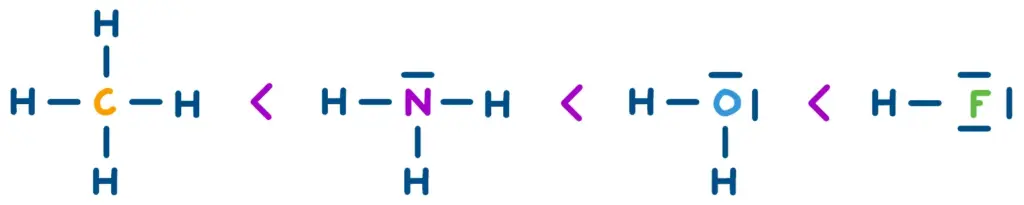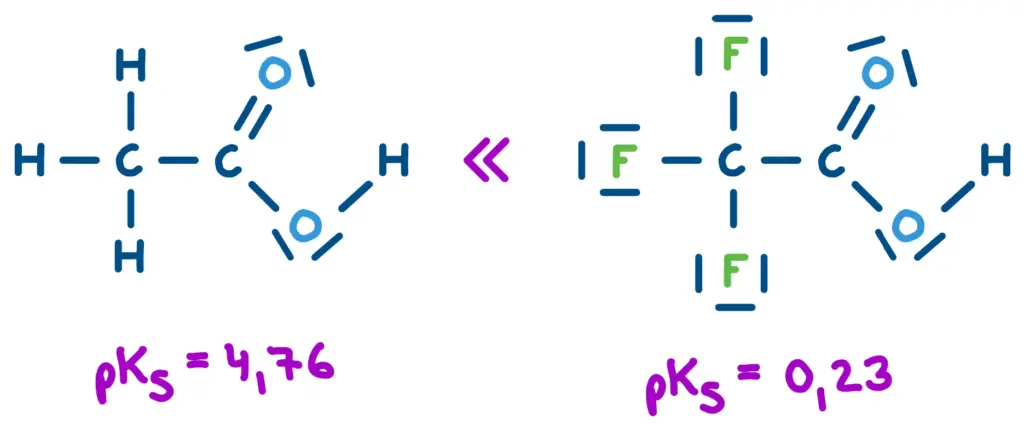Aufgaben
- Gruppenarbeit: Erklären Sie die unterschiedliche Säurestärke der in M1 genannten Beispielpaare, indem Sie …
- die Unterschiede in den Strukturen herausstellen,
- die saure Eigenschaft der schwächeren Säure erklären,
- den Effekt des Unterschieds erläutern.
Material
Allgemein
Eine Säure gibt in Wasser ein Proton (H+-Ion) ab. Wie leicht das gelingt, bestimmen drei miteinander verknüpfte Faktoren.
Polarität der Bindung zum Wasserstoff
Je stärker die positive Teilladung am Wasserstoff-Atom, desto leichter kann ein Proton abgespalten werden.
Bindungsstärke (Dissoziationsenergie)
Schwächere Bindungen lassen sich leichter spalten.
Stabilität der konjugierten Base
Je besser die negative Ladung nach der Abgabe eines Protons stabilisiert wird, desto stärker die Säure.
Starke Säuren kombinieren hohe Bindungspolarität, gut spaltbare Bindungen und eine besonders stabile konjugierte Base.
Sauerstoffsäuren
Sauerstoffsäuren sind Säuren, die eine O-H-Gruppe an ein Zentralatom gebunden haben, oft mit weiteren Sauerstoff-Atomen, z.B. Schwefelsäure H2SO4 oder hypochlorige Säure HOCl.
Warum können Sauerstoffsäuren stark sein? Das elektronegative Zentralatom zieht Elektronendichte über den Sauerstoff-Atomsteg ab. Dadurch wird die O-H-Bindung polarer, die Säurewirkung dadurch stärker. Nach der Protonenabgabe verteilt sich die negative Ladung der konjugierten Base über die gebundenen Sauerstoff-Atome am Zentralatom, oft zusätzlich durch Mesomerie stabilisiert.
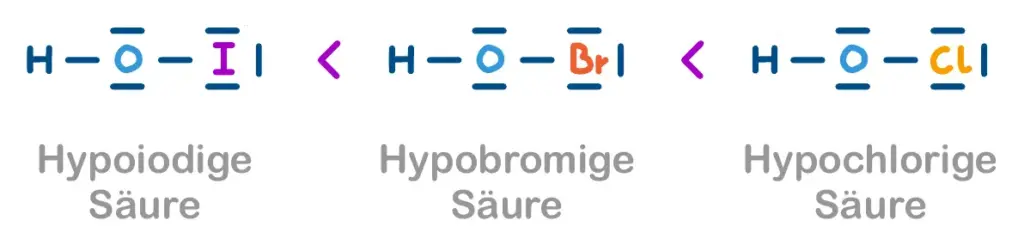
Gleiche O-Anzahl - unterschiedliches Zentralatom
Eine höhere Elektronegativität vom Zentralatom führt zu einer stärkeren Säure, zum Beispiel:
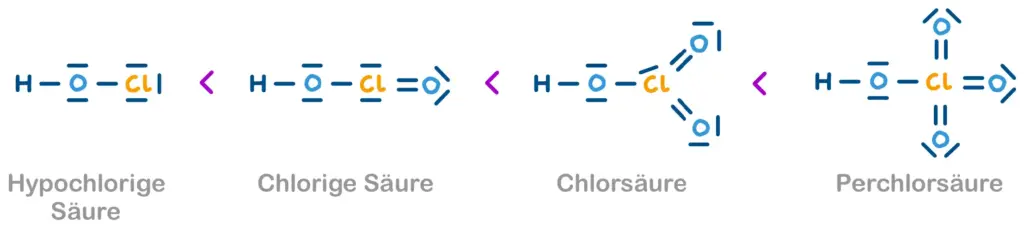
Gleiches Zentralatom - unterschiedliche O-Anzahl
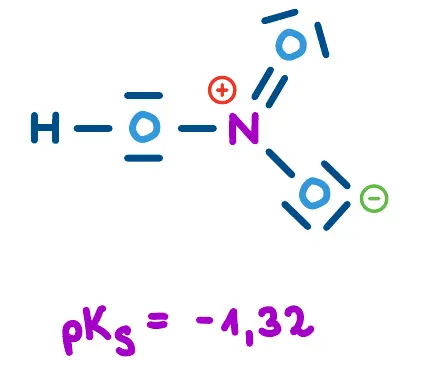
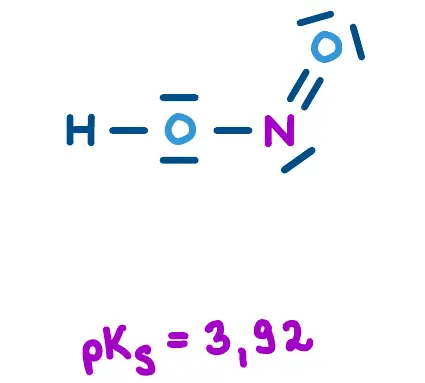
Mehr gebundene Sauerstoff-Atome am Zentralatom Y führen zu einer stärkeren Säure, weil diese zusätzlich Elektronendichte abziehen und die Polarität einer O-H-Bindung am Zentralatom verstärken. Zudem bewirken zusätzliche Sauerstoffatome eine bessere Ladungsverteilung:
Sauerstoffsäuren des Chlors. Mit jedem weiteren Sauerstoffatom am zentralen Chloratom nimmt die Säurestärke von links nach rechts zu.
Warum sind einige O-H-Verbindungen basisch (z.B. NaOH)? Ist das Zentralatom Y ein Metall mit einer sehr geringen Elektronegativität, liegt die Bindung zur OH-Gruppe eher ionisch vor (Na+ OH–). Dann wird leicht OH– (Hydroxid-Ion) abgegeben, der Stoff reagiert basisch.
Ist Y ein Nichtmetall ist die Bindung zur OH-Gruppe kovalent und eine OH– wird nicht freigesetzt. Stattdessen kann ein Proton abgegeben werden, der Stoff reagiert neutral oder sauer.
Elementwasserstoffsäuren
Elementwasserstoffsäuren sind Säuren, die nur aus Wasserstoff und einem weiteren Nichtmetall X bestehen, z.B. HCl. Im Periodensystem zeigen sich Trends innerhalb einer Atomgruppe / Elementfamilie von oben nach unten, oder innerhalb einer Periode von links nach rechts:
Trends innerhalb einer Gruppe (von oben nach unten)
Die Atome werden größer, die H-X-Bindung länger und schwächer. Dadurch nimmt die Säurestärke tendenziell zu.
Die Säurestärke nimmt bei den Halogenwasserstoffsäuren von Fluorwasserstoff über Chlorwasserstoff und Bromwasserstoff bis zum Iodwasserstoff zu. Dies liegt daran, dass das größere Iodatom die Bindung zum Wasserstoff schwächt, wodurch das Proton (H+) leichter abgespalten werden kann.
Trends innerhalb einer Periode (von links nach rechts)
Die Bindungsstärke ändert sich wenig, entscheidend ist die Elektronegativität von X. Mit steigender Elektronegativität wird der gebundene Wasserstoff stärker positiv polarisiert, wodurch die Säurestärke zunimmt.
Obwohl HF sehr polar ist, ist es unter den Halogenwasserstoffen nicht die stärkste Säure, weil die H-F-Bindung ungewöhnlich stark ist.
Kohlenstoff, Stickstoff, Sauerstoff und Fluor befinden sich im Periodensystem innerhalb einer Periode. Die Elektronegativität von X nimmt von links nach rechts zu.
Sonderfall ionische Hydride
In ionischen Hydriden, zum Beispiel Natriumhydrid (NaH), trägt der Wasserstoff eine negative Ladung (H–). In Wasser wirkt es basisch und nicht sauer.
Zusammengefasst: In einer Gruppe dominiert die Bindungsenergie (Schwächer = stärker sauer). In einer Periode dominiert die Polarität (Polarer = stärker sauer).
Carbonsäuren
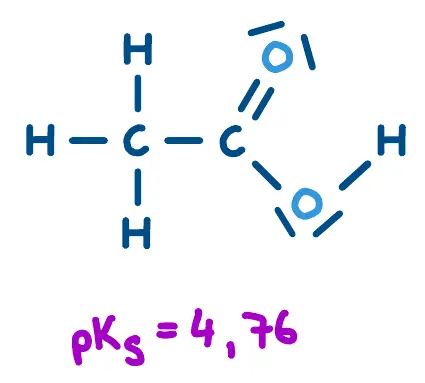
Carbonsäuren sind typischerweise schwache bis mittelstarke Säuren. Der Wasserstoff innerhalb der Carboxygruppe ist für die saure Wirkung verantwortlich.
Zwei Hauptgründe für ihre Säurestärke
- Der Carbonylsauerstoff zieht Elektronendichte ab, wodurch die O-H-Bindung polarer wird.
- Die konjugierte Base ist durch Mesomerie stabilisiert: Die negative Ladung verteilt sich gleichwertig über beide Sauerstoff-Atome in der Carboxylat-Gruppe (R-COO–).
Substituenteneffekte
Elektronenziehende Gruppen (z.B. -NO2, -F, -CF3) verstärken die saure Wirkung der Carboxygruppe (negativer induktiver Effekt bzw. -I-Effekt). Trifluoressigsäure (F3C-COOH) ist deutlich stärker sauer als Essigsäure, weil die CF3-Gruppe einen starken -I-Effekt aufweist.
Mesomerie
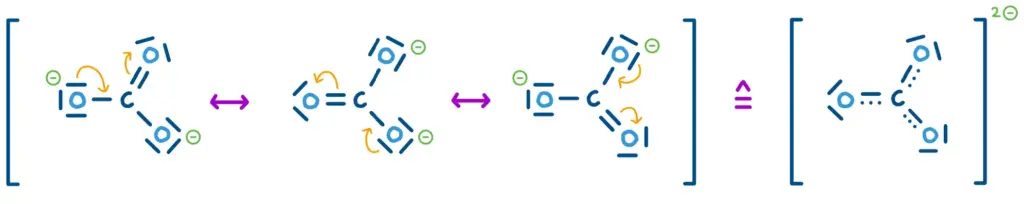
Mesomerie beschreibt ein chemisches Phänomen, bei dem einige Elektronen in einem Molekül delokalisiert sind. Die Elektronenverteilung des Moleküls kann dann nicht durch eine einzelne Strukturformel beschrieben werden, sondern nur durch eine Kombination mehrerer so genannter Grenzformeln. Die tatsächliche Elektronenverteilung liegt irgendwo zwischen diesen Grenzformeln. Dies führt zu einer erhöhten Stabilität des Moleküls. Ein Beispiel für ein mesomeriestabilisiertes Molekül ist das uns bekannte Carbonat-Ion CO32- in Abb. 6.
Übung
- Erklären Sie die unterschiedliche Säurestärke der in M3 angegebenen Stoffe im Vergleich zur Essigsäure.
Weitere Stoffe und ihre Säurestärke
Weiteres
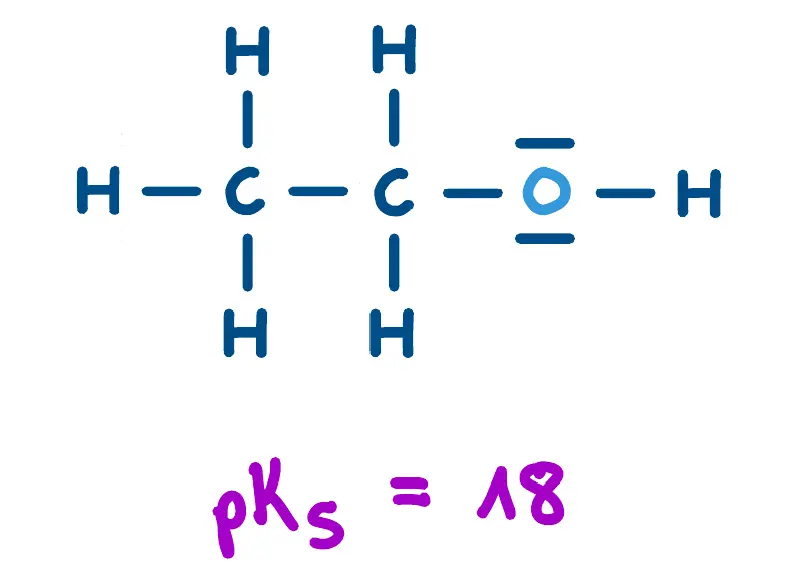
Ethanol.
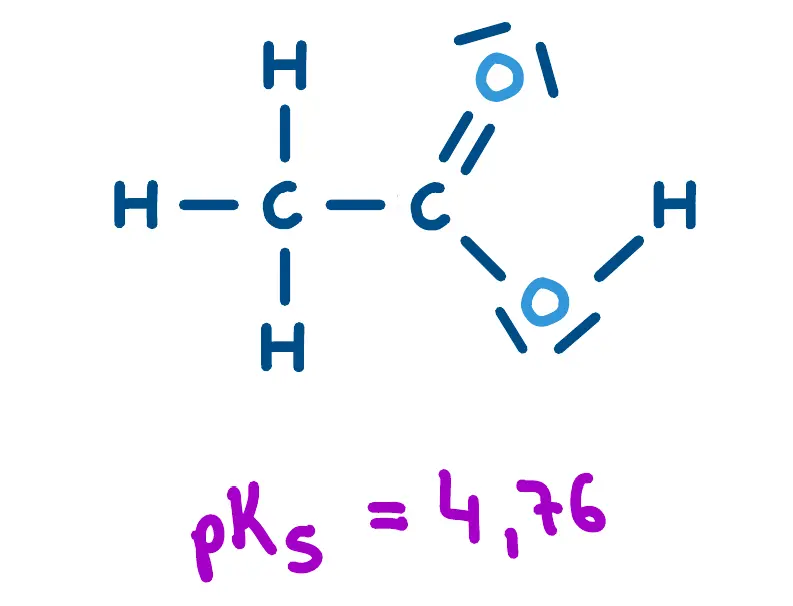
Essigsäure.
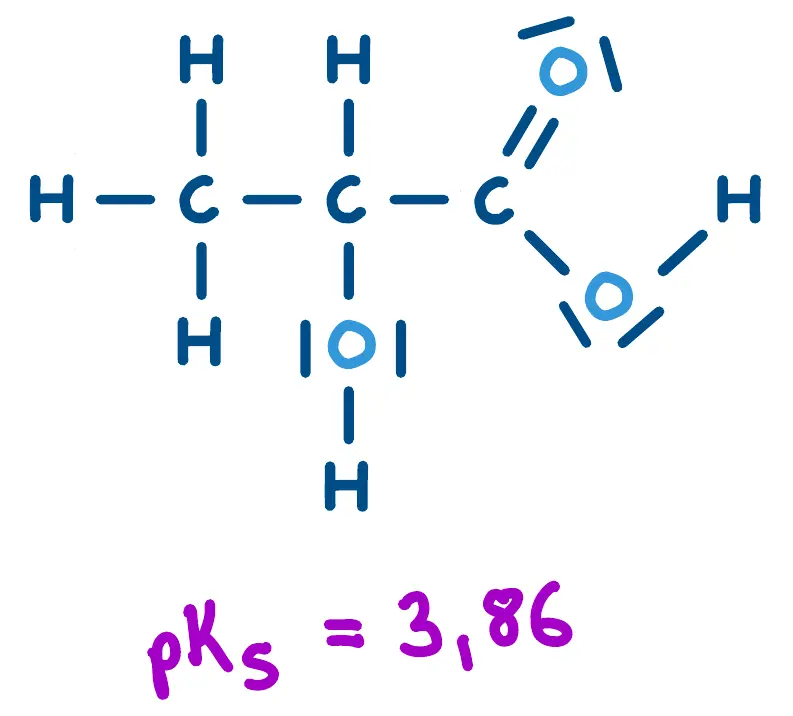
Milchsäure (2-Hydroxypropansäure)
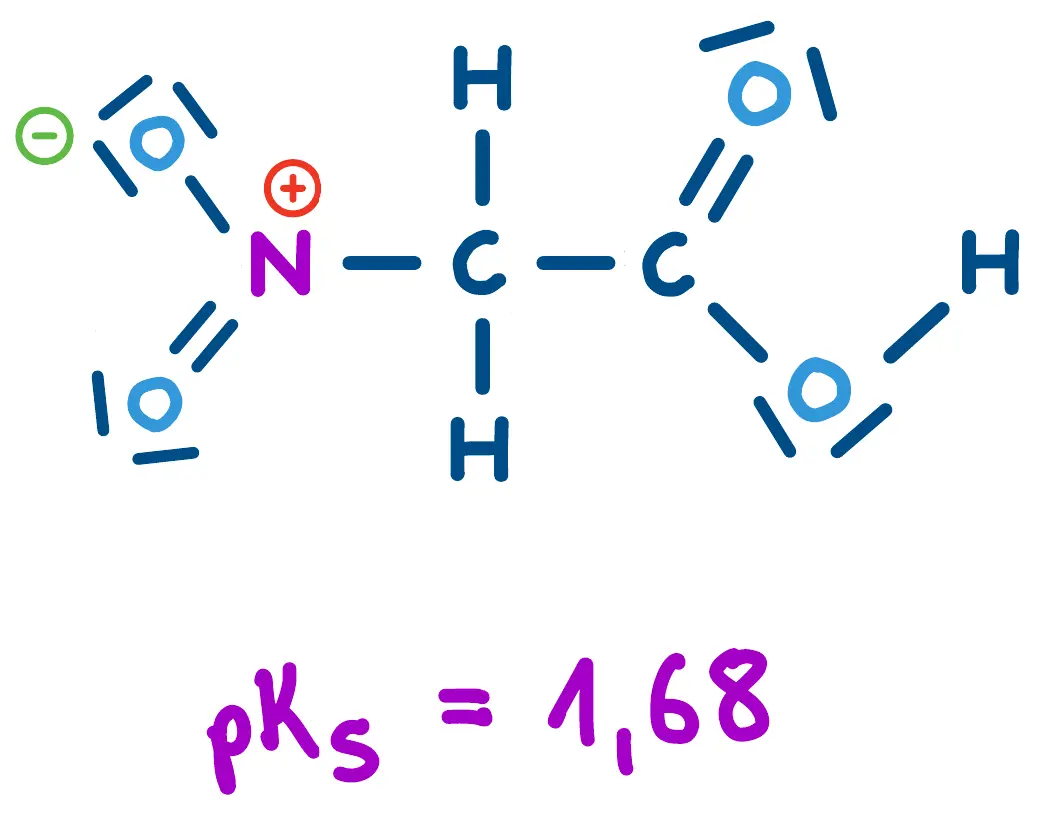
2-Nitroethansäure.