Aufgaben
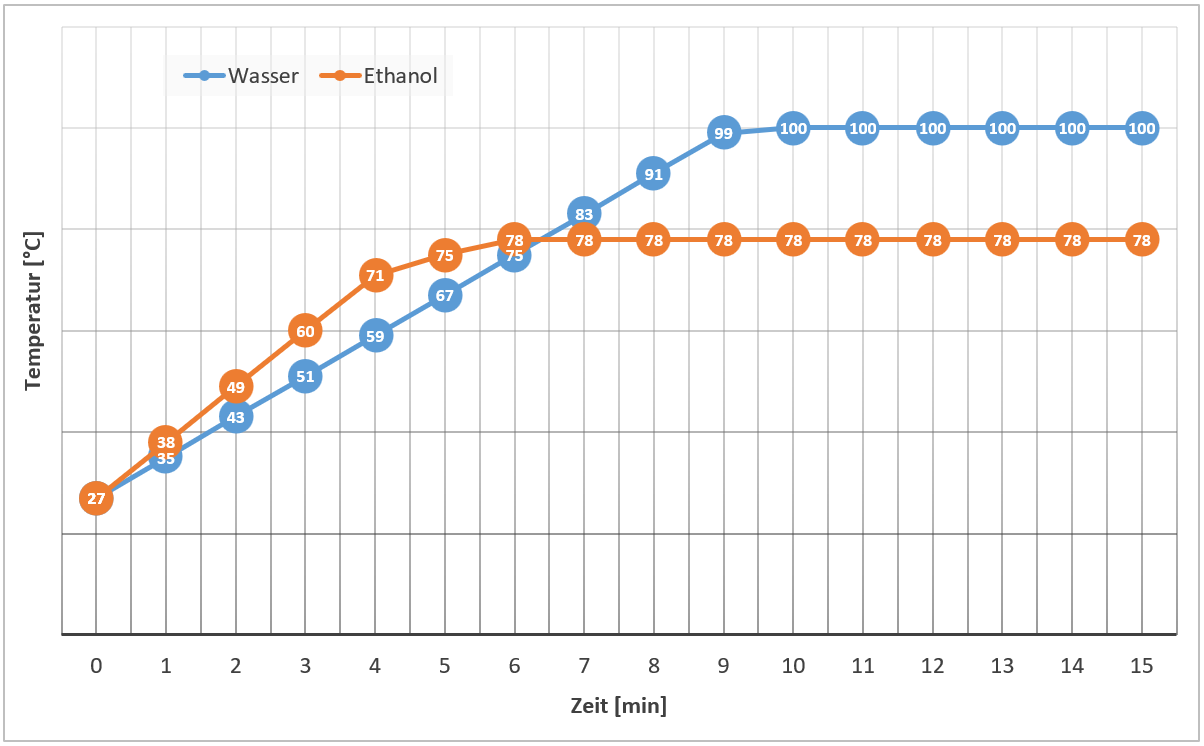
- Entnehmen Sie dem Diagramm in Abb. 1 die Siedetemperaturen von reinem Wasser und reinem Ethanol. Stellen Sie verbal einen Zusammenhang zwischen der Stoffeigenschaft („Siedetemperatur„) und der Teilchenebene („Wechselwirkungen, Zusammenhalt„) her, z. B. Die Siedetemperatur von … ist höher als …, weil die Wassermoleküle prinzipiell …
- Skizzieren Sie ein Teilchenmodell für flüssiges Wasser und daneben ein Teilchenmodell für flüssiges Ethanol jeweils als Ansammlung von mehreren Teilchen (z.B. jeweils 6 Teilchen). Skizzieren Sie in ihrer Darstellung der Flüssigkeit auch den Übergang von flüssig zu gasförmig durch Hinzufügen von weiteren Teilchen.
- Beschreiben Sie in einem kurzen Text daneben den Siedevorgang auf Teilchenebene mit Hilfe ihrer Skizze(n). Nutzen Sie dazu die Informationen aus M1, die den umgekehrten Vorgang darstellen.
- Erläutern Sie mit Hilfe von M1 die unterschiedlichen Siedetemperaturen der Reinstoffe Wasser und Ethanol basierend auf den zwischenmolekularen Kräften. Zeichnen Sie diese in ihre ursprüngliche Skizze ein.
Material
Siedediagramme von Reinstoffen
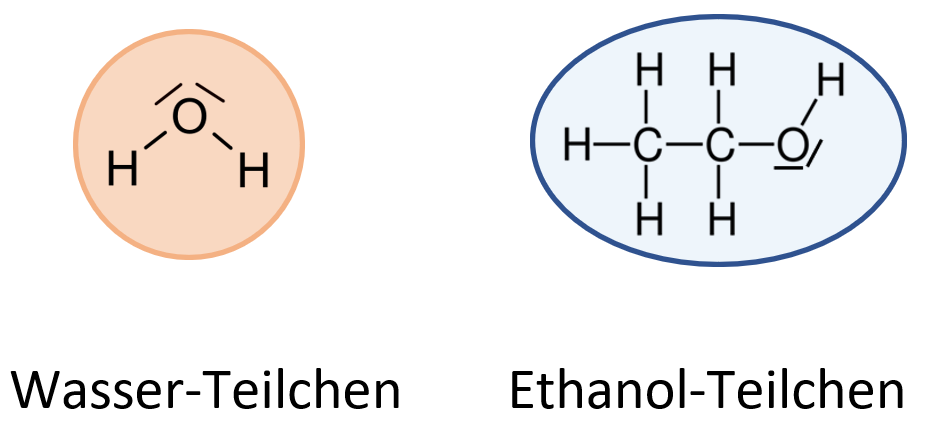
Molekülmodelle
Struktur - Eigenschafts - Beziehungen
Molekülstrukturen und Stoffeigenschaften hängen oftmals zusammen.
Ziehen sich beispielsweise Moleküle aufgrund ihres räumlichen Baus unterschiedlich stark an, führt dies auf der Stoffebene zu verschieden hohen Siedetemperaturen wie bei Wasser und Ethanol
Polare Bindungen und Anziehungskräfte
In einem Gas sind die Geschwindigkeiten von Molekülen und der Abstand zwischen ihnen in der Regel groß. Die Moleküle stoßen häufig zusammen, halten aber nicht aneinander fest.
Kühlt man ein Gas ab, werden die Moleküle langsamer und die verschiedenen Anziehungskräfte zwischen ihnen wirksamer bzw. stark genug, dass sie ab einem gewissen Punkt zusammenhalten können.
Will man umgekehrt die Moleküle einer Flüssigkeit voneinander trennen, muss man Energie hinzufügen, um diese Anziehungskräfte zu überwinden.
Die Anziehungskräfte zwischen Wassermolekülen basieren darauf, dass diese aufgrund von polaren Elektronenpaarbindungen in den Molekülen und ihrer Gestalt sogenannte permanente Dipole bilden.
Zur Erinnerung: Bei den polaren Bindungen werden die Bindungselektronen zu dem elektronegativeren Atom hin angezogen. Dadurch enthält das Molekül dauerhaft eine negative und eine positive Partialladung (Teilladung). Ein Dipol entsteht dann, wenn die negativen und positiven Partialladungen nicht gleichmäßig im Molekül verteilt sind und ihre Ladungsschwerpunkte nicht zusammenfallen. So ist das Wasser-Molekül ein Dipol, es hat einen ausgeprägten sogenannten Dipolmoment. Für das Kohlenstoffdioxid-Molekül gilt dies z. B. trotz der polaren Bindungen im Molekül nicht.
Moleküle mit ausgeprägten Dipolmomenten ziehen sich an, zwischen den Molekülen herrschen Dipol-Dipol-Kräfte.
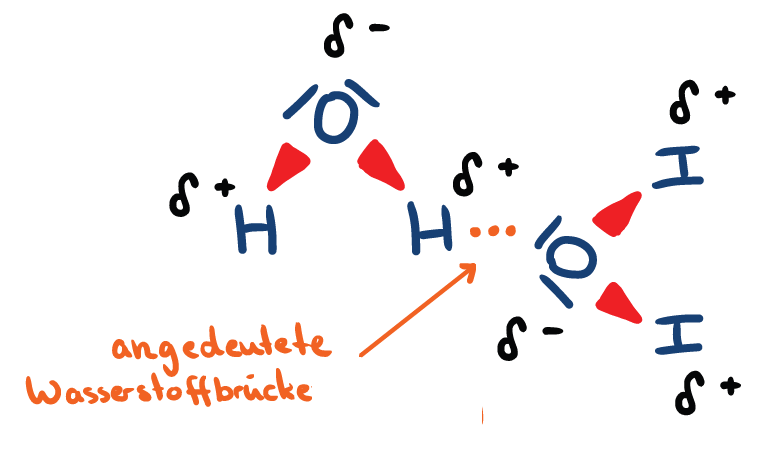
Zwei Wassermoleküle mit ihren polaren Bindungen (rot) und einer angedeuteten Wasserstoffbrücke (orange).
Noch eine Besonderheit: ist in den Molekülen ein Wasserstoffatom an ein besonders stark elektronegatives Atom gebunden, z. B. ein Sauerstoffatom (oder Stickstoffatom), kann es zwischen dem partiell positiv geladenen Wasserstoffatom des einen Moleküls und dem freien Elektronenpaar eines Sauerstoffatoms eines benachbarten Moleküls eine regelrechte „Brücke“ geben. Eine solche sogenannte Wasserstoffbrücke hat in etwa 1/10 der Stärke einer echten Elektronenpaarbindung und ist so gesehen eine besonders starke Art der Dipol-Dipol-Wechselwirkung.
Weitergedacht
- Erklären Sie, warum die Temperatur einer Flüssigkeit eines siedenden Reinstoffes trotz Energiezufuhr nicht weiter ansteigt.
- Erläutern Sie unter Verwendung der hier erlernten oder geübten Fachbegriffe, warum eine Trennung von Wasser und Ethanol durch Sieden nicht möglich ist.
Neben der Dipol-Dipol-Kraft und den Wasserstoffbrückenbindungen gibt es noch eine weitere Anziehungskraft zwischen Molekülen: Die Van-der-Waals-Kraft. Dieser Kraft widmen wir uns im nächsten Material.