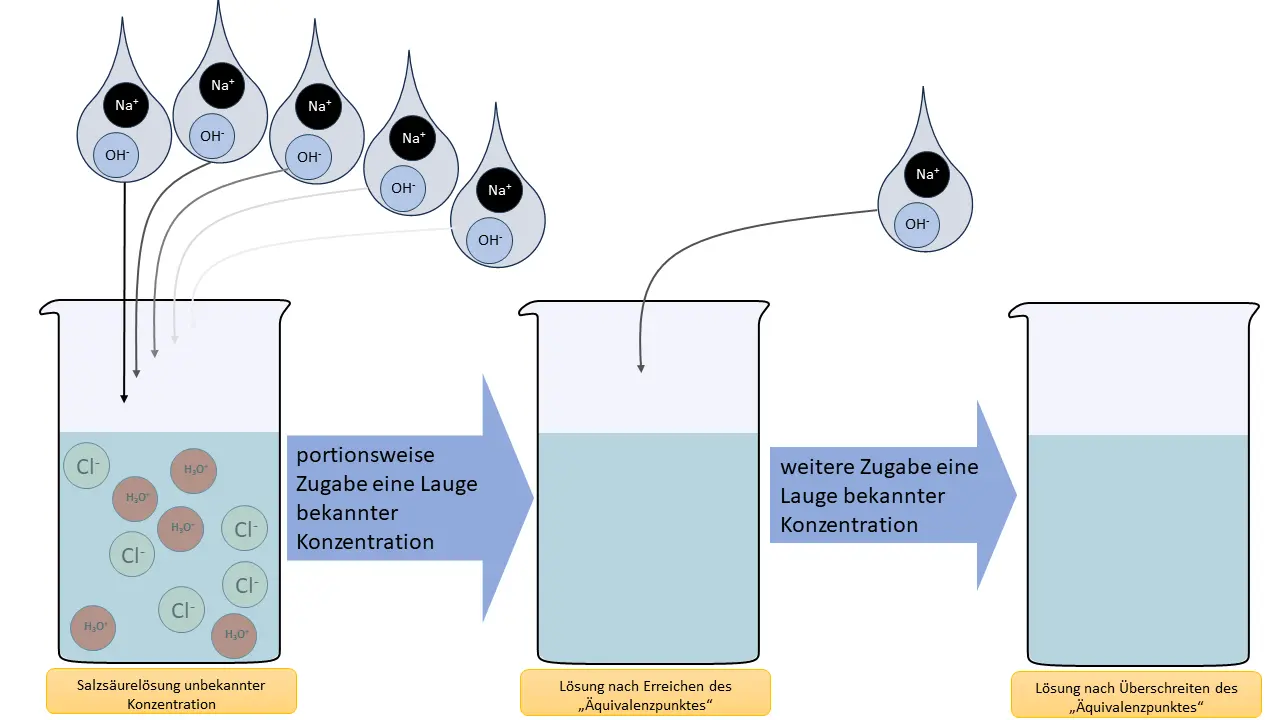
Wir haben eine Flasche Salzsäure mit fraglicher Konzentration. Wie können wir herausfinden, ob die auf dem Etikett angegebene Konzentration korrekt ist?
Wir könnten doch einfach den pH-Wert messen, oder?
Laut Buch wäre es genauer, Natronlauge bekannter Konzentration hinzuzugeben.
Logisch, bis die Lösung dann neutral ist. Dann wissen wir, wie viele Hydroxid-Ionen hinzugeben wurden und können daraus ableiten, wie viele Säuremoleküle vorhanden waren. Aber wie wollen wir das erkennen?
Aufgaben
- Führen Sie den Versuch V1 oder V2 durch.
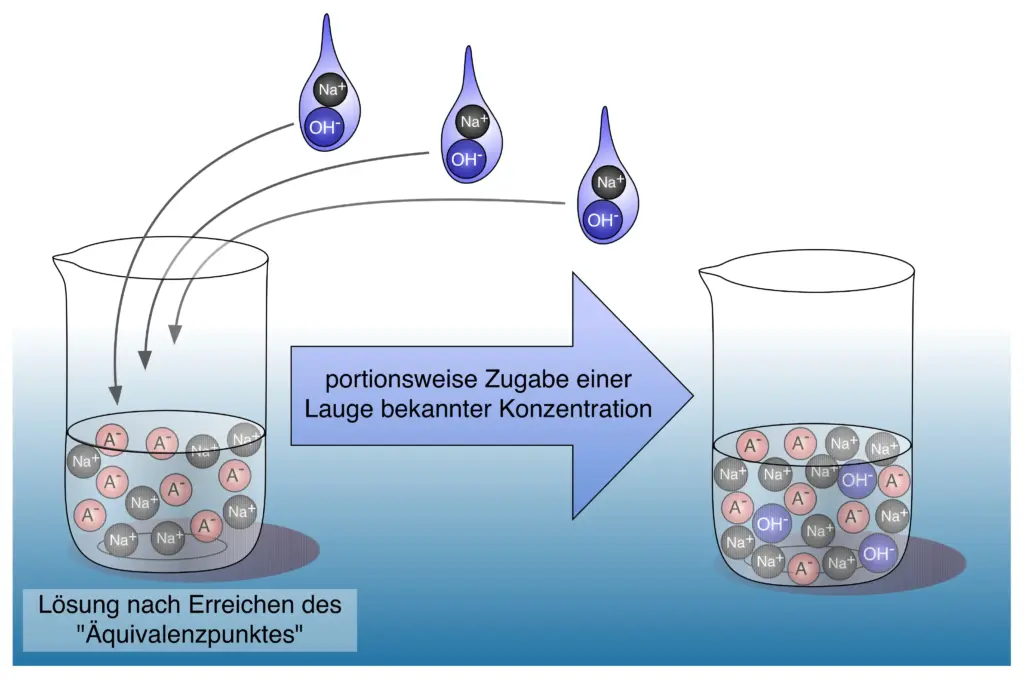
- Erläutern Sie unter Verwendung von M1 den Zustand der Lösung vor und bei Erreichen des Umschlagpunktes auf Teilchenebene. Stellen Sie zeichnerisch dar, was nach Erreichen des Umschlagpunktes bei Zugabe einer weiteren Portion Lauge passiert.
- Berechnen Sie mit Hilfe von M1 die Konzentration unserer Salzsäure.
Titration mit Bürette
Materialien
- Schutzbrille
- Bürette
-
Stativmaterial
- Stativ, Stativklemme, Stativmuffe
- Magnetrührer mit Rührfisch
- Messzylinder
- Erlenmeyerkolben oder Becherglas 250 mL
- Ggf. Trichter zum Befüllen der Bürette
Chemikalien
- Salzsäure mit fraglicher Konzentration
- Natronlauge 0,5 mol/L
- Destilliertes Wasser
- Bromthymolblau
- Phenolphthalein-Lösung < 1%
Durchführung
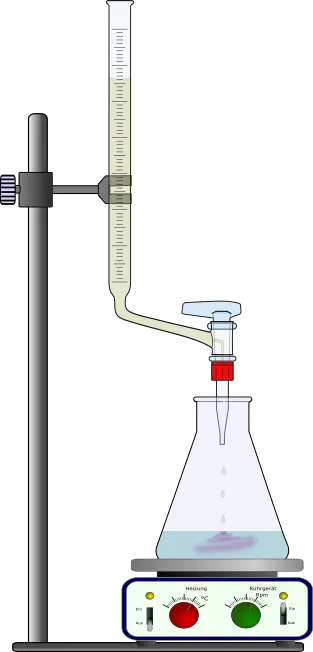
- Apparatur gemäß Abb. 1 aufbauen.
- Bürette ggf. mit Trichter oder einer Spritze von oben mit Natronlauge befüllen. Das Befüllen darf nie über Augenhöhe geschehen, da bei einem Unfall ernsthafte Augenschäden zu befürchten wären. Die Bürette wird zunächst absichtlich mit etwas mehr Natronlauge befüllt. Überschüssiges Volumen wird dann unten abgelassen.
- 20 mL Salzsäure in den Erlenmeyerkolben geben und auf 100 mL mit dest. Wasser auffüllen.
- Wenige Tropfen Indikator dazugeben und Magnetrührer einschalten.
- In 1 mL Schritten portionsweise Natronlauge zur Salzsäure titrieren bis zum dauerhaften Farbumschlag. Notieren Sie das benötigte Volumen an Natronlauge.
- Die gesamte Natronlauge ablassen. Die vereinigte Lösung über den Abguss entsorgen.
Aufbau
Aufbau mit Bürette. 1
Titration mit Spritzen
Materialien
- Schutzbrille
-
diverse Spritzen
- z.B. aus einem Spritzenkoffer
-
Stativmaterial
- Stativ, Stativklemme, Stativmuffe
- Magnetrührer mit Rührfisch
- Messzylinder
- Erlenmeyerkolben oder Becherglas 250 mL
- Ggf. Trichter zum Befüllen der Bürette
Chemikalien
- Salzsäure mit fraglicher Konzentration
- Natronlauge 0,5 mol/L
- Destilliertes Wasser
- Bromthymolblau
- Phenolphthalein-Lösung < 1%
Durchführung
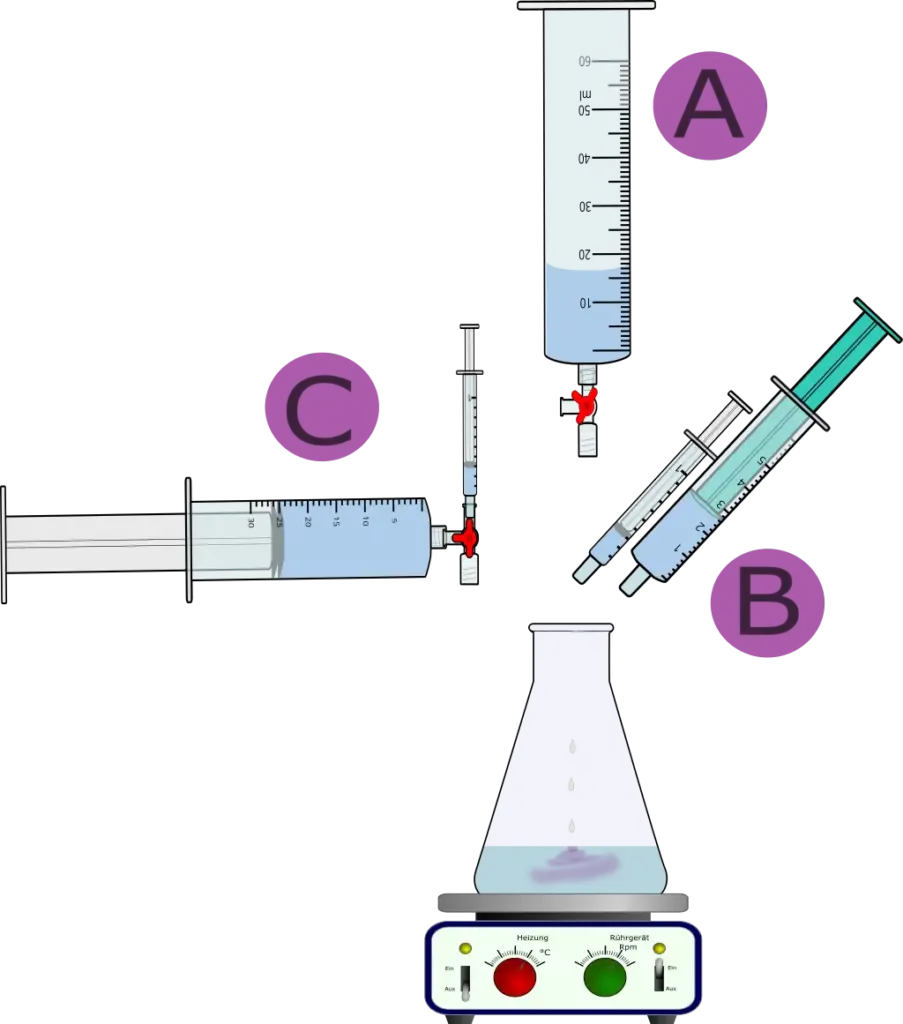
- Apparatur gemäß Galerie 1 Variante B aufbauen.
- Eine größere Spritze mit Natronlauge aufziehen.
- 20 mL Salzsäure in den Erlenmeyerkolben geben und auf 100 mL mit dest. Wasser auffüllen.
- Wenige Tropfen Indikator dazugeben und Magnetrührer einschalten.
- In 1 mL Schritten portionsweise Natronlauge zur Salzsäure titrieren bis zum dauerhaften Farbumschlag. Notieren Sie das benötigte Volumen an Natronlauge.
- Die gesamte Natronlauge ablassen. Die vereinigte Lösung über den Abguss entsorgen.
Aufbau
Aufbau mit Spritzen (ChemZ). Variante A: Spritze ohne Stempel als Kunststoffbürette verwenden. Variante B: Spritzen mit Natronlauge aufziehen. Variante C: Titration von Natronlauge aus kleiner Spritze in Salzsäure über einen Dreiwegehahn. 1
Teilchenmodell & Berechnung
Teilchenmodell
Becherglasmodell. 1
Neutralisationsgleichung
Berechnung
Grundlage für die Bestimmung einer unbekannten Stoffmengenkonzentration in mol pro Liter ist die Neutralisationsreaktion.
Weitergedacht
- Entscheiden Sie begründet, welche der vorgeschlagenen Neutralisationsgleichungen in M1 die Abläufe treffender darstellt.
- Stellen Sie eine Formel zur Berechnung der Konzentration einer zweiprotonigen Säure (zum Beispiel Kohlensäure H2CO3) basierend auf der Titration mit Natronlauge auf.
- Diskutieren Sie, ob eine Säure-Base-Titration mit Indikator auch mit einer schwachen und einer starken Base durchführbar wäre.
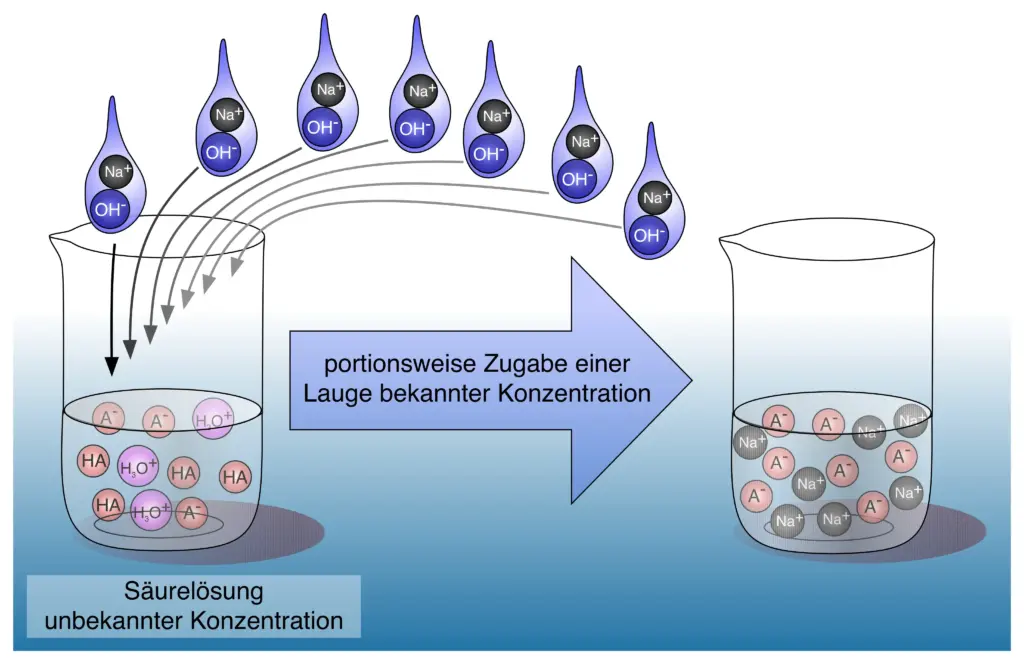
Erweitertes Teilchenmodell
Weiteres
Erweitertes Becherglasmodell zur Titration. 2
Zusammenfassung & Übung
Weiteres
Die Titration ist eines der wichtigsten Verfahren der quantitativen Analyse. Bei der einfachsten Variante misst man zunächst das Volumen der zu untersuchenden Lösung, versetzt sie mit einem Indikator und lässt eine Maßlösung mit bekannter Stoffmengenkonzentration portionsweise zufließen. Eine Farbänderung des Indikators zeigt das Ende der Titration an. Mit Hilfe des Volumens der zugeflossenen Maßlösung und mit Hilfe der Reaktionsgleichung kann die Stoffmengenkonzentration der zu untersuchenden Lösung berechnet werden. Die Reaktionsgleichung wird ohne Berücksichtigung der tatsächlich in der Lösung vorliegenden Teilchen notiert. Für die Neutralisation von beispielsweise Schwefelsäure mit Natronlauge als Maßlösung lautet sie:
Aus der Reaktionsgleichung kann entnommen werden, dass zur Neutralisation eines einzelnen Schwefelsäure-Teilchens zwei Natronlauge-Teilchen notwendig sind. In Bezug auf die Stoffmengen lässt sich somit ein Verhältnis aufstellen:
Mit n(Stoff) = c(Stoff) * V(Stoff) ergibt sich für die Konzentration der schwefelsauren Lösung:
Nun müssen nur noch die bekannten Werte in die Gleichung eingesetzt werden. Die Berechnung wird mit einem Antwortsatz abgeschlossen.
Übung
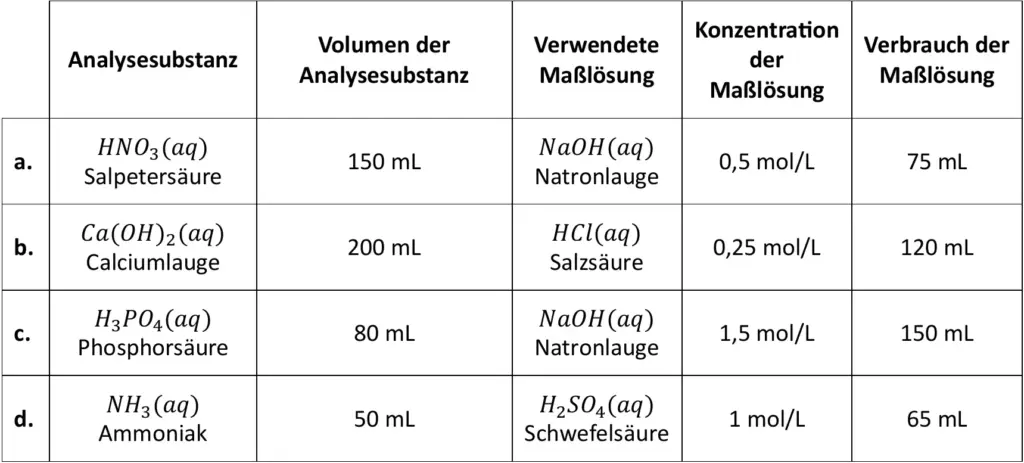
Geben Sie jeweils die Neutralisationsgleichung an, kennzeichnen Sie korrespondierende Säure-Base-Paare und berechnen Sie die Konzentration der Analysesubstanz. Notieren Sie immer den vollständigen Rechenweg mit Antwortsatz.