Was erwartet Dich?
Weiteres
Hast du schon einmal darüber nachgedacht, wie dein Körper an einer Stelle Sauerstoff aufnehmen und an anderer wieder freisetzen kann – und warum beides zuverlässig funktioniert? Viele Prozesse laufen nicht einfach vollständig ab, sondern stellen sich als Gleichgewichte zwischen Hin- und Rückreaktionen ein, die sich beeinflussen lassen.
Diese Idee begegnet dir nicht nur im Körper, sondern auch in natürlichen Stoffkreisläufen oder in technischen Anwendungen. Aktuelle Herausforderungen wie der Klimawandel hängen ebenso eng mit solchen Gleichgewichten zusammen.
Im Folgenden wirst du untersuchen, wie chemische Gleichgewichte funktionieren, wie man sie gezielt verändern kann und was dies alles direkt oder indirekt mit dir zu tun hat.
Weiteres
Können wir direkt mit den Kontexten anfangen? Die klingen interessant.
Das haben wir uns auch überlegt. Aber dann sind die Sachverhalte direkt auch sehr komplex. Daher schieben wir noch ein paar kurze „Theorieeinheiten“ davor. Keine Sorge – es lohnt sich!
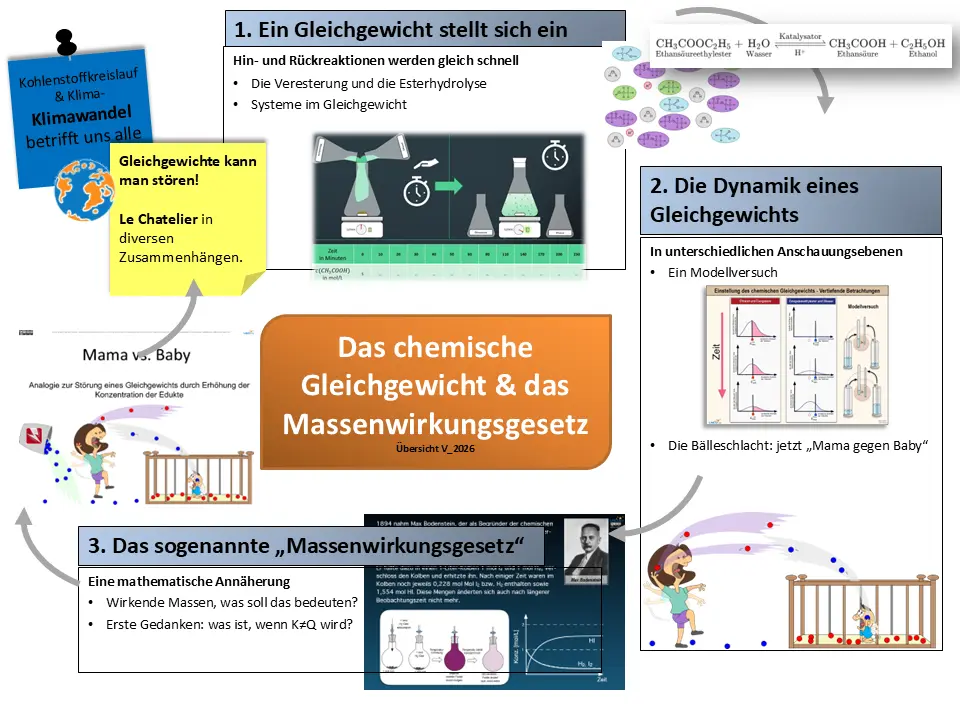
Übersicht über den kurzen Theorieblock
Advance Organizer4