Material
Warum Kinetik?
Die Legitimation der Themenfeldes rein über eine effektive Steuerung von Reaktionen mit Blick auf die „wirtschaftliche Herstellung unterschiedlicher Produkte wie Medikamente und
Aromastoffe“1 ist nach unserer Ansicht bei weitem nicht ausreichend.
Eine Notwendigkeit der Behandlung ergibt sich für uns eher aus der Tatsache, dass im schulischen Kontext chemische Gleichgewichte und deren Beeinflussung in der Regel nicht thermodynamisch hergeleitet werden, sondern durch die Betrachtung der der Reaktionsgeschwindigkeit.
Und erst „mit der Einbeziehung des chemischen Gleichgewichtes in die Betrachtung chemischer Reaktionen und der Möglichkeit seiner Beeinflussung können die Auswirkungen anthropogener Eingriffe in Kreisläufe der Natur beispielsweise hinsichtlich der für die kommenden Generationen wichtigen Fragen des Klimawandels eingeschätzt
und der ökologische und ökonomische Nutzen in technischen Verfahren beurteilt werden.“2.
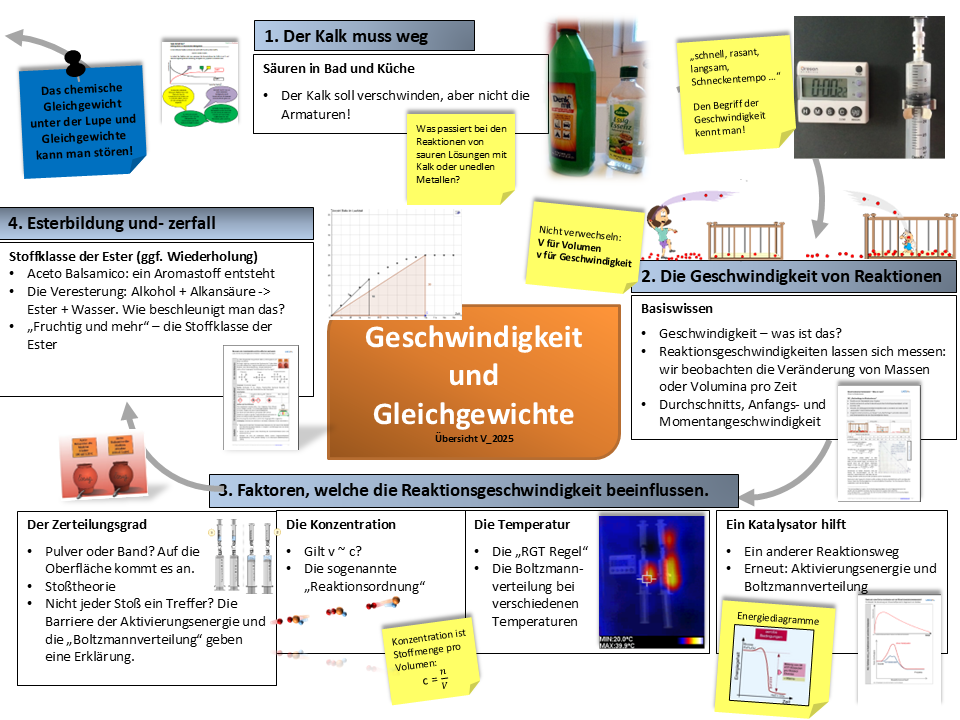
Ein möglicher Unterrichtsgang
Inhalte, konkretisierte Kompetenzerwartungen, Anmerkungen
Wie wirken Kalkentferner?
Was passiert, wenn man Kalk mit sauren Reinigern zusammenbringt? Welches Gas entsteht? Wie funktioniert es besonders gut und warum soll man vorsichtig beim Reinigen von Armaturen (aus unedlen Metallen) sein?
Die bereits aus dem Themenkomplex „Saure Lösungen“ (Sekundarstufe I) bekannte Reaktion einer sauren Lösung mit Kalk bzw. Magnesium wird exemplarisch genutzt, um den Begriff der Reaktionsgeschwindigkeit einzuführen.
Der Umgang mit der Spritzentechnik ChemZ (Auffangen eines Gases, Umfüllen) macht dies besonders einfach und eindrucksvoll möglich! Die Reaktion von Salzsäure mit Magnesium wird als „Leitexperiment“ genau in den Blick genommen (Versuch zum Auffangen des Gases, Bestimmung als Wasserstoff) und wenig später bei der Faktorenvarianz erneut genutzt.
Die Bälleschlacht im Kinderzimmer
Anhand einer Analogie erfolgt die Einführung von Anfangs-, Durchschnitts- und Momentangeschwindigkeit sowie der Betrachtung des Betrags.
Der Einfluss von c bzw. k wird angelegt.
Konkrete „Teilchen“ in Form von Bällen ermöglichen ein Zählen/Rechnen sowie die Verknüpfung von Wertetabellen und Grafen.
Bewusst wird das Aufräumen in der Analogie „nacheinander“ betrachtet. Erst später wird dann die „Gleichzeitigkeit der Abläufe“ das chemische Gleichgewicht als dynamisch erkennbar machen.
Vom Kinderzimmer ins Labor
Bei der Reaktionsgeschwindigkeit handelt es sich um eine Konzentrationsänderung pro Zeit. Gut beobachten kann man vor allem Massen- oder Volumenänderung beim Entstehen von Gasen!
Der Versuch mit Magnesium ist leichter zu deuten und wird daher verwendet.
In die Kurvenauswertung einfließen sollte die Bestimmung der Durchschnittsgeschwindigkeit und der Anfangsgeschwindigkeit.
.
Der Einfluss des Zerteilungsgrades
Der gleiche Versuch wird nun immer wieder mit Varianz eines Faktors erneut durchgeführt und ausgewertet.
Die Vergrößerung der Oberfläche hat für Lernende ersichtlich einen Einfluss und ist auch einfach zu erklären. Der Fokus liegt dabei auf der Teilchenebene (Einführung der Stoßtheorie). In Vorbereitung der RGT-Regel wird hier (für nur eine Temperatur) schon geklärt, dass nicht jeder Stoß zum Treffer führt, dass es einer Mindestenergie bedarf und dass nur wenige Teilchen in einer Stoffprobe über die Mindestenergie verfügen.
Konzentration und Stoßtheorie
Auch die Konzentration hat einen Einfluss! Dies erklärt zudem, warum die Geschwindigkeit im Laufe der Reaktion abnimmt.
Erfahrungsgemäß ist die Mathematisierung der Proportionalität wichtig. Der Proportionalitätsfaktor wird im Folgenden benötigt und die „Treffererfolgswahrscheinlichkeit“ und später „K“ als Gleichgewichtskonstante mathematisch abstrakt beschreiben zu können.
Basierend auf der Stoßtheorie würde man nicht erwarten, dass es nur empirisch zu ermittelnde Reaktionsordnungen gibt. Hier genügt zunächst eine kurze Betrachtung mit dem Hinweis, dass manche Reaktionen mehrschrittig ablaufen.
Die RGT Regel
Das Modell der Stoßtheorie liefert scheinbar einfache Erklärungen, da mit einer Temperaturerhöhung die Geschwindigkeit der Teilchen und damit die „Anzahl möglicher Stöße“ zunimmt.
Die alleinige Argumentation über die veränderte Anzahl von Stößen hält aber einer genaueren Betrachtung nicht Stand und muss erweitert werden. Wichtig ist die Anzahl der „molekularen Treffer“, die zu einer Reaktion führen.
Hierzu werden parallel erneut ein Enthalpie Diagramm, Aktivierungsenergie, Boltzmannverteilung und Mindestenergie bei verschiedenen Temperaturen betrachtet und die Beziehungen zueinander verdeutlicht. Interessant ist es, bei der Auswertung des Versuchs auch auf gegenläufige Wirkungen (exotherme Reaktion führt zur Erhöhung der Temperatur bei gleichzeitiger Abnahme der Konzentration der Lösung) einzugehen.
Die Rolle eines Katalysators
Die Katalyse im Anschluss an die RGT-Regel zu betrachten hat den Vorteil, dass alle für die Begründungszusammenhänge notwendigen Begriffe und Diagramme (u. a. Enthalpiediagramm, Boltzmannverteilung) bekannt sind.
Ein parallel durchgeführter (Demo-)Versuch mit Wasserstoffperoxid und Katalase (Trockenhefe) veranschaulicht dies nicht nur, sondern ermöglicht auch eine Verknüpfung mit den Inhalten des Biologieunterrichts (Enzymatik).
Eine Veresterungsreaktion erfolgt im Essig im Beisein von Restalkohol scheinbar automatisch.
Ihre exemplarische Betrachtung, ggf. weitere Syntheseversuche und die Beschreibung der Kondensationsreaktionen richten das Hauptaugenmerk noch einmal zusammenfassend auf die Geschwindigkeit von Reaktionen und deren Beeinflussung.
Nachfolgend lässt sich am Beispiel der Veresterung gut begreifbar machen, dass Reaktionen, die in einer Phase stattfinden, in der Regel nicht vollständig ablaufen, sondern Rückreaktionen dazu führen, dass sich ein chemisches Gleichgewicht einstellt.
Dessen Dynamik auf Teilchenebene, das Massenwirkungsgesetz und das Prinzip von Le Chatelier sind dann Inhalte der anschließenden Unterrichtsreihen.