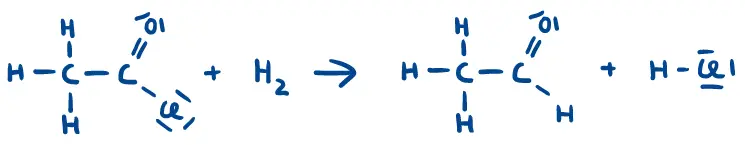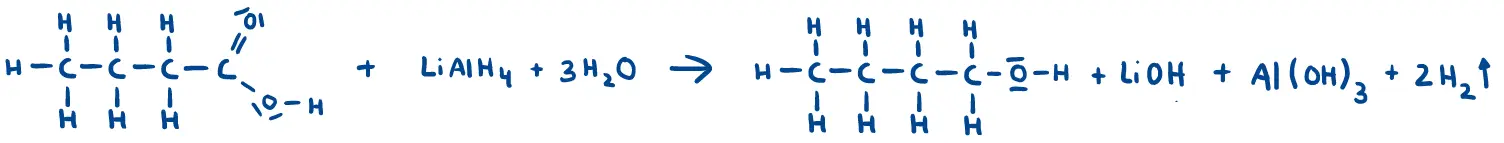Aufgaben
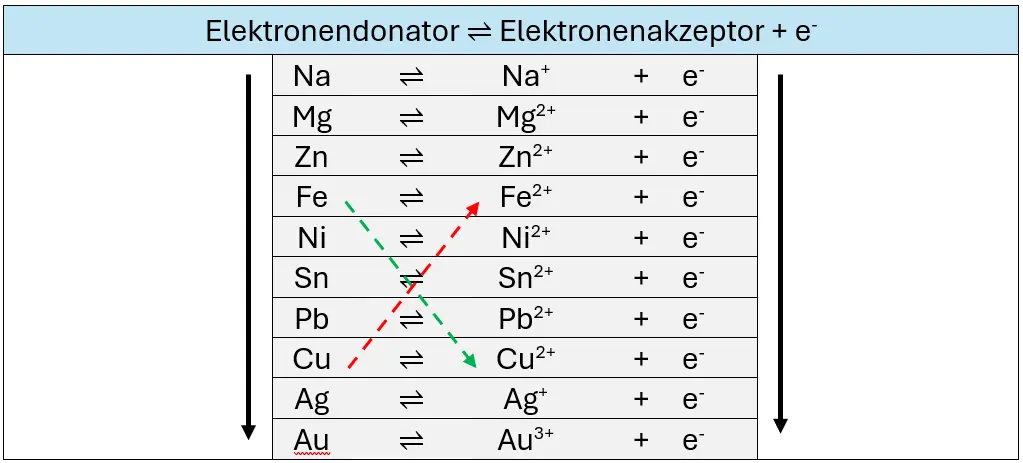
- Üblicherweise werden in der Redoxreihe die Redoxpaare unter Angabe der entsprechenden Anzahl der abgegebenen Elektronen angegeben. Tragen Sie für jedes Redoxpaar in der Tabelle 1 die zutreffende Elektronenzahl ein.
- Die Redoxreihe gibt verschiedene Tendenzen wieder (edler/unedler Charakter, Oxidations- bzw. Reduktionswirkung, Tendenz Elektronen abzugeben/aufzunehmen).
- Beschriften Sie die Pfeile links und rechts von Tabelle 1 entsprechend.
- Formulieren Sie einen Merksatz sowohl für die reduzierte als auch für die oxidierte Form (Elektronendonator, Elektronenakzeptor).
- Bei welchem der nachfolgenden Versuchsansätze erwarten Sie eine Redoxreaktion? Formulieren Sie für diese Fälle ein Redoxschema.
- Sn + NiSO4
- Ni + PbSO4
- NiSO4 + Pb
- AgNO3 + Cu
- Ag + Au(NO3)3
M1
Material
Weiteres
Ausschnitt aus der Redoxreihe der Metalle.1
Aufgaben
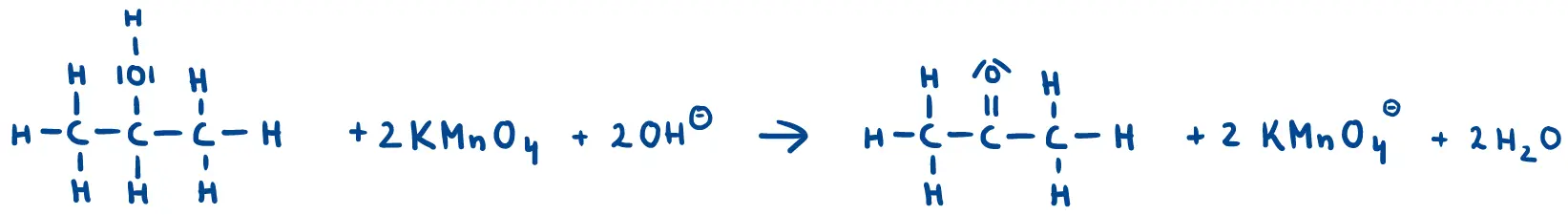
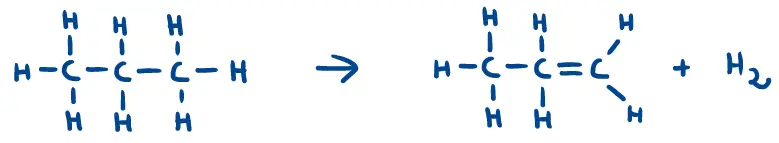
- Spätestens bei der Redoxtitration von Oxalsäure mit Kaliumpermanganat wissen wir, dass Redoxreaktionen kein alleiniges Phänomen zwischen Metallen und Metallsalzen sind. Auch organische Verbindungen können an Redoxreaktionen beteiligt sein. Zeigen Sie, dass es sich bei den Reaktionen in M2 um Redoxreaktionen handelt, indem Sie…
- die Oxidationszahlen zu allen Atomen angeben und die Atome kennzeichnen, die eine Änderung in ihrer Oxidationszahl erfahren haben,
- den Ort und den Prozess der Oxidation und Reduktion mit einem beschrifteten Pfeil kennzeichnen und die Anzahl der übertragenen Elektronen angeben.
- Wie fit sind Sie noch in der Benennung von Molekülen? Finden Sie es heraus, indem Sie alle organischen Moleküle in den Redoxreaktionen benennen.
Aufgaben
Die vorangegangene Redoxreaktion (2) in Abb. 2 soll die Grundlage einer Redoxtitration darstellen.
- Geben Sie das Stoffmengenverhältnis zwischen der organischen Verbindung (= Analysesubstanz) und Kaliumpermanganat (= Maßlösung) an.
- Berechnen Sie die Stoffmasse in Gramm der Analysesubstanz unter der Annahme, dass 25 mL einer 0,4 molaren Maßlösung bei der Redoxtitration verbraucht wurden.
M(Analysesubstanz) = 60,10 g/mol