Aufgaben
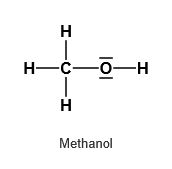
- Zeichnen Sie die Strukturformeln von Methanol, Propan-1-ol, Propan-2-ol und 2-Methylpropan-2-ol.
- Ordnen Sie den Alkoholen aus A1 jeweils den korrekten Alkoholtyp (primär, sekundär, tertiär) und das typische Oxidationsprodukt zu. Hinweise: Sie können die Vorlage nutzen.
- „Wenn ein sekundärer Alkohol zuerst zum Keton oxidiert wurde, kann er mit milden Mitteln nicht weiter oxidiert werden.“
Diskutieren Sie, ob der Citrat-Isomerisierungs-Schritt im Citratzyklus in Abb. 3 als „Umgehung“ eines ähnlichen Problems im Stoffwechsel verstanden werden kann.
Vorlage und Lösungshilfe zu A2

Methanol → primär → Aldehyd → ggf. Carbonsäure
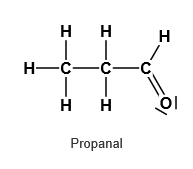
Propan-1-ol → primär → Propanal
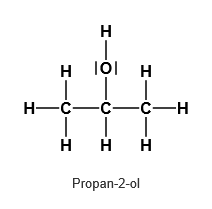
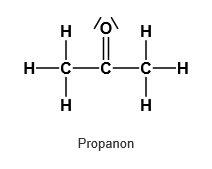
Propan-2-ol → sekundär → Propanon (Aceton)
2-Methylpropan-2-ol → tertiär → nicht oxidierbar unter milden Bedingungen
Aldehyde – reaktive Stoffe mit vielen Gesichtern
Aldehyde entstehen durch die Oxidation primärer Alkohole
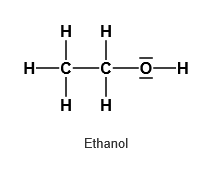
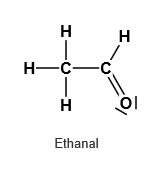
Aldehyde entstehen u. a. durch die Oxidation primärer Alkohole. Bei der Oxidation wird die Hydroxygruppe (–OH) in eine endständige Carbonylgruppe (–CHO) überführt. Ein bekanntes Beispiel ist die Oxidation von Ethanol zu Ethanal im Körper. Da bei der Reaktion vom Alkoholmolekül formal zwei Wasserstoffatome abgespalten werden, leitet sich das Wort Aldehyd von „Alkohol dehydriert“ (lat. alcoholus dehydrogenatus) ab.
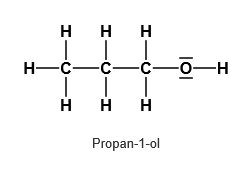
Beispiele für primäre Alkohole und für Aldehyde.1
Methanal und Ethanal als einfachste Vertreter der homologen Reihe der Alkanale sind bei Raumtemperatur flüchtige, stechend riechende Stoffe. Sie sind als krebserregend eingestuft und werden daher nicht in Schülerexperimenten eingesetzt.
Aus diesem Grund haben wir im Experiment lieber Propan-1-ol genutzt, da hieraus das weniger gefährliche Propanal entstanden ist.
Aldehyde lassen sich leicht weiteroxidieren
Bei der weiteren Oxidation von Aldehyden entstehen Carbonsäuren (Alkansäuren). Beispielsweise wird Ethanal weiter zu Ethansäure (Essigsäure) oxidiert, Propanal zu Propansäure usw. Diese Oxidation lässt sich für Nachweisreaktionen nutzen: Aldehyde wirken aufgrund ihrer leichten Oxidierbarkeit als Reduktionsmittel und können bestimmte Nachweisreagenzien reduzieren. Zwei klassische Aldehyd-Nachweise sind die Tollens-Probe (Silberspiegelprobe) und die Fehling-Probe.
Ein mögliches Ergebnis der Tollensprobe.2
Aldehyde im Stoffwechsel
Aldehyde spielen nicht nur bei Duftstoffen eine Rolle, sondern auch im Stoffwechsel. Es gibt Zucker, deren „offene“ Molekülform eine Aldehydgruppe besitzt. Ein Beispiel hierfür ist Glucose. Diese Aldehydgruppe erklärt, warum derartige Zucker als reduzierende Zucker wirken und sich mit Nachweisreaktionen wie der Fehling- oder Tollens-Probe erkennen lassen.
Warum sowohl kurzkettige Aldehyde als auch Zucker im Stoffwechsel nicht ungefährlich sind und mit welchen „Tricks“ der menschliche Körper letzterem begegnet, wird in zwei Materialen für den Leistungskurs einmal genauer unter die Lupe genommen.
Andere Beispiele für Verbindungen mit einer Carbonylgruppe
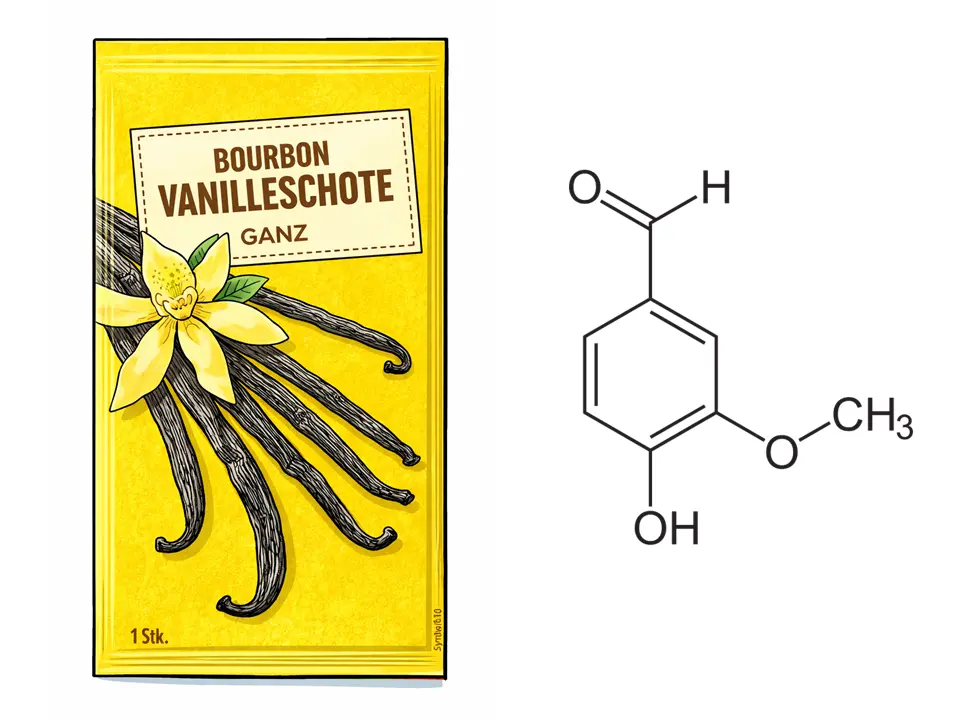
Größere Moleküle mit einer Carbonylgruppe sind meist weniger gefährlich. Vanillin ist z. B. Bestandteil der für viele Menschen angenehme riechenden Vanille. Vanille wird natürlich aus den Schoten bestimmter Orchideenarten gewonnen: Nach der Bestäubung wachsen grüne Vanilleschoten heran, die nach der Ernte durch ein aufwendiges Fermentations- und Trocknungsverfahren ihren typischen Geruch und Geschmack entwickeln basierend auf einer Vielzahl von Stoffen, u. a. Vanillin. Vanillin alleine kann man seit dem späten 19. Jahrhundert auch industriell produzieren.
Vanilleschoten enthalten Vanillin.3
Achte beim nächsten Einkauf einmal auf den feinen Unterschied: Vanillezucker enthält echte Vanille, zum Beispiel gemahlene Vanilleschoten. Vanillinzucker hingegen enthält meist nur Vanillin, den einzelnen Aromastoff, der nicht aus der ganzen Vanilleschote stammt.
Einfacher „Vanillinzucker“ darf deshalb keine Vanille-Abbildung tragen, denn diese ist Produkten mit echter Vanille vorbehalten.
Ketone entstehen aus sekundären Alkoholen
Weiteres
Ketone entstehen u. a. durch die Oxidation sekundärer Alkohole. Dabei wird die Hydroxygruppe (–OH) in eine nicht endständige Carbonylgruppe (>C=O) überführt. Ein bekanntes Beispiel ist die Oxidation von Propan-2-ol zu Propanon (Aceton).
Beispiele für einen sekundären Alkohol und ein Keton.1
Ketone lassen sich nicht einfach weiteroxidieren
Ketone lassen sich nicht einfach weiter oxidieren, da am Carbonylkohlenstoff kein Wasserstoffatom gebunden ist. Deshalb zeigen sie weder bei der Tollens-Probe noch bei der Fehling-Probe eine positive Reaktion.
Dies gilt unter milden, schulischen Bedingungen. Stärkere Oxidationsmittel würden die C–C-Bindungen brechen.
Primäre, sekundäre und tertiäre Alkohole im Stoffwechsel
Die Oxidierbarkeit eines Alkohols hängt entscheidend davon ab, ob am Kohlenstoffatom mit der Hydroxygruppe ein Wasserstoffatom gebunden ist. Primäre und sekundäre Alkohole besitzen ein solches Wasserstoffatom und können daher oxidiert werden. Tertiäre Alkohole hingegen sind unter milden Bedingungen nicht oxidierbar, da am OH-tragenden Kohlenstoffatom ausschließlich Kohlenstoffreste gebunden sind und kein Wasserstoff für die Bildung einer Carbonylgruppe zur Verfügung steht.
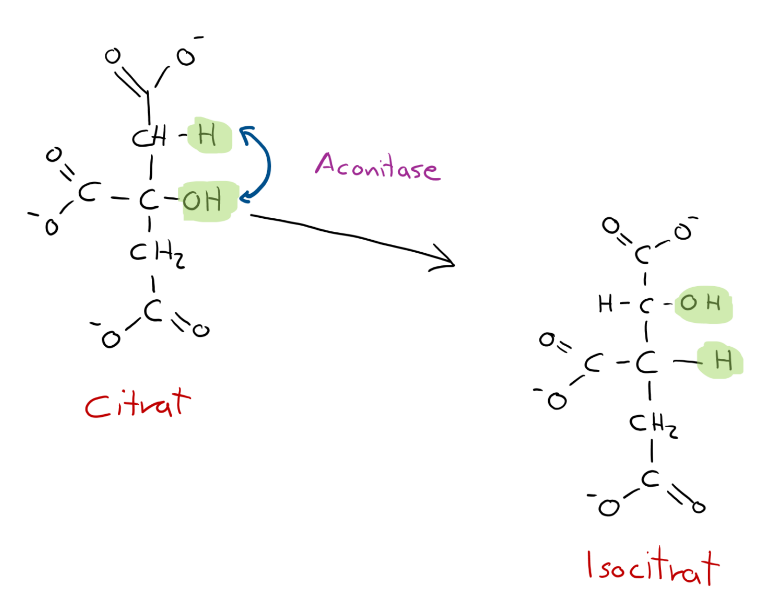
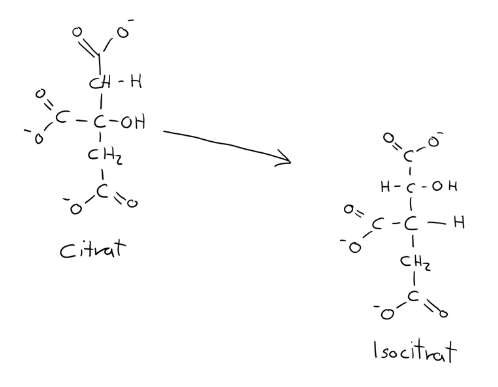
Isomerisierung im Schritt 2 des Citratcyclus.4
Dieses grundlegende Struktur-Reaktivitäts-Prinzip findet sich auch im Stoffwechsel wieder, zum Beispiel im Citratzyklus. Das Molekül Citrat besitzt eine Hydroxygruppe an einem Kohlenstoffatom, das mit drei weiteren Kohlenstoffatomen verbunden ist. Chemisch betrachtet handelt es sich dabei um einen tertiären Alkohol, der sich nicht direkt oxidieren lässt. Eine unmittelbare Oxidation im Citratzyklus wäre daher nicht möglich.
Um diese chemische Einschränkung zu überwinden, katalysiert das Enzym Aconitase eine Umlagerung von Citrat zu Isocitrat. Dabei wird die Hydroxygruppe auf ein benachbartes Kohlenstoffatom verschoben. Isocitrat enthält damit einen sekundären Alkohol, der nun oxidierbar ist.
Erst nach dieser Umlagerung kann die Hydroxygruppe im nächsten Schritt zu einer Ketogruppe (>C=O) oxidiert werden, was die anschließende oxidative Decarboxylierung im Citratzyklus ermöglicht.