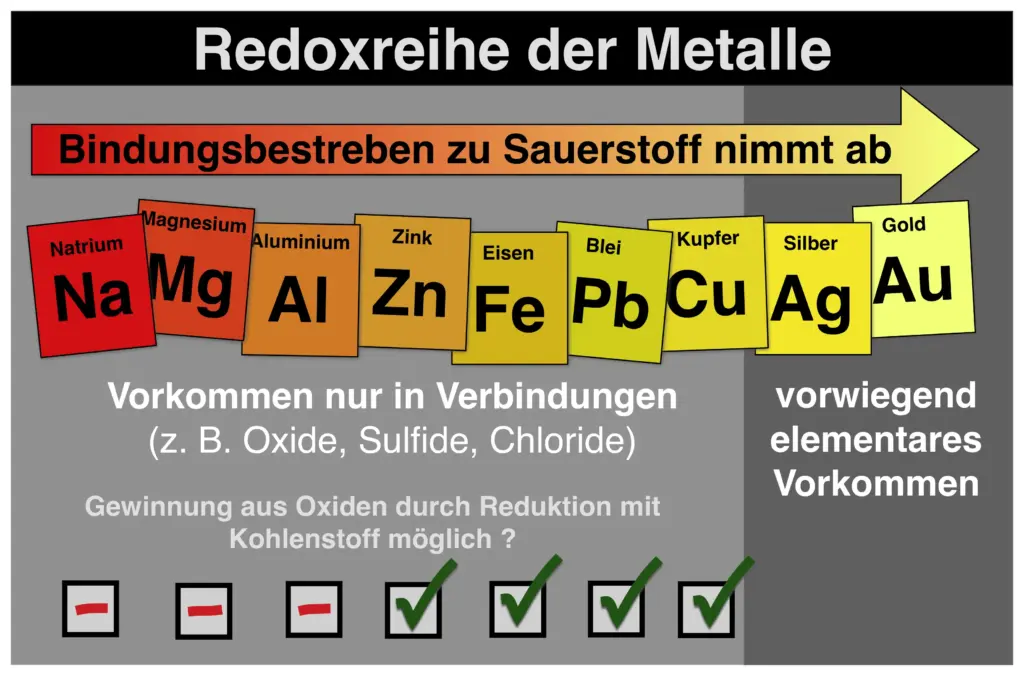
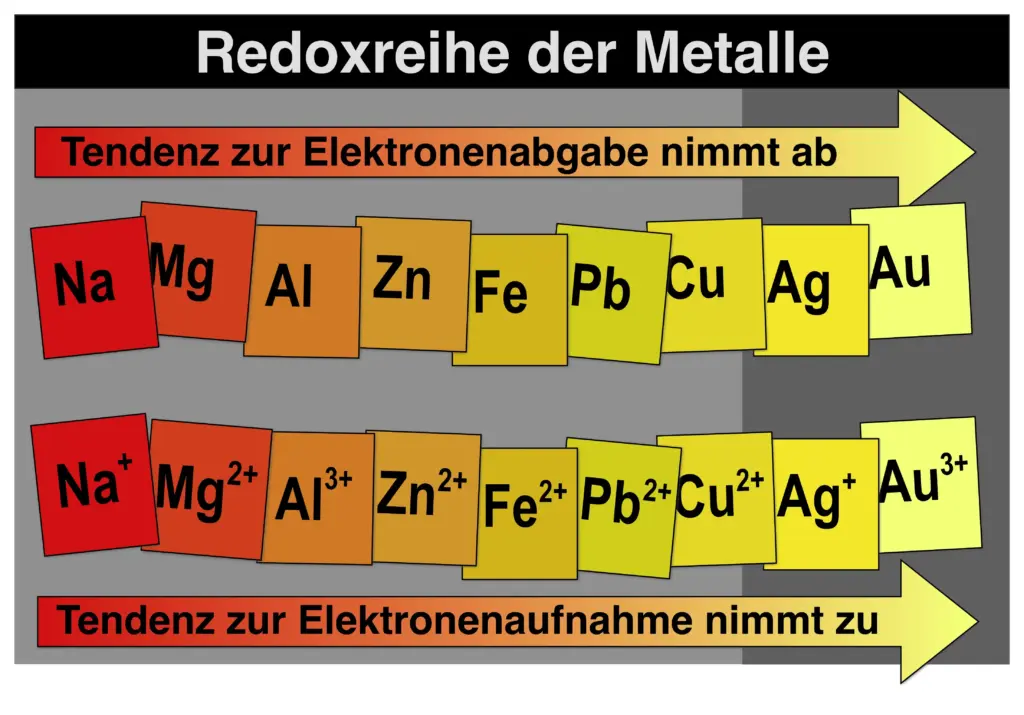
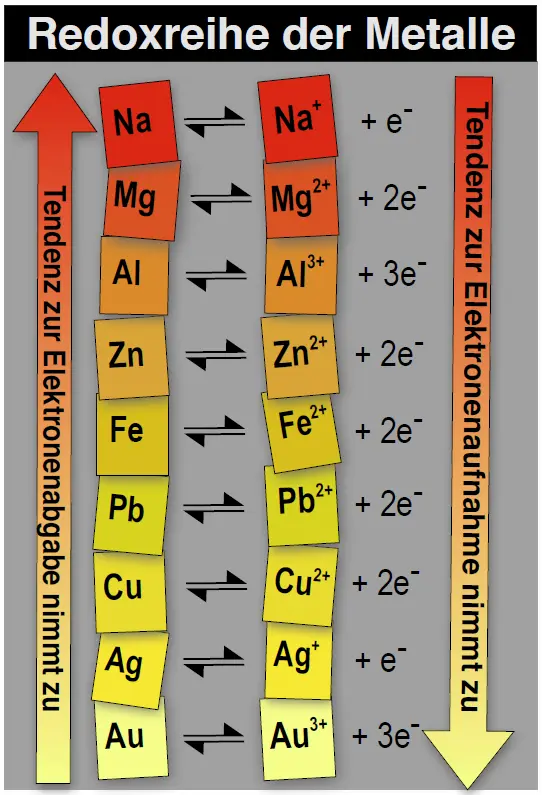
Was wäre wenn?
Zink oder Silber im selben Bergwerk
Stell dir vor, man hätte nicht nur die Eisen-Leiter sondern auch eine Gießkanne aus Zink oder Münzen und einen Ring aus Silber in der Kupfermine liegen gelassen.


Zinkgießkanne | Silbermünzen und -ring im Kupferbergwerk1
Was andere vermuten
Ich glaube, es wäre dasselbe passiert wie mit der Eisen-Leiter! Wahrscheinlich würde auf der Gießkanne und den Münzen später elementares Kupfer haften.
Wenn ich mir unsere „alte Redoxreihe der Metalle“ anschaue, denke ich etwas anderes.
Eine Redoxreihe der Metalle.2
Aufgaben
- Stelle mit Hilfe von Material 1 eine begründete Vermutung auf, was mit dem Zinkblech oder dem Silberring im Laufe der Zeit passiert wäre.
- Plane einen Versuch, mit dem man diese Vermutungen prüfen könnte.
- Führe V1 nach eine Besprechung durch. Notiere alle Beobachtungen und werte sie aus.
Hilfen zur Auswertung
Zink-, Silber- und Eisenblech in Kupfersulfatlösung3
Frage dich, ob beim Eintauchen des Silberblechs oder des Zinkblechs in die Lösung etwas passiert ist.
Falls nein:
Schreibe auf „keine Reaktion“
Falls ja:
- Notiere zunächst, welches Metall sich aus welchem Metall-Kation gebildet hat. Bist du unsicher, schaue noch mal beim Eisen nach – da war es genauso! Schreibe es direkt in einer Reaktionsgleichung.
- Notiere davor den Fachbegriff (Oxidation oder Reduktion). Schau ruhig noch mal beim Beispiel mit der Eisenleiter, was die Fachbegriffe ausdrücken.
- Überlege, woher die Elektronen stammen könnten und welche Ionen gleichzeitig entstanden sein müssen, auch wenn wir sie nicht sehen können.
- Notiere für diese zweite, gleichzeitig ablaufende Reaktion auch eine Reaktionsgleichung und schreibe den Fachbegriff davor
Vielleicht hilft es dir, die dir Teilchen erst noch einmal vorzustellen? Dann lade dir das Bild herunter und zeichne sie ein.
Eine Redoxreihe der Metalle.2
Überprüfung diverser Redoxreaktionen
Materialien
- Pipetten
- Schleifschwämme / Schmirgelpapier
- Papiertuch
Chemikalien
- Eisen-Blech
- Zink-Blech
- Silber-Blech
- Kupfer-Blech
- Kupfersulfat-Lösung 0,1 mol/L
- Zinksulfat-Lösung 0,1 mol/L
-
Eisen(II)sulfat-Lösung 0,1 mol/L
- Frisch ansetzen!
- Silbernitrat-Lösung 0,1 mol/L
Ausgangsvermutung
Atome unedler Metalle geben im Verhältnis einfacher ihre Elektronen ab als die edlerer. Umgekehrt müssten Ionen der edleren Metalle besser Elektronen aufnehmen als Ionen unedlerer Metalle.
Könnte es sein, das nur das Metallatom des unedleren Metalls seine Elektronen an das Ion des edleren Metalls abgibt. Aber nie umgekehrt?
Durchführung
- Alle Bleche abschmirgeln und so von Verunreinigungen befreien.
- Bleche auf einem Papiertuch legen und darauf einen Tropfen der verschiedenen Metallsalz-Lösungen tropfen.
- Die Beobachtungen tabellarisch festhalten (siehe unten).
Aufbau.4
Beobachtung
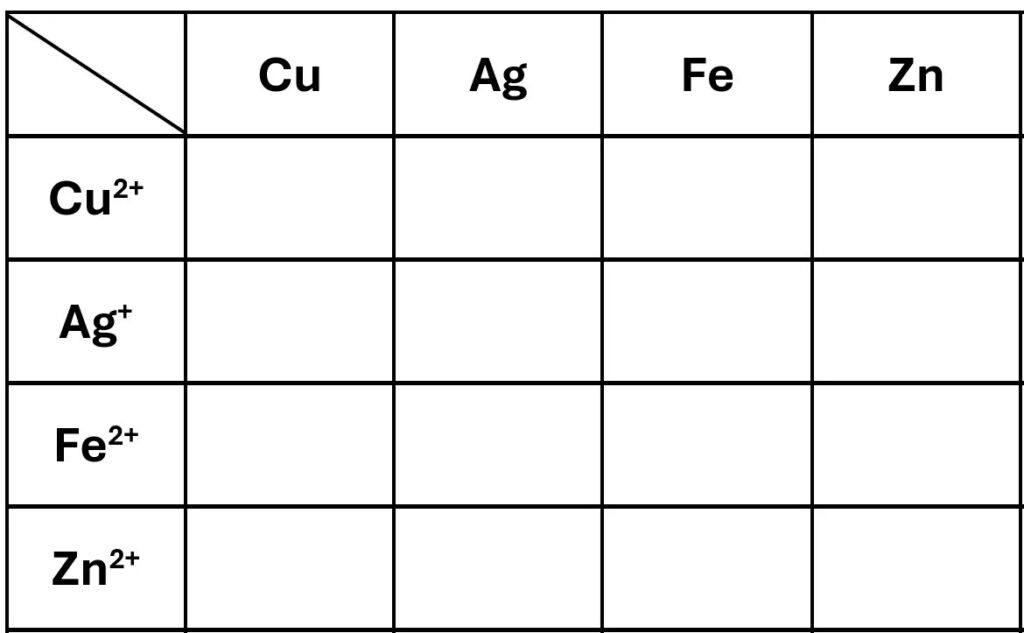

Oben Rechts: Zink, recht daneben: Eisen. Unten links: Kupfer, rechts daneben Silber.4
Entsorgen und Aufräumen
-
Reste der Metallsalzlösungen mit einer Pipette aufnehmen und im Sammelbehälter für Schwermetallsalze geben.
-
Alle verunreinigte Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
Weitergedacht
- Stelle heraus, was Material 2 zusätzlich zu unseren bisherigen zwei Versuchen verdeutlicht.
- Wähle ein beliebiges Metall und eine wässrige Lösung des Salzes eines anderen Metalls aus. Mache eine Vorhersage, ob beim Eintauchen des von dir gewählten Metalls in die Lösung des anderen Metallsalzes eine Reaktion stattfinden würde.