Spannung ist immer Potentialdifferenz
Weiteres
Man kann Spannungen immer nur als Gesamtunterschied der Potentiale zwischen zwei Halbzellen messen. Stellen wir uns vor, wir würden im Daniell-Element eine Halbzelle durch eine Halbzelle mit einem anderen Metall in seiner Metallsalz-Lösung austauschen.
Weiteres
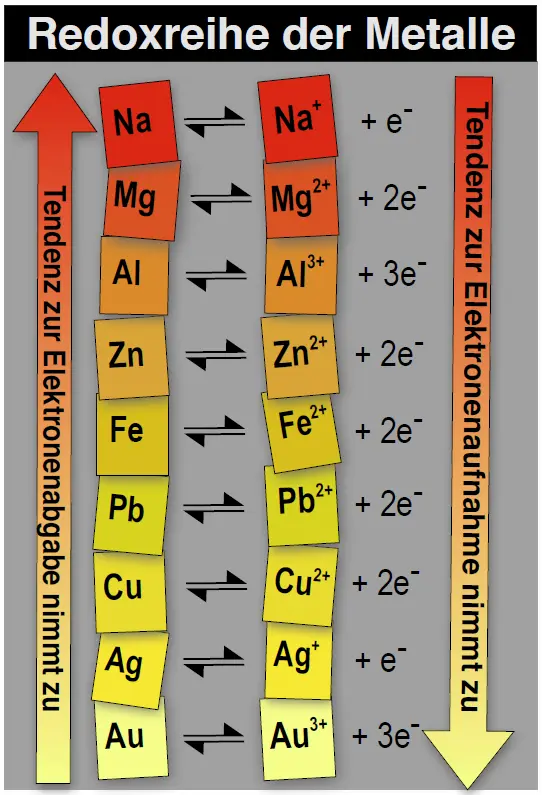
Die Redoxreihe der Metalle.1
Aufgaben
- Wählen Sie Redoxpaare aus der Redoxreihe der Metalle aus und legen Sie hypothetisch dar, welche Veränderungen der Spannung im Vergleich zum Daniell-Element (Zn/Zn2+ // Cu2+/Cu) Sie erwarten würden. Nutzen Sie in ihrer Argumentation auch Fachbegriffe: Potential, Lösungstension, elektrochemische Doppelschicht.
- Führen Sie Versuch V1 durch.
Zellkombinationen testen
Materialien
-
Filterpapier
- zugeschnitten & angefeuchtet
- Zellblock
- Spannungsmessgerät
- Multimeter
- Elektrischer Verbraucher
- z.B. Motor oder Lämpchen
Chemikalien
- Kupfer-Blech
- Zink-Blech
- Silber-Blech
- Kupfersulfat-Lösung 0,1 mol/L
- Zinksulfat-Lösung 0,1 mol/L
- Silbernitrat-Lösung 0,1 mol/L
Sicherheitshinweis
Silbernitrat hinterlässt braun/schwarze Flecken auf der Haut. Ihr Kontakt mit der Haut und den Augen ist daher strengstens zu vermeiden. Alle hier verwendeten Metallsalz-Lösungen sind umweltschädlich und gehören nicht in den Abguss! Entsorgungshinweise beachten!
Durchführung
- Oberflächenverunreinigungen auf den Metall-Blechen (Elektroden) abschmirgeln.
- Legen Sie zwischen den Zellblock-Hälften doppellagig angefeuchtetes Filterpapier (= Diaphragma).
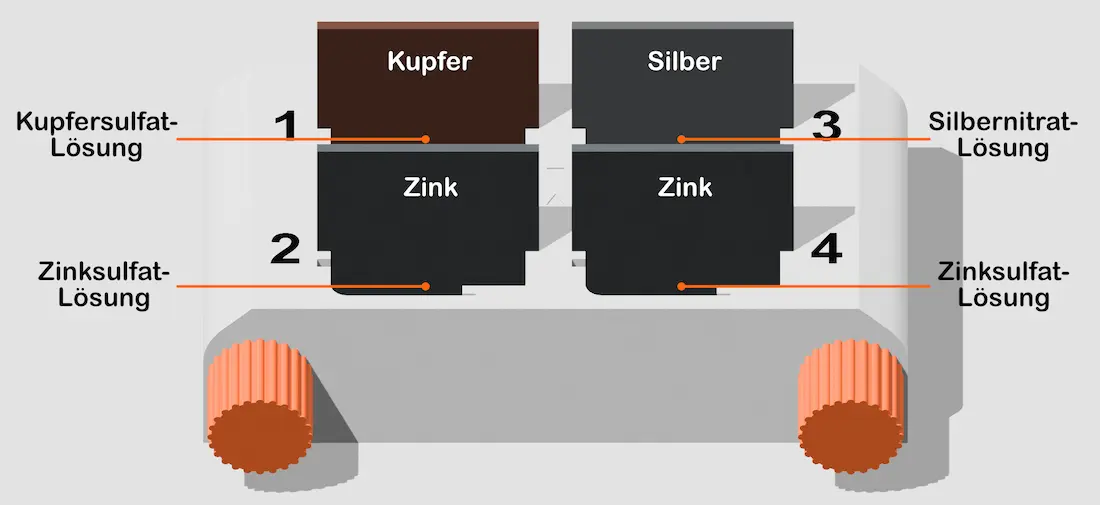
- Befüllen Sie 4 Halbzellen des Zellblocks bis zur inneren Markierung nach folgendem Schema:
Aufbau Zellblock.2
- Messen Sie die Zellspannung zwischen zwei Halbzellen, auch über Kreuz und notieren Sie ihre Messwerte tabellarisch gemäß der Vorlage unter Beobachtung.
- Übernehmen Sie die gemessenen Werte von zwei weiteren Gruppen und berechnen Sie den Mittelwert.
- Versuchen Sie den elektrischen Verbraucher mit der besten Zellkombination in Betrieb zu nehmen. Sollte dies nicht gelingen: Schließen Sie sich mit anderen Gruppen zusammen und überlegen Sie sich eine Strategie zur Inbetriebnahme des Verbrauchers ohne auf weitere Chemikalien zurückgreifen zu müssen.
Beobachtung
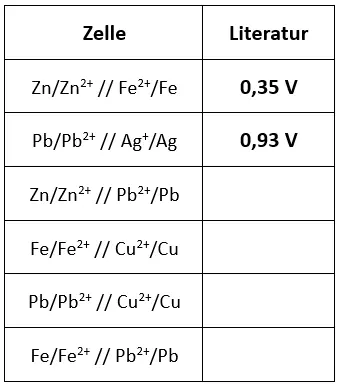
Vorlage.2
Entsorgen und Aufräumen
-
Die Flüssigkeiten mit Hilfe der Tropfflaschen aufsaugen. Überschüssige Lösungen in den Entsorgungsbehälter für Schwermetalle geben.
-
Alle verunreinigte Labormaterialien spülen und trocknen! Metall-Bleche blank schmirgeln.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
Aufgaben
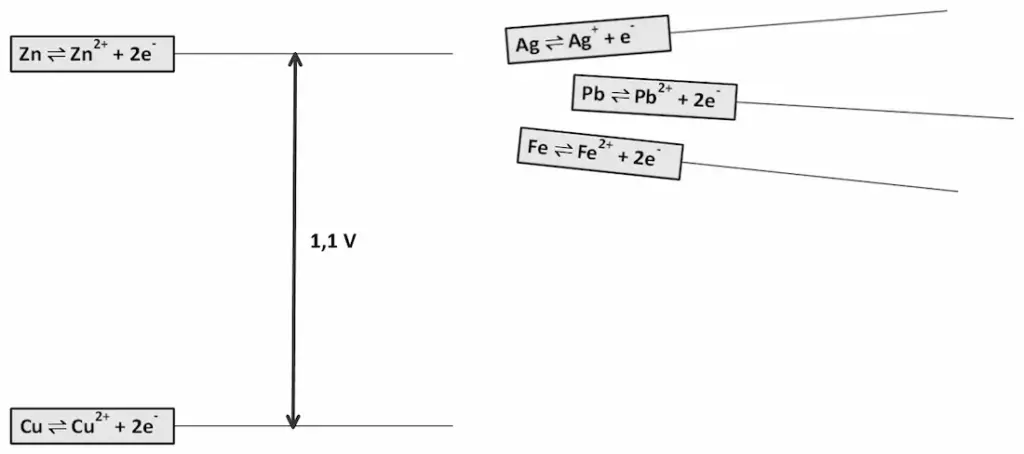
- In M2 finden Sie den Beginn der Erweiterung der Redoxreihe zu einer Spannungsreihe. Hierbei sind die Redoxpaare des Daniell-Elements im Abstand ihrer Potentialdifferenz eingetragen. Ergänzen Sie alle weiteren Redoxpaare derart, dass die Potentialdifferenzen veranschaulicht werden. Ordnen Sie hierzu die Redoxpaare der Halbzellen rechts sinnvoll übereinander an. Symbolisieren Sie die gemessene Spannung in Form entsprechend langer Pfeile.
Weitergedacht
- Suchen Sie nach Gesetzmäßigkeiten innerhalb ihrer gemessenen und vorgegebenen Messwerte. Bestimmen Sie mit Hilfe der gefundenen Gesetzmäßigkeiten die fehlenden Zellspannungen in Abb. 5.
- Muss man experimentell experimentell die Potentialdifferenzen aller erdenklicher Redoxpaare gegeneinander bestimmen, um zu einer vollständigen Spannungsreihe zu kommen?
- Recherchieren Sie, was man unter einer Parallelschaltung und einer Reihenschaltung versteht.