Der berühmte Streuversuch: Ausgangslage und Design
Zu Besuch bei einem berühmten Versuch
Ernest Rutherfords Labor zu Beginn des 20. Jahrhunderts.1
Im abgedunkelten Labor an der Universität Manchester um 1911 herrscht konzentrierte Ruhe. Ernest Rutherford lässt seine Mitarbeiter Hans Geiger und Ernest Marsden geduldig winzige Lichtblitze auf einem Leuchtschirm2 zählen.
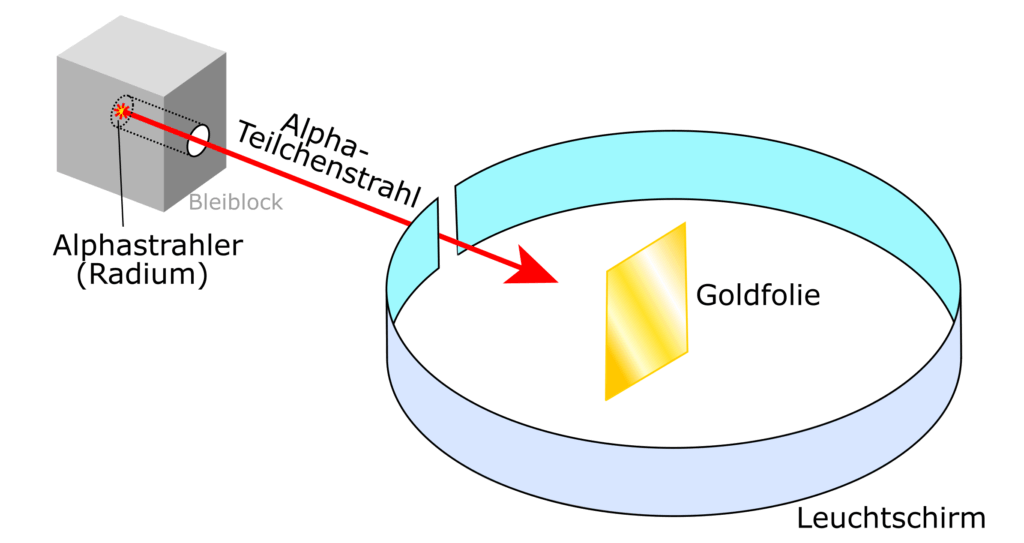
Sie hatten in dem Labor zuvor einen Versuch aufgebaut, bei dem aus einem Bleiblock mit einer winzigen Öffnung eine schwache Strahlung aus sogenannten Alpha-Teilchen auf eine hauchdünne Goldfolie treffen konnte. Die Goldfolie war so dünn, dass sie aus nur etwa tausend Atomschichten bestand.
Rund um die Folie hatten sie einen Leuchtschirm platziert. Bei jedem Treffer durch ein Alpha-Teilchen auf diesen Leuchtschirm blitzte der Schirm nun kurz auf. Beide notierten wahrscheinlich in einer Skizze auf einem Papier die Treffer.
mehr zu Alpha-Teilchen
Alpha-Strahlung besteht aus kleinen Alpha-Teilchen.
Rutherford kannte die Arbeiten zur Radioaktivität u. a. von Marie Curie und nutzte daher mit seinen Mitarbeitern sogenannte Alpha-Teilchen, um Atome „abzutasten“. Er und die anderen Forscherinnen und Forscher wussten nur, dass die Alpha-Teilchen positiv geladene Bruchstücke von „radioaktiven“ Atomen sind.
Wir wissen heute: Alpha-Teilchen bestehen genau aus 2 Protonen + 2 Neutronen.
Eine umfassende Würdigung von Marie Curie würde Bücher füllen. In Kürze soll hier hervorgehoben werden, wie ihre Forschung die Experimente von Ernest Rutherford zur Alpha‑Strahlung vorbereitete. Gemeinsam mit Pierre Curie erforschte sie Ende des 19. Jahrhunderts die von Henri Becquerel entdeckte Radioaktivität, prägte den Begriff „Radioaktivität“ und isolierte die neuen Elemente Polonium und Radium. Entscheidend: Sie zeigte, dass Radioaktivität eine Eigenschaft der Atome selbst ist – nicht eine Wirkung äußerer Einflüsse. Radium sendet besonders intensive Alpha‑Strahlung aus.
Curie entwickelte präzise Messverfahren und machte radiumhaltige Präparate verfügbar, die als starke, verlässliche Quellen für Alpha‑Teilchen dienten. Genau solche Quellen nutzten Rutherford und seine Mitarbeiter, um Atome zu „sondieren“.
Damit legten Curies Arbeiten zwei Grundlagen für Rutherfords Durchbruch: verlässliche Alpha‑Quellen und das Verständnis, dass Strahlung im Innersten der Atome entsteht.
Animation des Versuchs
Lass uns diesen berühmten Versuch heute einmal in einer Animation nachstellen. Machen wir uns zunächst gemeinsam mit dem Aufbau und der Animation vertraut.
Skizze des Versuchsaufbaus3
Hilfe bei Fachtexten
Du verstehst einen Fachtext nicht vollständig?
Aufgaben zur Beobachtung
- Mache dich gemeinsam mit allen im Plenum mit der Animation vertraut.
- Startet in eurer Gruppe die Animation und beobachtet den animierten Leuchtschirm für zwei Minuten. Nutzt gemeinsam euer Whiteboard so, als ob es ein Abbild des gebogenen Leuchtschirms wäre, und markiert jeden Lichtblitz als Treffer in Form eines Punkts.
- Beschreibe für dich das Trefferbild: Wo gibt es überall Punkte und wo häufen sich Punkte?
- Vergleiche im Plenum mit allen gemeinsam die beobachtete Verteilung der Lichtblitze.
Aufgaben zur Auswertung
- Lade dir die Skizze des Versuchsaufbaus aus M1 herunter und zeichne in die Versuchsskizze einige typische Flugbahnen der Alpha-Teilchen, die sich aus dem Trefferbild ableiten lassen.
- Beschreibe, wohin die meisten Alpha‑Teilchen flogen, und leite daraus eine erste Aussage über den „Innenraum“ eines Goldatoms ab.
- Nimm Stellung dazu, warum der Versuch „Streuversuch“ genannt wird.
Aufgaben zur Modellierung
- Erkläre die Erwartungen an den Versuch, die sich aus Annahmen vorheriger Atommodellen wie in M2 Abb. 3 ergeben hätten. Was müsste jeweils mit den Alpha‑Teilchen passieren?
- Vergleiche nun diese Erwartungen mit den Beobachtungen und begründe, was nach diesem Versuch jeweils gegen die Tragfähigkeit der „vorherigen“ Modelle spricht.
- Benenne ein oder mehrere Kriterien, die ein verändertes Atommodell erfüllen muss, um die Beobachtungen des Streuversuchs zu erklären.
- Lies M2 zu Ende und ergänze deine Gedanken.
Auswertung und ein neues Modell
Kurzer Gedanke vorab
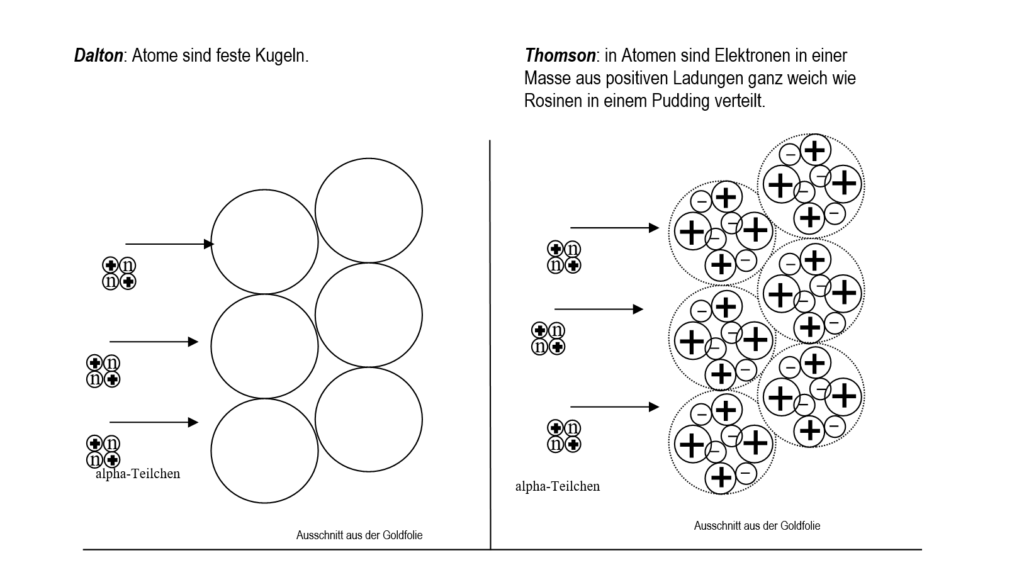
Für die Auswertung wird es hilfreich sein, wenn wir uns im Atommodell nach Dalton und dem Rosinenkuchen-Atommodell nach Thomson einmal vorstellen, wie es modellhaft aussähe, wenn Alpha-Teilchen auf die Atome der Goldfolie prallen.
Wie sähe ein Aufprall von Alpha-Teilchen in unseren bisherigen Modellen aus?5
Was war für Rutherford das Besondere?
Rutherford ließ Marsden und Geiger auch am Rand des Leuchtschirms nach Leuchtblitzen Ausschau halten. Wahrscheinlich hat er etwas geahnt.
Wohl zur Überraschung seiner Mitarbeiter erschienen auf dem Leuchtschirm auch hier Blitze. Es gab also Treffer, die zeigten, dass wenige Alpha-Teilchen stark abgelenkt werden und manche sogar zurückprallten. Diese Beobachtung war für sich genommen sensationell.
Rutherford sagte dazu Folgendes:
„It was almost as incredible as if you had fired a 15-inch shell at a piece of tissue paper and it came back and hit you.“6
Rutherfords Schlussfolgerungen
Vergegenwärtige dir noch einmal die Ladung des Alpha-Teilchens.
Aus den Beobachtungen, dass viele Alpha-Teilchen die Goldatome einfach passierten, einige wenige abgelenkt wurden und zudem etwa jedes 100.000 Alpha-Teilchen reflektiert wurde, zog Rutherford seine entscheidende Schlussfolgerung:
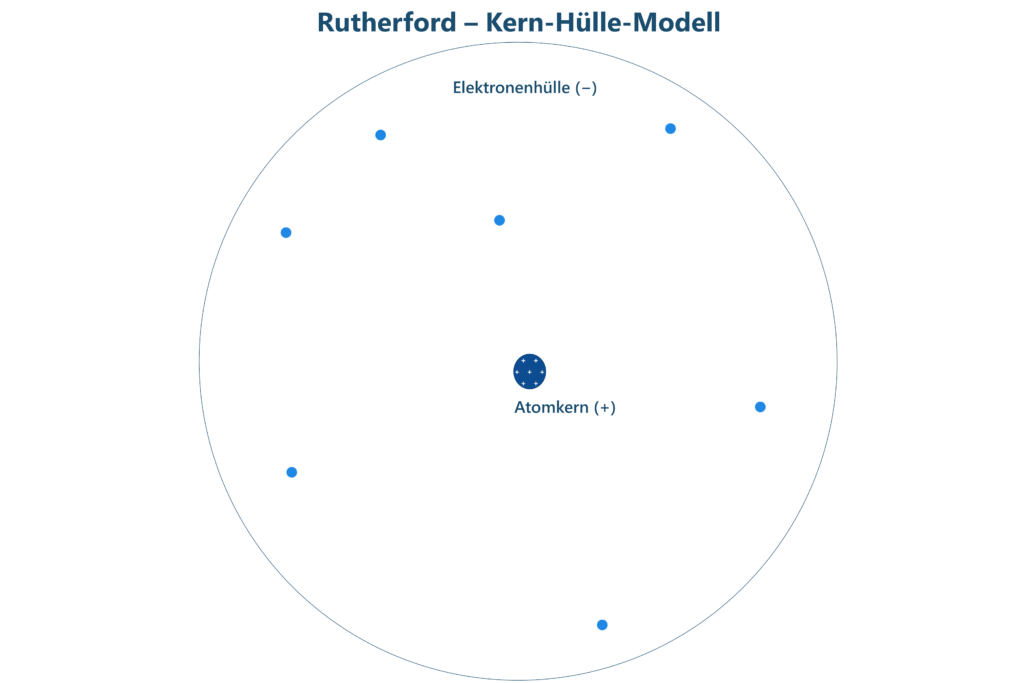
Die positive Ladung und fast die gesamte Masse eines Atoms ist in einem winzigen Kern konzentriert. Um den Kern herum befindet sich eine vergleichsweise „leere“ Hülle aus Elektronen. Diese wiederum haben eine viel geringere Masse als die Protonen.
So entstand das berühmte Kern‑Hülle‑Modell, das unser Verständnis vom Atombau grundlegend veränderte.
Das Kern-Hülle-Modell des Atoms
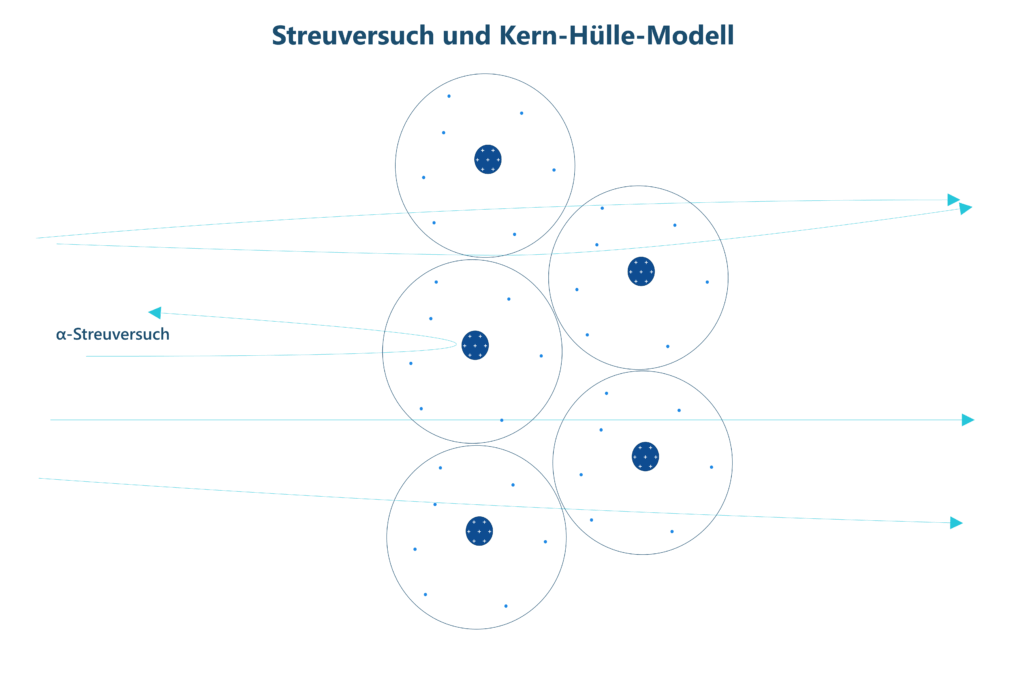
Streuversuch und Kern-Hülle-Modell7
Wichtigste Aussagen des Kern-Hülle-Modells
- Jedes Atom besteht aus einem sehr kleinen, positiv geladenen Atomkern und einer negativ geladenen Elektronenhülle.
- Fast die gesamte Masse steckt im Kern; die Hülle ist größtenteils leerer Raum.
- Größenverhältnis: Der Atomdurchmesser ist je nach Element etwa 10.000 bis 100.000‑mal größer als der Kerndurchmesser. Vergleich: Wäre das Atom so groß wie ein Fußballstadion, wäre der Kern maximal etwa erbsengroß in der Mitte.
- In der Hülle befinden sich Elektronen (−) mit sehr kleiner Masse.
- Die positiven Ladungsträger im Kern heißen Protonen (+); insgesamt ist das Atom elektrisch neutral. Also ist die Anzahl der Elektronen = Anzahl der Protonen.
- Die Neutronen (neutral) im Kern wurden erst später entdeckt; im einfachen Rutherford‑Modell werden sie daher oft weggelassen.