Metalle - typische Eigenschaften - gleiche Bindungsart
Alle Metalle haben ähnliche Eigenschaften. Hier lernst du, was dies mit der Bindung zwischen den Metallatomen zu tun hat!
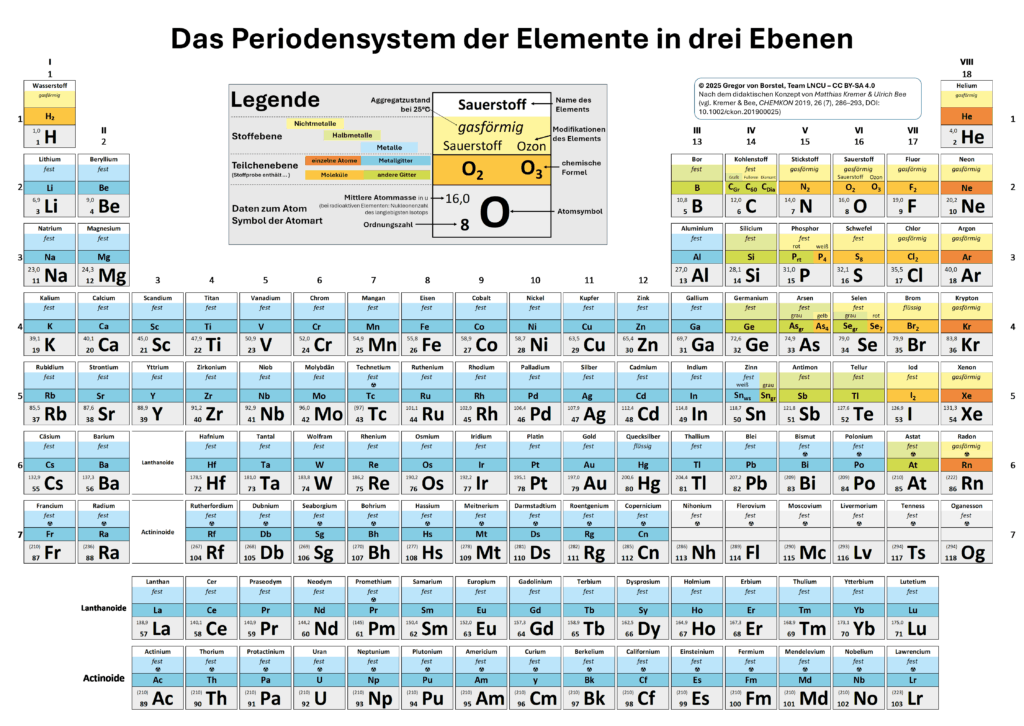
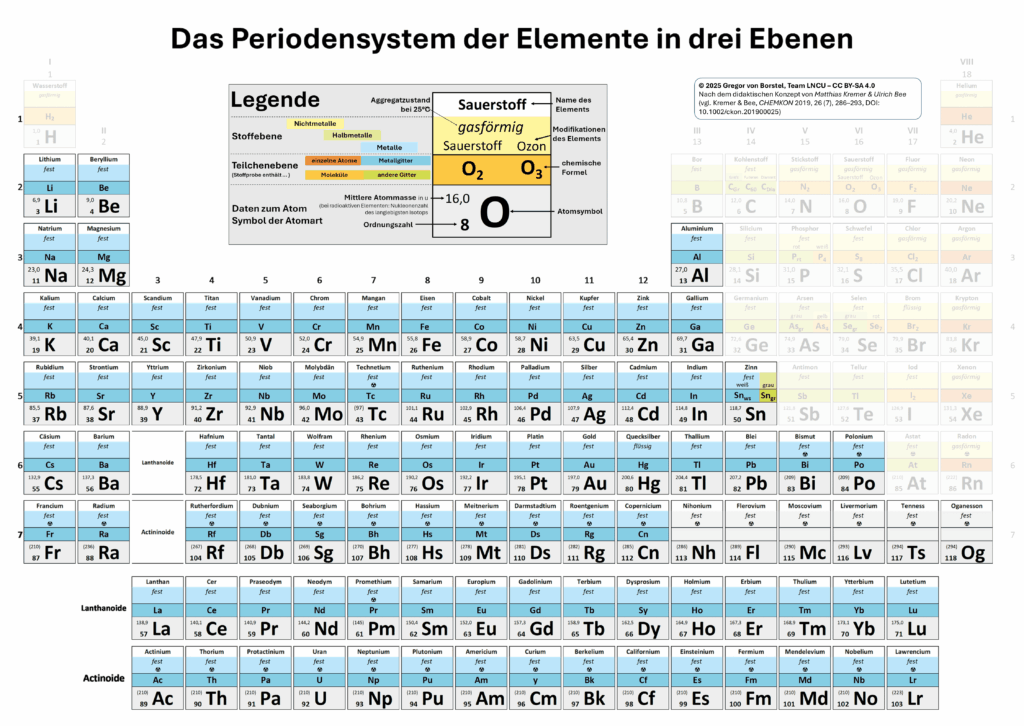
Die meisten Elemente gehören zur Kategorie der Metalle
Die Metalle im PSE3.1
Weiteres
Schaue noch einmal genauer in das Periodensystem PSE³. Schätze ab, wie groß der Anteil der Element ist, die auf Stoffebene Metalle sind und auf Teilchenebene eine metallische Bindung eingehen.
Weiteres
Erinnerst du dich, was alle Stoffe kennzeichnet, die zur Kategorie Metalle gehören?
Beispiel Kupfer
Diverse Kupferstücke2
Kennzeichen aller Metalle
Verformbarkeit, elektrische Leitfähigkeit, Wärmeleitfähigkeit, Glanz
Wie kann ein Stoff gleichzeitig stabil, verformbar und leitfähig sein?
Aufgabenstellung zur Erkundung
- Benenne mit Hilfe von M1 die Eigenschaften, die allen Metallen gemeinsam sind.
- Mache dich mit dem „Elektronengas-Modell“ in M2 vertraut.
- Öffne die Animation zur Abb. 2 und nutze die Anleitung in der Sprechblase. Erkläre, was mit den verschiedenen „Kugeln“ in dieser Animation dargestellt werden soll.
Arbeitsteilige Erarbeitung
- Gruppe A Erläutere basierend auf dem Modell die elektrische Leitfähigkeit eines Metall.
- Gruppe B Erläutere basierend auf dem Modell die Verformbarkeit eines Metall.
Wie soll ich das machen?
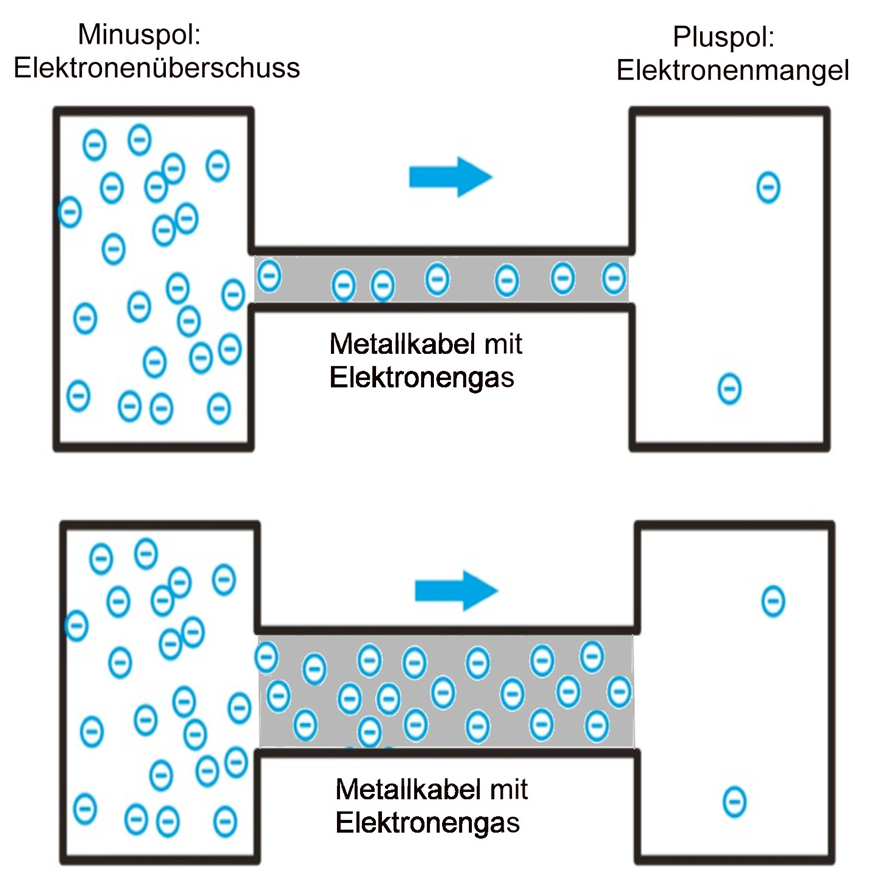
Elektrische Leitfähigkeit bedeutet auf Teilchenebene, dass sich Elektronen durch das Metallgitter bewegen können. Verformbarkeit bedeutet auf Teilchenebene, dass sich die Teilchen neu anordnen, ohne den Zusammenhalt zu verlieren.
Du kannst die Animation nutzen. Schau sie dir gut an und schreibe dir ein paar Stichworte auf, die du später vortragen kannst.
Lass die Animation für die Klasse ablaufen und erläutere begleitend, was beim Verformen (Stromleiten) auf Teilchenebene mit dem Metallgitter bzw. de Elektronengas passiert.
Elektrische Leitfähigkeit bedeutet auf Teilchenebene, dass sich Elektronen durch das Metallgitter bewegen können. Verformbarkeit bedeutet auf Teilchenebene, dass sich die Teilchen neu anordnen, ohne den Zusammenhalt zu verlieren.
Hier eine ausführliche Beschreibung der Methode „Filmleiste“.
Kurzbeschreibung: Du kannst die Standbilder nutzen.
- Mache je ein Bildschirmfoto von zwei oder drei aufeinanderfolgenden Zuständen (oder zeichne sie selbst).
- Lege die Bilder in einen Art Filmsteifen nebeneinander.
- Zeichne gegebenenfalls noch etwas hinzu (einen Hammer, ein Elektron hinein/hinaus, Pfeile für Bewegung oder etwas anderes).
- Notiere einen erklärenden Text neben deinen Bildern.
- Erläutere dann in deinem Vortrag mit Bild und Text, was beim Verformen (Stromleiten) auf Teilchenebene mit dem Metallgitter bzw. de Elektronengas passiert.
Die metallische Bindung im Modell
Das sogenannte Elektronengas-Modell
In Metallen sind die Atome dicht und regelmäßig angeordnet.
Die eigentlichen Valenzelektronen jedes Atoms werden nur schwach gebunden und können das Atom verlassen, um in den Anziehungsbereich andere Kerne zu gelangen. Unzählige Metallatome bilden daher ein Gitter aus positiven Atomrümpfen umgeben von einem verbindenden „Elektronengas“.
Ein Modell der metallischen Bindung.3
Diese Animation findest du bei LEIFIchemie. Lass uns gemeinsam darüber sprechen, was die blauen und die lilafarbenen Kreise symbolisieren.
Das Modell erklärt die Eigenschaften
Das Elektronengasmodell kann u. a. die Verformbarkeit und die elektrische Leitfähigkeit von Metallen erklären.
Eine Blechdose wird verbeult. Link auf eine Animation.4
- Nutze den Link hinter dem Bild.
- Starte die Animation mit „ruffle“, drücke den Playbutton, wähle unten im Menü L für „Ladungen einblenden“.
- Betrachte beide Animationen: „Metallbindung“ zeigt die Verformbarkeit und „elektrische Leitfähigkeit“ den Stromfluss im Metall.
Wir halten fest
- Beschreibe den typischen Aufbau eines Metalls auf Teilchenebene mit eigenen Worten.
- Ein Metallgitter besteht aus einer nicht vorstellbar großen Zahl von Metallatomen. Wenn man die Formel dafür aufschreiben will, versucht man den kleinsten Baustein zu beschreiben: Schau noch einmal in das PSE³. Wie lautet die Formelschreibweise für ein Metall?
Deutlich weitergedacht
- Nutze M3, um zu erklären, warum nicht die Atome aller Stoffe auf Teilchenebene eine metallische Bindung eingehen.
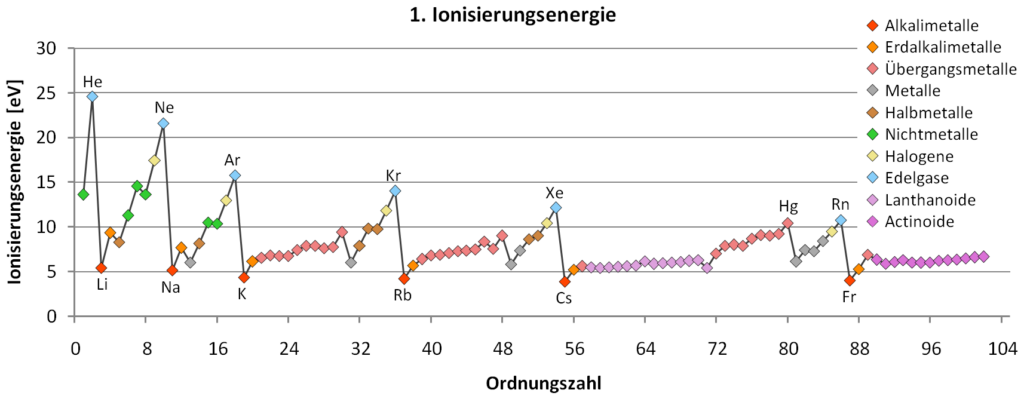
- Stelle basierend auf dem Schalenmodell und dem Begriff der Ionisierungsenergie eine Vermutung auf, warum nur die Valenzelektronen eines Metallatoms an der metallischen Bindung beteiligt sind. Überlege: was musst du recherchieren, um deine Vermutung exemplarisch prüfen zu können.
- Erkläre mit Hilfe der Abbildungen in der Galerie 2 und unserem Modell ob dicke oder dünne Kabel den elektrischen Strom besser leiten und warum dünne Kabel bei zu starkem Stromfluss zu glühen beginnen und im Extremfall schmelzen.
- Erkläre den Kurvenverlauf im Diagramm der Galerie 3 auf Teilchenebene in unserem Modell. Bedenke, was beim Erwärmen des Stoffes mit den Atomrümpfen passiert. Erläutere mit Hilfe des Diagramms, warum Computer zur Leistungssteigerung über ein Kühlsystem verfügen.
Material
Weiteres
Absolute Werte für die erste Ionisierungsenergien5