Veränderung der Kohlenstoffdioxidkonzentration in der Atmosphäre
Weiteres
In den vergangenen Jahrzehnten stieg die Konzentration von Kohlenstoffdioxid in der Atmosphäre durch die zunehmende Verbrennung fossiler Brennstoffe enorm an. Aufgrund der Wirkung als Treibhausgas hat dies enorme Folge.
Und die Konzentration des Kohlenstoffdioxids wäre wahrscheinlich ohne die Meere noch rasanter angestiegen. Expert:innen gehen davon aus, dass die Weltmeere in den letzten Jahrzehnten einen großen Teil des zusätzlich in die Atmosphäre gebrachten Kohlenstoffdioxids aufgenommen haben.
Weiteres
Durch die Erhöhung des Kohlenstoffdioxidgehalts der Atmosphäre wird es also nicht nur wärmer auf der Erde. Zugleich verändert sich auch die Oxonium-Ionenkonzentration und damit der pH-Wert der Ozeane.
Welche Auswirkungen dies für Lebewesen konkret hat, werden wir noch sehen. Zuerst wollen wir wollen experimentell prüfen, ob die Erhöhung der Konzentration von Kohlenstoffdioxid über einer wässrigen Lösung, die Menge an gelöstem Kohlenstoffdioxid und der pH-Wert der Lösung tatsächlich zusammenhängen.
Lass uns dann direkt auch die Erniedrigung betrachten. Man plant ja irgendwie auch Kohlenstoffdioxid aus der Atmosphäre wieder zu entfernen. Würde das zugleich eine Versauerung der Meere verringern?
Aufgaben
- Erklären Sie mit Hilfe von M2, warum wir zur experimentellen Prüfung der Aussagen aus M1
- sowohl die Konzentration an Kohlenstoffdioxid in der Gasphase erhöhen können wie in V1,
- als auch den Druck von Kohlenstoffdioxid durch ein Vergrößern der Gasphase erniedrigen können wie in V2 .
- Führen Sie in einer kleinen Gruppe die Versuche V1 und V2 direkt hintereinander durch. Alternativ steht eine Videografie beider Experimente in V2 mit zur Verfügung.
- Legen Sie zwei Versuchsprotokolle (Beginn jeweils via copy & paste) an und halten Sie darin alle Beobachtungen fest.
- Schlussfolgern Sie Schritt für Schritt, welchen Zusammenhang die beiden Versuche zwischen einer Veränderung der Konzentration von Kohlenstoffdioxid c(CO2) oder des Drucks von Kohlenstoffdioxid p(CO2) in der Gasphase und dem pH-Wert der wässrigen Lösung darunter zeigen. Nutzen Sie die fünf Schritte, die in den Anregungen vorgegeben sind.
Anregungen für eine Schlussfolgerung
Zu Beginn liegt ein Gleichgewicht zwischen gasförmigem (atmosphärischem) Kohlenstoffdioxid und gelöstem Kohlenstoffdioxid vor.
Daran sind weitere Gleichgewichte gekoppelt. Die Konzentration der Oxonium-Ionen im Wasser ist so gering, dass der pH-Wert größer als 5,2 (wahrscheinlich sogar ca. 7) beträgt. Dies erkennt man unter anderem daran, dass …
Man erhöht massiv die Konzentration an gasförmiges Kohlenstoffdioxid in der Gasphase über der Lösung.
Das erste Gleichgewicht gestört. Es folgt eine Vergrößerung der Konzentration an gelöstem Kohlenstoffdioxid, was man daraus schließen kann, dass
Auch die daran gekoppelten Gleichgewichte werden gestört. Es kommt einer Erhöhung der Konzentration der Oxonium-Ionen (Erniedrigung des pH-Wertes), erkennbar …
Ein neues Gleichgewicht stellt sich ein. Wir messen zwar keine direkten Konzentrationen, können dies aber daran erkennen, dass …
Im Vergleich zum vorherigen Gleichgewicht zu Beginn sind sowohl … als auch …
Wir stören erneut das Gleichgewicht in dem wir nun das Volumen der Gasphase extrem vergrößern. Dadurch verringert …
… Gleichgewicht … Das erkennen wir daran …
Konzentration und Druck eines Gases
Infokasten: Konzentration und Druck bei Gasen
Konzentrationsangaben in der Luft erfolgen oft in ppm oder Vol%:
- ppm (parts per million) gibt an, wie viele Teilchen eines Stoffes unter 1 000 000 Teilchen Luft vorhanden sind (z. B. 420 ppm CO2).
- Vol% (Volumenprozent) gibt an, wie viel Volumenanteil ein Gas am Gesamtvolumen hat (z. B. 21 Vol% O2).
Der Druck in Gasen hängt aber zugleich davon aber, wie viele Teilchen sich in einem bestimmten Volumen befinden.
Bei konstanter Temperatur sind Druck und Konzentration proportional.
Merke:
- Mehr Teilchen pro Volumen führen zu einem höheren Druck.
- Mehr Teilchen im gleichen Raum → mehr Stöße → höherer Druck.
Wer es noch genauer wissen will: Partialdruck
In unserer Atmosphäre üben alle Gasteilchen zusammen einen bestimmten Gesamtdruck1 aus. Auf Meereshöhe beträgt er etwa 101 Kilopascal (kPa).
Jedes einzelne Gas im Gemisch trägt zu diesem Gesamtdruck bei – seinen Anteil bezeichnen wir als Partialdruck. Addiert man also die Partialdrücke aller Gase in der Luft (Stickstoff, Sauerstoff, Kohlenstoffdioxid, etc.), ergibt sich der Gesamtdruck.
Der Anteil an CO2 macht heute beispielsweise etwas mehr als 0,04 % der Luft aus. Sein Partialdruck berechnet sich als Anteil am Gesamtdruck: 101 kPa · 0,0004 = 0,04 kPa. Dies bedeutet, dass von dem gesamten Druck, den wir spüren, nur 0,04 kPa vom CO2 stammen. Und wenn wir vom „CO2 -Anstieg“ in der Atmosphäre sprechen, meinen wir eigentlich die Erhöhung seines Partialdrucks.
Der Partialdruck spielt eine zentrale Rolle u. a. bei vielen biologischen Vorgängen. Beispielsweise nutzen wir beim Atmen unterschiedliche Partialdrücke für den Gasaustausch in der Lunge. CO2 bewegt sich dabei von Orten höheren Partialdrucks (Blut) zu Orten niedrigeren Partialdrucks (Lungenalveolen).
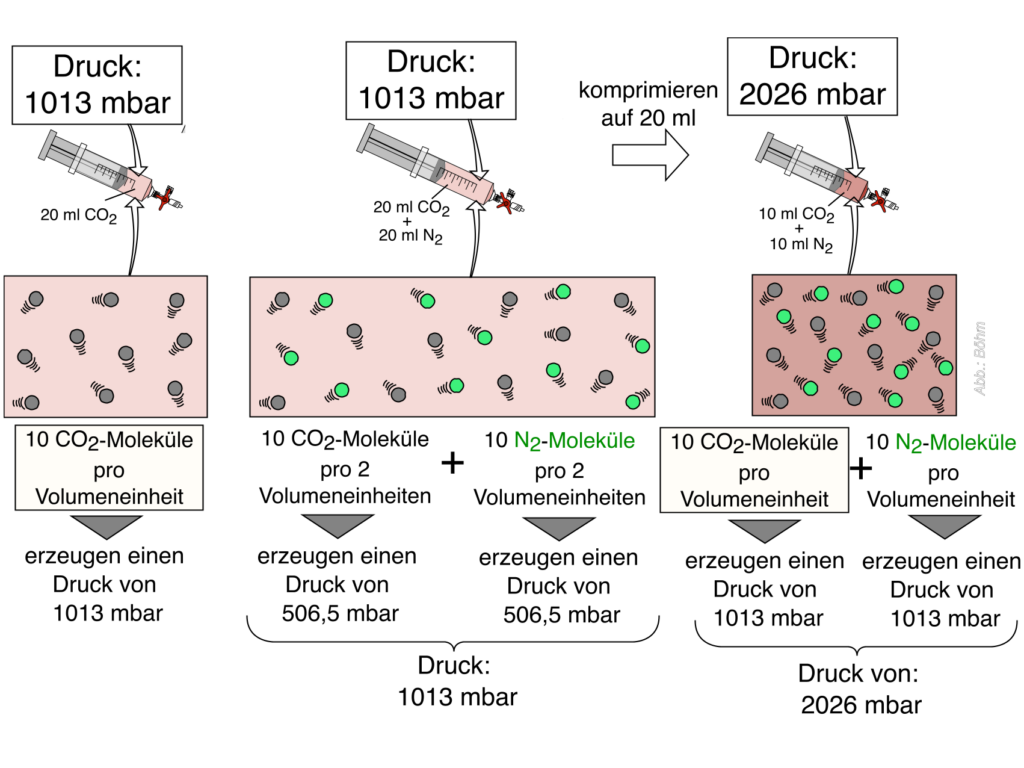
Zusammenhang von Druck und Partialdruck2
Erhöhung der Kohlenstoffdioxidkonzentration
Versuchsfrage und -design
Was bewirkt eine Konzentrationserhöhung des Gases über der wässrigen Lösung? Wir tauschen einmal die Luft über der Flüssigkeit gegen reines Kohlenstoffdioxid aus, um dies zu testen.
Materialien
- Schutzbrille
- Becherglas 400 mL
-
Spritze 30 mL
- mit 10 mL wässriger Indikator-Lösung befüllen
-
Spritze 12 mL
- mit 10 mL Kohlenstoffdioxid befüllen
- Dreiwegehahn
Chemikalien
- Wasser
-
Mischindikator Nr. 5 in Ethanol
- auch Tashiro-Indikator, Farbumschlag bei ca. pH 5,2
-
Kohlenstoffdioxid
- Von der Lehrkraft einzufüllen
Aufbau und Durchführung
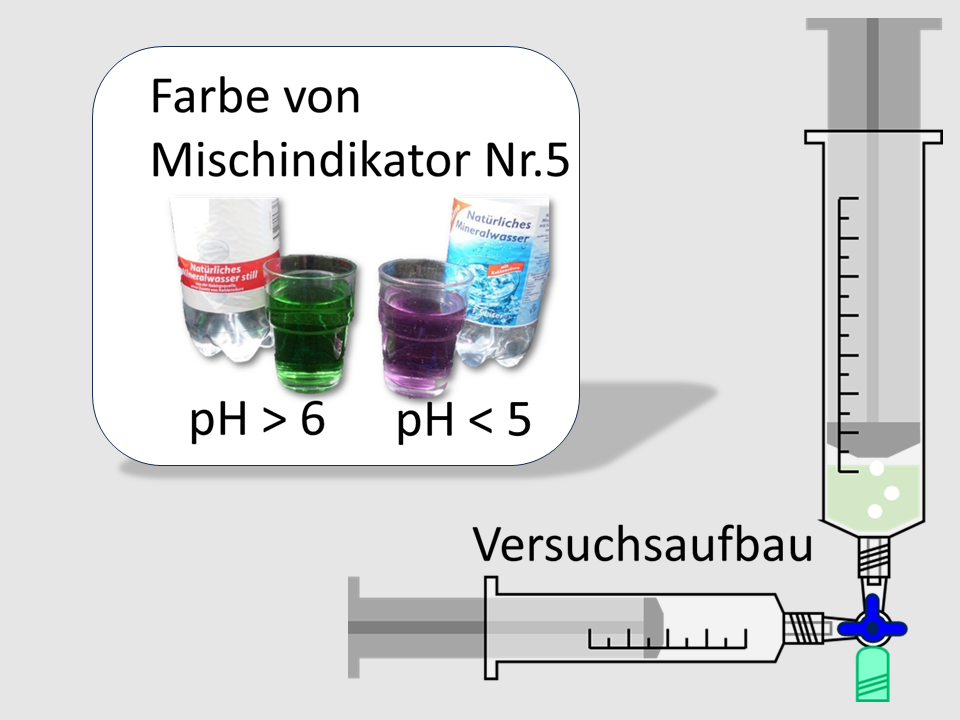
Versuchsaufbau und Farbe des Indikators bei verschiedenene pH-Werten.3
- In einem Becherglas für alle werden so viele Tropfen Indikator zu 200mL Wasser gegeben, dass eine deutliche Grünfärbung wahrnehmbar ist.
- Aus dem Becherglas werden 10 mL der Lösung in einer 30 mL Spritze aufgezogen.
- Die 12 mL Spritze wird aus einem Spender mit Kohlenstoffdioxid befüllt.
- Über den 3-Wegehahn gibt man das Kohlenstoffdioxid zu der wässrigen Indikatorlösung in die 30 mL Spritze. Dies simuliert eine extreme Anreicherung der Atmosphäre mit Kohlenstoffdioxid. Der Hahn wird verschlossen und die kleine Spritze abgeschraubt. Durch Schütteln kann man eine Wellenbewegung des Oberflächenwassers simulieren.
- Beobachten Sie, ob sich das Volumen des Gases Kohlenstoffdioxid verringert oder es zu einem Farbwechsel der wässrigen Lösung mit Indikator kommt.
Entsorgen und Aufräumen
-
Die Lösung in der 30 mL Spritze wird in Versuch 2 weiter benötigt.
Verringerung des Drucks in der Gasphase
Versuchsfrage und -design
Was bewirkt nachfolgend eine Druckerniedrigung des Gases über der wässrigen Lösung? Wir vergrößern einmal das Volumen der Gasphase über der Flüssigkeit, um dies zu testen.
Materialien
- Schutzbrille
-
Spritze 30 mL
- mit wässriger Indikator-Lösung aus V1 befüllt
- Spritze 12 mL
- Dreiwegehahn
- Kombiverschlussstopfen
Chemikalien
-
wässrige, kohlenstoffdioxidhaltige Lösung aus V1
- enthält Tashiro-Indikator, Farbumschlag bei ca. pH 5,2
Ersatzweise
Zugabe von Kohlenstoffdioxid und anschließende Druckverminderung4
Aufbau und Durchführung
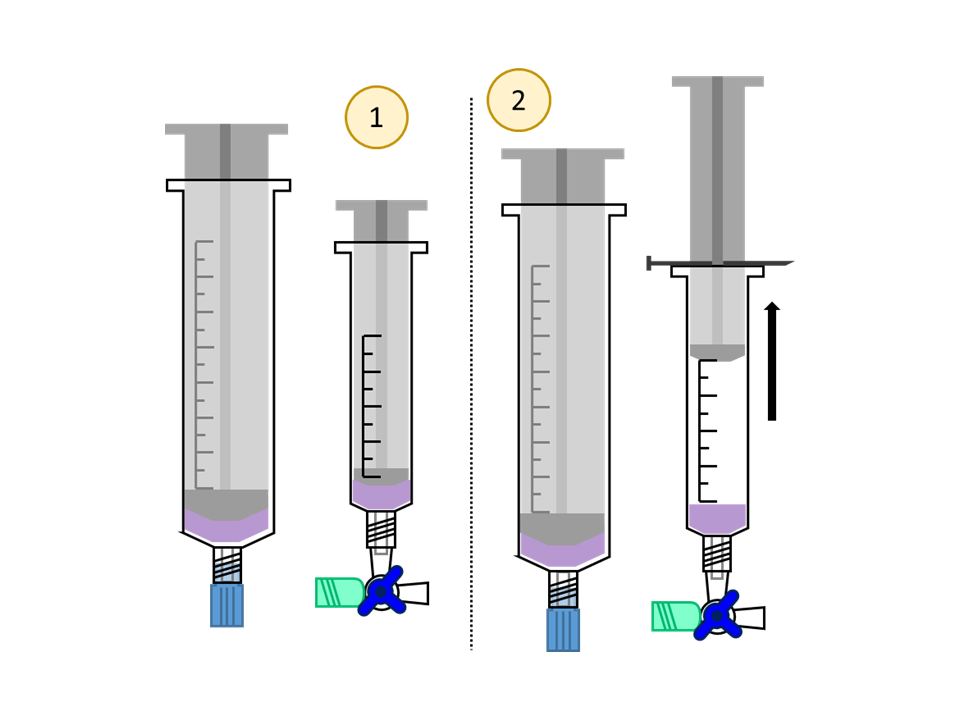
Versuchsaufbau zur Druckverminderung über der Lösung3
- Verbinden Sie die Spritzen erneut über den 3-Wegehahn und geben Sie aus der 30 mL Spritze ca. 2 mL der gefärbten Lösung zurück in die 12 mL Spritze.
- Die 30 mL Spritze wird abgenommen, verschlossen und zum Farbvergleich bei Seite gelegt.
- Der Stempel der kleinen Spritze wird maximal herausgezogen und festgehalten. Dieser kann wahrweise mit einem Nagel arretiert werden, sofern ein Loch im Stempel vorhanden ist.
- Schütteln Sie die Spritze, um eine Bewegung des Oberflächenwassers zu simulieren.
- Beobachten Sie, ob Gasblasen aufsteigen oder es zu einem Farbwechsel kommt.
Entsorgen und Aufräumen
-
Reste in den Ausguss geben und mit viel Wasser nachspülen.
-
Geräte mit Wasser spülen und an der Luft trocknen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.